Миома матки является основной причиной обращения женщин позднего репродуктивного возраста к гинекологу. Эта доброкачественная опухоль встречается не менее чем у 20–25% женщин [1] и, в зависимости от размеров, может вызывать различные клинические проявления, включая дисменорею, меноррагию, железодефицитную анемию, бесплодие, тазовую боль или симптомы сдавления смежных органов [2, 3].
На сегодняшний день не существует медикаментозной терапии, способной полностью избавить пациентку от миомы матки; по этой причине очень часто выбор гинекологов склоняется в пользу хирургического лечения [4]. Лекарственным препаратам отводится ограниченная роль в предоперационной подготовке для купирования метроррагии и анемии, уменьшения размеров миоматозных узлов [5]. С этой целью преимущественно используются комбинированные оральные контрацептивы (КОК), прогестины (Прг), агонисты гонадотропин-рилизинг гормона (АГнРГ), селективные модуляторы прогестероновых рецепторов (СМПР), препараты железа и нестероидные противовоспалительные средства (НПВС) [5–8].
 В последние несколько лет появляется все больше публикаций об использовании такого представителя СМПР, как улипристала ацетат (УПА), обладающего способностью модулировать проапоптотические и пролиферативные процессы в клетках миоматозных узлов [9–12] и приводить к уменьшению не только клинических симптомов заболевания, но и размеров опухоли.
В последние несколько лет появляется все больше публикаций об использовании такого представителя СМПР, как улипристала ацетат (УПА), обладающего способностью модулировать проапоптотические и пролиферативные процессы в клетках миоматозных узлов [9–12] и приводить к уменьшению не только клинических симптомов заболевания, но и размеров опухоли.
Изначально УПА рассматривался как препарат для предоперационной подготовки [9, 10]. Однако результаты клинических наблюдений продемонстрировали, что в ряде случаев по окончании 3-месячного курса терапии пациентки были настолько удовлетворены результатами лечения, что отказывались от хирургического вмешательства. Проведенные вслед за этим исследования PEARL 3 и 4 [11, 12] показали эффективность и безопасность от двух до четырех повторных курсов лечения.
Таким образом, УПА можно рассматривать как препарат, дающий потенциальную возможность женщинам, не желающим подвергаться хирургическому лечению, избежать операции.
Цель исследования: оценка динамики сокращения миоматозных узлов у пациенток с миомой матки, получавших терапию УПА. Дополнительно была проведена оценка профиля безопасности УПА.
Материал и методы исследования
Наш опыт применения СМПР включает наблюдение за 91 пациенткой с миомой матки, принимавших УПА в дозе 5 мг в сутки на протяжении 3 месяцев.
В исследование вошли пациентки в возрасте 25–40 лет с множественной миомой матки общим размером 250–400 см3, которым планировалось выполнение миомэктомии. В исследование не включались пациентки, которые получали гормональную терапию в течение 6 месяцев до исследования; при наличии гиперпластических процессов эндометрия; предраковых поражений шейки матки, раковых заболеваниях любой локализации в настоящее время или в анамнезе. Не вошли в исследование женщины, ранее перенесшие эмболизацию маточных артерий или ФУЗ-аблацию; имеющие эндокринные заболевания в стадии декомпенсации.
При обследовании пациенток помимо традиционной оценки антропометрических параметров, общего и гинекологического анамнеза, истории заболевания, проводилось трансвагинальное и трансабдоминальное ультразвуковое исследование (ТВ УЗИ, ТА УЗИ) органов малого таза в режимах В, ЦДК и PW на 5–7-й день менструального цикла на аппарате DC-8 фирмы Mindray конвексным датчиком С5-2Е 1,3–6,0 МГц радиусом 51 мм, линейным датчиком L12–3E3,0–13,0 МГц 38 мм и внутриполостным мироконвексным датчиком 2,6–12,8 МГц, 11 мм. ТА УЗИ осуществляли серией продольных, поперечных и косых сканирований, позволяющих измерить длину, ширину, передне-задний размеры матки при ее размерах, превышающих 12-недельный срок беременности. С целью оценки динамики сокращения размеров узлов оценивался их объемный размер до и после окончания 3-месячного курса лечения. При множественной миоме матки, рассчитывался объем трех наиболее крупных из них.
 Всем пациенткам в начале и по окончании лечения было выполнено клиническое исследование крови, исследование биохимических параметров, отражающих состояние углеводного и липидного обмена, исследование свертывающей системы крови. Также проводилось гистологическое исследование аспиратов слизистой оболочки тела матки до начала терапии и по ее окончании. Пациентки были проинформированы о возможных побочных эффектах терапии и фиксировали их в дневниках наблюдения.
Всем пациенткам в начале и по окончании лечения было выполнено клиническое исследование крови, исследование биохимических параметров, отражающих состояние углеводного и липидного обмена, исследование свертывающей системы крови. Также проводилось гистологическое исследование аспиратов слизистой оболочки тела матки до начала терапии и по ее окончании. Пациентки были проинформированы о возможных побочных эффектах терапии и фиксировали их в дневниках наблюдения.
Результаты исследования
Сразу по окончании терапии 37 пациенток (40,6%) отказались от хирургического вмешательства, так как были удовлетворены результатами лечения. Наблюдение за ними было продолжено на протяжении дополнительных 6 месяцев. По прошествии этого времени от операции продолжали отказываться 5 пациенток (5,5% общего числа), а остальным 32 была проведена планировавшаяся раньше миомэктомия с временной окклюзией маточных артерий [13]. В большинстве случаев (n=21) причиной вмешательства стало возобновление аномальных маточных кровотечений. У остальных 11 женщин отмечалось бессимптомное восстановление первоначальных размеров узлов, и они отказались от продолжения медикаментозной супрессивной терапии, отдав предпочтение хирургическому лечению. В среднем, от момента начала лечения до операции проходило 8±0,2 месяца, из которых 3 месяца соответствовали периоду активной терапии.
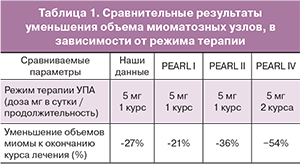
Таким образом, по нашим данным, проведенное лечение позволило отсрочить хирургическое вмешательство у 40% больных, однако этот эффект не был стойким и через полгода по окончании терапии лишь 5,5% женщин не нуждались в операции. Вероятно, их число могло бы быть больше, если бы гормональная терапия была продолжена путем проведения повторного курса лечения препаратами из группы СМПР или аГнРГ. В пользу этого предположения свидетельствуют данные исследования PEARL 4 [12] (табл. 1), в котором было зафиксировано более значимое уменьшение размеров узлов после двух курсов 3-месячного лечения по сравнению с одним.
По данным наших наблюдений по окончании 3 месяцев терапии объем узлов уменьшился на 27,2% (табл. 1). На фоне лечения к концу первого месяца аменорея развилась у 32 пациенток (35,2%), а к окончанию курса лечения – у 65 пациенток (71,4%).
Таким образом, УПА в дозе 5 мг/сут обеспечил достижение аменореи у значительного числа женщин (71%) к концу третьего месяца терапии, что можно считать важным терапевтическим эффектом для пациенток, страдающих аномальными маточными кровотечениями на фоне миомы матки и нуждающихся в отсроченном хирургическом лечении.
При оценке профиля безопасности ни у одной из пациенток нами не было выявлено статистически значимых изменений уровня триглицеридов, холестерина, липопротеидов низкой, очень низкой и высокой плотности, глюкозы. Также не было значимых изменений показателей свертывающей системы крови.
Анализ профиля переносимости показал, что 42,9% пациенток испытывали различные побочные эффекты терапии (табл. 2). В нашей серии наблюдений не было зарегистрировано ни одного случая маточных кровотечений или экспульсии миоматозных узлов. Среди незначительных побочных эффектов чаще всего пациентки отмечали приливы (19,8%), нагрубание молочных желез и головные боли (5,5%).
Заключение
Полученные данные об эффективности и безопасности применения УПА подтверждают полученные ранее результаты в исследованиях PEARL I, II, III, IV. При хорошем клиническом профиле переносимости и безопасности УПА в дозе 5 мг/сут обеспечил уменьшение узлов на 27% и достижение аменореи у 71% женщин к концу третьего месяца терапии, что можно считать значимым терапевтическим эффектом.



