Преждевременная недостаточность яичников (ПНЯ) – это клинический синдром, характеризующийся гипергонадотропной аменореей и прогрессивным снижением уровня половых гормонов вследствие потери функциональной активности яичников у женщин до 40 лет [1, 2]. Диагноз ПНЯ ассоциируется с ранней потерей фертильности, эмоциональными и сексуальными нарушениями, последствиями эстрогенодефицита на системном уровне и повышенным риском развития возраст-ассоциированных заболеваний у еще молодых женщин [2].
Клинические проявления эстрогенодефицита, характерные для ПНЯ, имеют особенности и не являются идентичными симптомам, характерным для классического климактерического синдрома [2, 3]. Интенсивность большинства симптомов, по данным литературы, не снижается с возрастом, как в случае с естественной менопаузой [4]. Молодые женщины с ПНЯ в течение длительного времени испытывают состояние хронического стресса, что во многом обусловлено психотравмирующим эффектом поставленного диагноза и нежеланием его принять. Все это существенным образом отражается на качестве жизни пациенток, что подтверждают результаты недавнего метаанализа, в котором качество жизни, связанное со здоровьем, у женщин с ПНЯ было ниже, чем у женщин того же возраста с сохраненной функцией яичников [5]. Важно отметить, что снижение качества жизни было выявлено даже среди пациенток, которые регулярно принимали заместительную гормональную терапию (ЗГТ).
В 2014 г. американские ученые на основании проведенного ими исследования сделали вывод о том, что женщины с ПНЯ испытывают значительный спектр менопаузальных симптомов и имеют потенциальную неудовлетворенность проводимым лечением [6]. ЗГТ как основная стратегия в лечении данной патологии призвана восполнять дефицит половых гормонов и компенсировать утраченную функцию яичников до возраста естественной менопаузы [7]. В идеале эта терапия должна адекватно восполнять дефицит эстрогенов, полностью купировать связанные с ним симптомы, предотвращать или существенно замедлять процессы преждевременного старения и удовлетворять самих пациенток.
В настоящее время особое внимание специалистов медицины уделяется вопросам субъективной оценки пациентами оказываемой им медицинской помощи, а также вопросам удовлетворенности терапией. Данный показатель – это степень, в которой пациенты считают, что лечение удовлетворяет их потребности в отношении здоровья [8]. Он косвенно отражает эффективность применяемой терапии и в значительной мере может оказывать влияние на степень приверженности к ней.
В исследовании, результаты которого были опубликованы в 2016 г., 52% пациенток с ПНЯ имели субоптимальные показатели приверженности лечению: женщины или никогда не принимали ЗГТ, или начинали терапию спустя длительное время после постановки диагноза, либо отказывались от продолжения терапии, находясь в возрасте моложе 45 лет [9]. В данной работе не проводился анализ причин полученных результатов, однако, обобщая выводы последних исследований по вопросам лечения пациенток с ПНЯ, можно обозначить основные нерешенные на сегодняшний день проблемы в этой области: отсроченная постановка диагноза, неудовлетворительные показатели приверженности к терапии, сохраняющиеся симптомы дефицита эстрогенов у ряда пациенток и низкие показатели качества жизни, несмотря на проводимую ЗГТ.
На сегодняшний день остается открытым вопрос об оптимальных дозах ЗГТ, которые следует рекомендовать пациенткам с ПНЯ. Сразу в нескольких руководящих документах ряда медицинских сообществ имеются указания, что для удовлетворения потребностей в отношении здоровья молодых женщин с ПНЯ могут понадобиться более высокие дозы гормональных препаратов, чем те, которые применяются у женщин в пери- и постменопаузе [2, 7, 10].
На наш взгляд, изучение показателей удовлетворенности терапией пациенток с ПНЯ – крайне важная задача. Во-первых, это является неотъемлемой частью концепции пациент-ориентированного подхода в медицине. Во-вторых, это сможет помочь врачам в правильном выборе адекватной гормональной терапии для обеспечения высокого качества жизни и успешной профилактики возраст-ассоциированных заболеваний в данной когорте пациенток.
Материалы и методы
Было проведено одномоментное исследование среди женщин, проходивших обследование и/или лечение в отделении гинекологической эндокринологии НМИЦ АГП им. В.И. Кулакова в период с 2016 по 2021 гг. Исследование было одобрено этическим комитетом Центра. Все участники подписали письменное (в случае очного интервью) или дали устное (в случае телефонного интервью) согласие на добровольное участие в опросе.
В исследование включали пациенток от 18 до 45 лет с установленным не менее 12 месяцев назад диагнозом ПНЯ и принимавших ЗГТ в непрерывном режиме в течение не менее 3 последних месяцев. Диагностические критерии ПНЯ соответствовали принятым в 2016 г. Европейским обществом репродукции и эмбриологии человека и включали: олиго/аменорею в течение не менее 4 месяцев, уровни фолликулостимулирующего гормона (ФСГ) >25 мМЕ/л, подтвержденные дважды с интервалом в 4–6 недель, возраст пациенток до 40 лет [11]. В исследование не включали пациенток с ятрогенной ПНЯ, изменениями кариотипа, историей онкологического заболевания в анамнезе, тяжелой соматической патологией, нарушениями функции щитовидной железы и надпочечников, наличием противопоказаний к ЗГТ.
На первом этапе в исследование были включены женщины, чьи данные находились в медицинской базе ФГБУ НМИЦ АГП им. В.И. Кулакова Минздрава России. Всего в базе были отобраны данные 350 пациенток, 296 из которых потенциально соответствовали критериям включения в исследование. С женщинами связывались по телефону, указанному в медицинской карте. 165 пациенток согласились ответить на вопросы интервью по телефону. Еще 60 пациенток были включены в исследование после посещения гинеколога на приеме в отделении гинекологической эндокринологии НМИЦ АГП им. В.И. Кулакова.
В ходе основного исследования оценку удовлетворенности пациенток терапией проводили с помощью структурированного интервью. Участницам также предлагали заполнить опросник Климактерическая шкала Грина (Greene Climacteric Scale, GCS) [12], с помощью которого оценивали тяжесть менопаузальных симптомов. Данный опросник характеризуется высокой валидностью и широко используется как в научных исследованиях, так и в клинической практике в различных странах мира [13, 14]. Степень выраженности симптомов определяется по 4-балльной шкале (от 0 баллов –нет симптома до 3 баллов – выраженное проявление симптома). При оценке результатов проводится подсчет общей суммы баллов, на основании чего выделяют легкую (11 и менее баллов), умеренную (от 12 до 19 баллов) и тяжелую (20 и более баллов) степени проявления климактерического синдрома (КС). Демографические показатели и клинические данные, а также сведения о диагностических исследованиях и проводимой фармакотерапии получали из первичной медицинской документации (амбулаторные карты) и в ходе общения с пациентками.
Для общей субъективной оценки удовлетворенности лечением пациенткам предлагали ответить на вопрос: «На сколько Вы удовлетворены Вашей текущей заместительной гормональной терапией?», выбрав один из готовых вариантов ответов: «удовлетворена полностью», «скорее удовлетворена», «скорее не удовлетворена», «не удовлетворена», «затрудняюсь ответить».
Первичной конечной точкой в данном исследовании был показатель удовлетворенности пациенток с ПНЯ заместительной гормональной терапией. Вторичными конечными точками были показатели удовлетворенности качеством медицинской помощи, уровень приверженности к лечению, частота и причины смены терапии, частота и тяжесть симптомов дефицита эстрогенов, которые сохранялись на фоне приема ЗГТ.
Статистический анализ
Статистический анализ проводили с использованием пакета прикладных программ Microsoft Office Excel 2010, IBM SPSS Statistics 25 HC IMAGO 5.0, лицензия № 5725-А54 и StatTech v. 2.0.0 (ООО «Статтех», Россия).
Количественные показатели оценивали на предмет соответствия нормальному распределению с помощью критерия Шапиро–Уилка (при числе исследуемых менее 50) или критерия Колмогорова–Смирнова (при числе исследуемых более 50). В случае нормального распределения количественные данные описывали с помощью среднего значения (M) и стандартного отклонения (SD). В случае отсутствия нормального распределения количественные данные описывали с помощью медианы (Me) и нижнего и верхнего квартилей (Q1–Q3). Категориальные данные описывались с указанием абсолютных значений и процентных долей.
Сравнение двух групп по количественному показателю, распределение которого соответствовало нормальному, выполняли с помощью t-теста Стьюдента. Сравнение двух групп по количественному показателю, распределение которого отличалось от нормального, выполняли с помощью U-критерия Манна–Уитни. Сравнение процентных долей при анализе четырехпольных таблиц сопряженности выполняли с помощью, критерия хи-квадрат Пирсона (при значениях ожидаемого явления более 10). Сравнение процентных долей при анализе многопольных таблиц сопряженности выполняли с помощью критерия хи-квадрат (χ2) Пирсона.
Для оценки диагностической значимости количественных признаков при прогнозировании определенного исхода, применяли метод анализа ROC-кривых. Разделяющее значение количественного признака в точке cut-off определяли по наивысшему значению индекса Юдена.
Результаты
Из 225 пациенток, отобранных для участия в исследовании, 223 (99,1%) ответили на все вопросы интервью, заполнили анкеты, и их данные подверглись окончательному анализу. Клинико-анамнестические и демографические данные участниц исследования представлены в таблице 1.
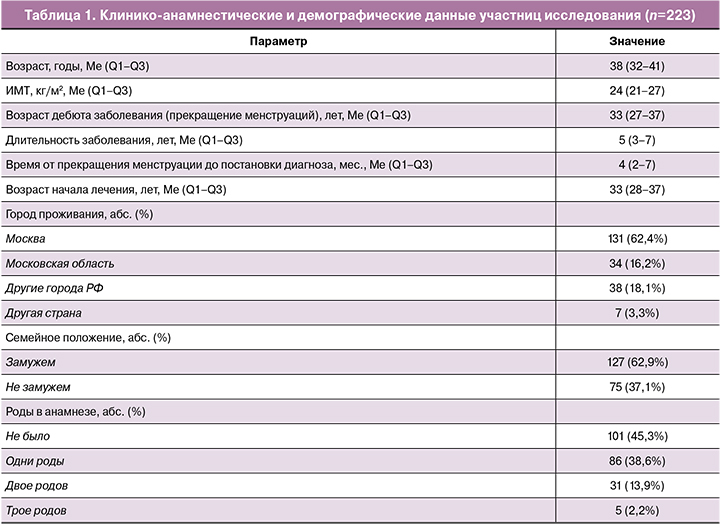
Всех участниц спрашивали об их опыте применения ЗГТ. Медиана длительности приема ЗГТ составила 4 года (2–6 лет), медиана возраста пациенток на момент начала лечения составила 33 года (28–37 лет). 17 (7,6%) участниц исследования делали хотя бы один перерыв в приеме ЗГТ. Медиана продолжительности перерывов составила 4 месяца (2–12 месяцев) с минимальным сроком 1 месяц и максимальным – 4 года. Не учитывали данные о перерывах в приеме ЗГТ по причине беременности и периода лактации у пациенток. Участниц спрашивали о причинах, по которым было приостановлено лечение. 10 (58,8%) женщин ответили, что перерыв(ы) в лечении был сделан из-за нежелания принимать ЗГТ и опасений по поводу ее негативных последствий для здоровья (в частности, возникновения онкологических заболеваний), 4 (23,5%) женщины прерывали терапию «на время для отдыха организма» либо по совету врача, либо самостоятельно, 3 (17,6%) женщины делали перерыв на 1–2 месяца из-за трудного финансового положения или отсутствия необходимых лекарственных препаратов в аптеке.
Структура препаратов ЗГТ, которую принимали пациентки на момент участия в исследовании, представлена на рисунке 1.
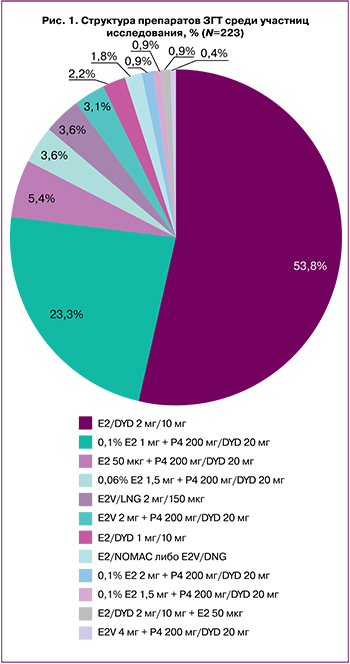
Большинство респонденток использовали ЛП, содержащие стандартную дозу эстрадиола (Е2) в составе циклической ЗГТ (комбинированные препараты или монопрепараты эстрогенов в сочетании с препаратами гестагенов): 120 (53,8%) женщин принимали пероральный препарат, содержащий 2 мг Е2 в сочетании с 10 мг дидрогестерона (E2/DYD 2 мг/10 мг), еще 52 (23,3%) пациентки применяли в качестве эстрогенного компонента ЗГТ эстрадиола гемигидрат 0,1% трансдермальный гель 1 г в сутки (0,1% E2 1 мг) в непрерывном режиме.
5 (2,2%) опрошенных женщин принимали препараты ЗГТ, содержащие низкую дозу Е2: 1 мг Е2 + 10 мг дидрогестерона (Е2/DYD 1 мг/10 мг) перорально. 4 (1,8%) женщины использовали комбинированные оральные контрацептивы (КОК) с Е2 в составе: 1,5 мг Е2 + 2,5 мг номегэстрола ацетат (E2/NOMAC 1,5 мг/2,5 мг) в режиме 24/4 и КОК с динамическим режимом дозирования эстрадиола валерата и диеногеста (E2V/DNG) в режиме 26/2.
4 (1,8%) респондентки на момент опроса применяли высокие дозировки трансдермального 0,1% геля с Е2 (0,1% E2), из них 2 (0,9%) пациентки по 2 г/сут (0,1% E2 – 2 мг) и 2 (0,9%) по 1,5 г/сут (0,1% E2 – 1,5 мг). 1 (0,4%) пациентка сообщила о приеме двойной дозы перорального препарата, содержащего эстрадиола валерат 2,0 мг (E2V 2 мг по 2 таблетки в сутки). Следует отметить, что 2 (0,9%) пациентки сообщили, что ранее принимали сочетание препаратов ЗГТ: E2/DYD 2 мг/10 мг + Е2 50 мкг и E2/DYD 2 мг/10 мг + гель с тестостероном 25 мг (Т 25 мг). Самостоятельно увеличили дозы препаратов ЗГТ 3 (1,4%) женщины, в остальных случаях – повышение дозы осуществлялось по рекомендации врача.
Среди 81 (36,3%) пациентки, которые на момент интервью применяли в непрерывном режиме трансдермальные формы эстрогенов или E2V перорально, 52 (64,2%) в качестве гестагенного компонента использовали дидрогестерон 20 мг в сутки (DYD 20 мг), 29 (35,8%) женщин применяли микронизированный прогестерон 200 мг в сутки (P4 200 мг), из них 24 (82,7%) использовали препарат Р4 вагинально и 5 (17,2%) перорально. Прогестагены применяли в циклическом режиме по 12 или 14 дней ежемесячно с последующей отменой.
В качестве основной релевантной переменной в данном исследовании была принята удовлетворенность лечением пациенток с ПНЯ. 223 женщины ответили на вопрос «Насколько Вы удовлетворены заместительной гормональной терапией, которую Вы получаете на данный момент?». Из них ответили «полностью удовлетворена» 19 (8,5%) респонденток, «скорее удовлетворена» – 101 женщина (45,3%). 53 (23,8%) женщины ответили, что «скорее не удовлетворены», а 39 (17,5%) участниц опроса были полностью «не удовлетворены» терапией. 11 (4,9%) пациенток «затруднялись» ответить на данный вопрос.
Для облегчения дальнейших расчетов и получения более обобщенных данных ответы пациенток относительно их удовлетворенности терапией были объединены в 2 категории: ответы «полностью удовлетворена» и «скорее удовлетворена» считали положительной оценкой терапии, ответы «не удовлетворена» или «скорее не удовлетворена» – отрицательной (негативной) оценкой (рис. 2). С той же целью препараты ЗГТ, которые принимали участницы исследования, были разделены в зависимости от дозы эстрогенного компонента, входящей в его состав: ЗГТ с низкой, стандартной и высокой дозой Е2 [2, 10]. КОК при этом рассматривали отдельно.
В ходе исследования был проведен анализ удовлетворенности терапией в зависимости от препарата ЗГТ, которые принимали участницы на момент исследования. Результаты данного анализа представлены в таблице 2.
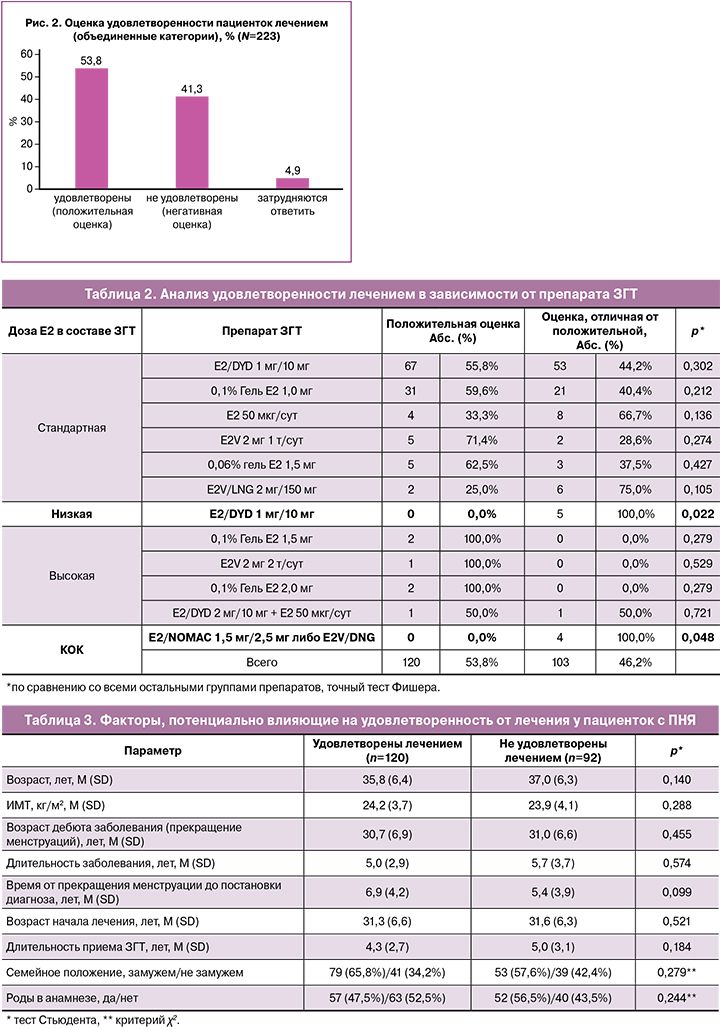
Для пациенток, которые использовали наиболее часто назначаемые препараты, содержащие стандартную дозу E2, были получены следующие показатели: 30 (57,7%) из 52 пациенток дали положительную оценку терапии 0,1% Е2 1,0 мг, и 66 (55%) из 120 пациенток – терапии Е2/DYD 2 мг/10 мг. Не было получено положительных оценок терапии от респонденток, которые принимали низкодозированную ЗГТ 1 мг/10 мг E2/DYD (0%) и КОК (E2/NOMAC 1,5 мг/2,5 мг либо E2V/DNG с динамическим режимом дозирования (0%)). Положительная оценка терапии в 100% случаев была дана пациентками, которые использовали ЗГТ с дозой Е2, превышающей стандартную (0,1% Е2 1,5 мг, 0,1% Е2 2,0 мг, E2V 2 мг по 2 таблетки в сутки в сочетании с гестагенами).
При оценке факторов, потенциально влияющих на удовлетворенность лечением (положительная и отрицательная оценки терапии), получены следующие результаты (табл. 3).
Неудовлетворительная оценка терапии не зависела от возраста пациенток, ИМТ, возраста дебюта заболевания, длительности заболевания, времени от прекращения менструации до постановки диагноза, возраста начала лечения, длительности приема ЗГТ, семейного положения, родов в анамнезе (p>0,05).
Одним из этапов исследования была оценка удовлетворенности его участниц качеством оказания медицинской помощи. Пациенткам задавали вопросы относительно сроков постановки диагноза, наблюдения у врача-гинеколога, опыта применения ЗГТ. 72 (32,3%) из опрошенных женщин дали негативную оценку качеству оказанной медицинской помощи. Среди причин неудовлетворения медицинским обслуживанием были названы: «отсроченная постановка диагноза», «отсутствие сочувствия со стороны врача», «постоянное упоминание врачом термина «менопауза», «отсутствие подробного разъяснения причин заболевания», а также «причин, по которым необходимо принимать ЗГТ», «неправильное назначение ЗГТ», по мнению пациенток.
Всех участниц исследования просили заполнить анкету GCS. Градация степени тяжести КС, согласно данной шкале, определяется простым суммированием баллов по каждому из пунктов анкеты. Медиана суммарных баллов по GCS среди всех заполнивших анкету женщин была равна 12 баллам (6–18 баллов), что соответствует средней степени тяжести КС, с минимальным количеством 0 баллов, которое оценивали как отсутствие климактерических симптомов, и максимальным количеством баллов, равным 40.
Распределение пациенток по степени тяжести КС было следующим: 89 (39,9%) участниц на момент заполнения анкеты имели проявления симптомов дефицита эстрогенов легкой степени, 87 (39,0%) – проявления средней степени тяжести, 43 (19,3%) женщины имели тяжелые клинические проявления эстрогенодефицита. Лишь 4 (1,8%) пациентки не указали на наличие какого-либо симптома из указанных в анкете.
Следующим этапом исследования было выполнение анализа показателя отрицательной оценки терапии в зависимости от общего балла по GCS. Результаты анализа представлены в таблице 4.
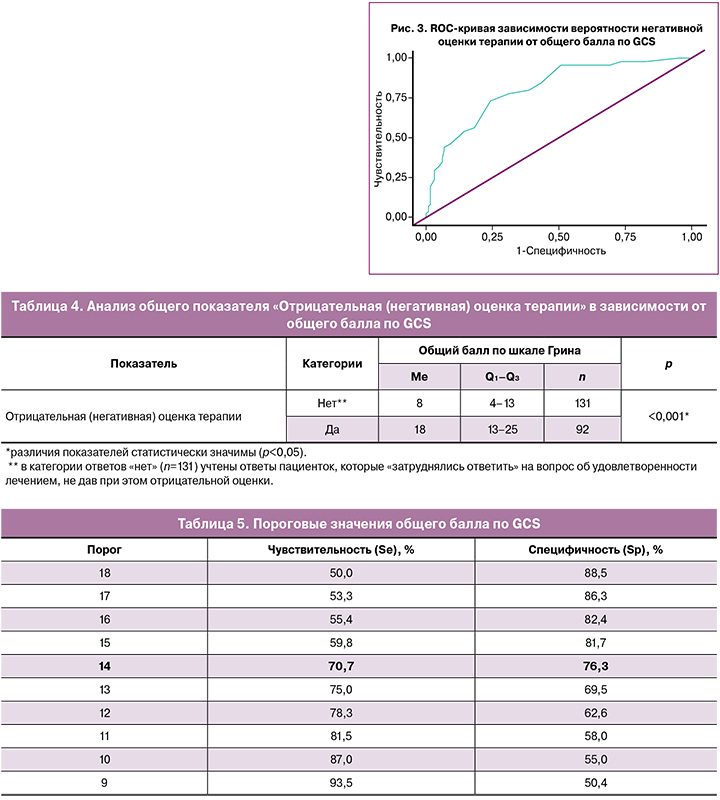
В соответствии с представленной таблицей при оценке неудовлетворенности терапией в зависимости от общего балла по GCS, были выявлены статистически значимые различия (p<0,001) (используемый метод: U-критерий Манна–Уитни). При оценке зависимости вероятности получения негативной оценки терапии от общего балла по GCS с помощью ROC-анализа была получена следующая кривая (рис. 3).
Площадь под ROC-кривой составила 0,802 (0,031) с 95% ДИ: 0,740–0,863. Полученная модель была статистически значимой (p<0,001). Пороговое значение общего балла по GCS в точке cut-off, которому соответствовало наивысшее значение индекса Юдена, составило 14 (табл. 5). Неудовлетворенность терапией прогнозировали при значении общего балла по GCS выше данной величины или равном ей. Чувствительность и специфичность модели составили 70,7 и 76,3% соответственно.
В заключительной части опроса участницам исследования, которые набрали 14 и более баллов по GCS, но были удовлетворены лечением (26 (11,7%) пациенток), задали вопрос, почему при наличии имеющихся симптомов они дали положительную оценку терапии. Среди наиболее частых ответов были: «если я не испытываю приливов, я уже довольна лечением» (8 (30,8%) пациенток), «я не верю, что мое состояние может стать лучше» (6 (23,1%) пациенток), «другая терапия не улучшила мое состояние» (5 (19,2%) пациенток), «если я отменю терапию, мне будет очень плохо» (3 (11,5%) пациентки).
Обсуждение
В нашей работе впервые в РФ проведен анализ удовлетворенности лечением пациенток с ПНЯ, а также представлены данные по частоте и тяжести симптомов эстрогенодефицита, сохранявшихся на фоне приема ими ЗГТ.
Глобальной медицинской проблемой, по данным литературы, является низкое качество коммуникации врача акушера-гинеколога и пациента с ПНЯ [2]. Высокий процент женщин остаются недовольными полученной от врача информацией о своем заболевании, а также о его последствиях для здоровья в отдаленной перспективе, целях и преимуществах использования ЗГТ, а также ее оптимальной длительности [15–17]. Данные настоящего исследования подтверждают эти выводы: более 30% опрошенных пациенток высказали неудовлетворенность качеством коммуникации с врачом, задержкой в постановке правильного диагноза, отсутствием полной информации о заболевании и низким уровнем психологической поддержки врача на приеме.
Опрос участниц исследования показал использование ими различных форм и наименований эстрадиол содержащих лекарственных средств. Следует сказать, что в РФ зарегистрировано большое количество ЛП, применяющихся в качестве заместительной (или менопаузальной) гормональной терапии у женщин. Основным показанием для них является купирование климактерических симптомов и профилактика остеопороза. По аналогии с естественной менопаузой, ввиду схожей симптоматики, женщинам с ПНЯ в большинстве случаев назначают те же схемы терапии без учета их возраста и потребностей. Почти половина женщин в нашем исследовании (53,8%) использовали в качестве ЗГТ пероральный ЛП, содержащий стандартную дозу Е2 (Е2/DYD 2 мг/10 мг). Еще 23,3% использовали в трансдермальный гель с Е2 в стандартной дозе (0,1% Е2 1,0 мг) в сочетании с гестагенами. Другие схемы терапии, в том числе ЗГТ с отличными от стандартных доз Е2, пациентки использовали значительно реже (в 5% и менее случаев).
Анализ удовлетворенности лечением показал, что «полностью удовлетворены» терапией были лишь 19 (8,5%) пациенток. С другой стороны, количество женщин, которые были «полностью не удовлетворены» принимаемой ими ЗГТ, было в 2 раза больше (39 (17,5%)). Суммарный процент неудовлетворенных терапией пациенток (41,3%) не превысил процент удовлетворенных лечением (53,8%), однако с клинической точки зрения он является слишком высоким, чтобы дать однозначную положительную оценку назначаемым сегодня дозам и схемам лечения пациенток с ПНЯ.
Удовлетворенность пациента лечением во многом является субъективным параметром. В исследованиях по поиску детерминант удовлетворенности качеством медицинской помощи и лечением выделены две группы факторов, влияющих на данный показатель. К первой группе относятся социально-культурные, психологические характеристики пациента, ко второй – характеристики деятельности медицинской организации, действий и поведения врача, а также эффективность назначаемого им лечения, которая в той или иной степени соответствует ожиданиям пациента [18, 19].
В нашей работе были выбраны факторы (возраст пациенток, ИМТ, длительность заболевания и приема ЗГТ, семейное положение, роды в анамнезе и ряд других), от которых, на наш взгляд, могла зависеть удовлетворенность лечением, однако между этими показателями не было получено положительных корреляционных связей. Это дает возможность предположить, что среди объективных показателей наибольшее влияние на удовлетворенность терапией оказывала ее клиническая эффективность, основанная на оценке своего состояния пациентками.
Самые низкие показатели удовлетворенности лечением были выявлены среди участниц исследования, которые принимали ЛП ЗГТ с низкой дозой Е2 (Е2/DYD 1 мг/10 мг), а также КОК (E2/NOMAC и Е2V/LNG). В литературе существуют ограниченные данные относительно применения КОК у пациенток с ПНЯ. В исследованиях, где эти препараты в сравнении с ЗГТ были ассоциированы с худшими результатами влияния на состояние скелета и показатели сердечно-сосудистой системы, связанные с сердечно-сосудистым риском, применяли КОК с синтетическими эстрогенами в режиме 21/7 [20]. КОК, которые принимали участницы настоящего исследования, с Е2 в составе и сокращенным безгормональным интервалом имеют лучший профиль безопасности и обеспечивают постоянный уровень эндогенного Е2 в крови, однако доза эстрогенного компонента может быть недостаточной для восполнения дефицита эстрогенов у ряда пациенток [21]. Режим использования препарата Е2V/LNG подразумевает 7-дневный перерыв, во время которого наступает менструальноподобное кровотечение. Отсутствие поступления эстрогенов в течение недельного перерыва ежемесячно вызывает резкие колебания уровня эстрогенов и может быть ассоциировано с возвращением симптомов, с чем также может быть связана невысокая удовлетворенность лечением данным препаратом. Что касается использования ЛП с низкой дозой Е2 в составе, то они не рекомендованы в качестве ЗГТ для пациенток с ПНЯ [2, 7, 10, 11].
Сопоставимые показатели удовлетворенности лечением (50–60%) были получены среди пациенток, которые принимали ЗГТ, содержащие стандартные дозы Е2 (Е2/DYD 2 мг/10 мг, 0,1% Е2 1,0 мг, 0,06% Е2 1,5 мг). Детальный анализ этих результатов, а также описание сохраняющихся симптомов эстрогенодефицита проводили на втором этапе исследования, и его данные будут приведены в следующей публикации.
Только треть пациенток (33,3%), которые использовали в качестве ЗГТ накожный пластырь с Е2 50 мкг/сут, были удовлетворены терапией. В нашей стране дозу высвобождаемого Е2 50 мкг/сут для накожного пластыря принято считать стандартной, однако в зарубежных исследованиях наиболее часто используется дозы Е2 75–100 мкг/сут. Также получены доказательства того, что доза Е2 не менее 100 мкг/сут позволяет эффективно купировать симптомы при ПНЯ и достичь средних уровней Е2 в сыворотке крови в диапазоне, характерном для молодых женщин с сохраненной функцией яичников [21].
Интерес представляют полученные данные о применении пациентками ЗГТ с высокими дозами Е2 (0,1% Е2 1,5 мг и 2,0 мг, Е2V 2 мг 2 т/сут) и добавлении дополнительных препаратов в стандартную схему ЗГТ (Е2/DYD 2 мг/10 мг + пластырь с Е2 50 мкг/сут и Е2/DYD 2 мг/10 мг + Т 25 мг, а также сообщения о самостоятельном увеличении пациентками дозы ЛП. Эти данные в совокупности с вышеизложенными результатами, позволяют предположить, что ЗГТ, содержащая низкие и в ряде случаев стандартные дозы Е2, не позволяет полностью купировать симптомы эстрогенодефицита у женщин с ПНЯ и обеспечить высокий уровень качества жизни. Показатели 100% удовлетворенности лечением только среди пациенток, которые принимали ЗГТ с превышающей стандартную дозой Е2, подтверждают эти выводы.
Одним из этапов исследования была оценка показателей, полученных в ходе заполнении пациентками GCS. Только 4 (1,8%) из опрошенных женщин не сообщили о каких-либо беспокоящих их симптомах, представленных в анкете. Процент женщин, которые ответили, что полностью удовлетворены (8,5%) или скорее удовлетворены (45,3%) лечением, превышает процент женщин, не набравших ни одного балла по GCS. Из этого следует, что положительную оценку терапии давали даже те участницы, которые на момент опроса имели те или иные клинические проявления дефицита эстрогенов.
Средний балл по GCS среди участниц исследования составил 12 баллов, что соответствует средней степени тяжести проявлений КС. При построении прогностической модели вероятности неудовлетворенности лечением в зависимости от степени проявления симптомов эстрогенодефицита, получено пороговое значение общего балла по GCS, равное 14. Полученный результат свидетельствует, что женщинам с ПНЯ необходимо испытывать существенные изменения в самочувствии, чтобы оценить их как неудовлетворенность лечением. Результаты исследования показали, что около 10% пациенток, набравших более 14 баллов при заполнении анкеты GCS, не предъявляли никаких активных жалоб на приеме. Это может быть связано как с недостаточной осведомленностью о своем заболевании, так и с имеющимся неудачным опытом смены ЛП в поисках «оптимальной» ЗГТ. Ситуация усугубляется тем, что врачи активно не спрашивают пациенток о наличии или отсутствии тех или иных симптомов. Как следствие, большинство женщин с сохраняющимися симптомами дефицита эстрогенов на фоне ЗГТ не получают адекватной помощи.
Наше исследование имеет ряд ограничений, связанных с его дизайном, при котором существует ошибка получения недостоверных или неполных данных. Регистрацию симптомов дефицита эстрогенов проводили с помощью опросника, разработанного для менопаузальных женщин, где клинические симптомы могут в той или иной степени отличаться от симптомов, характерных для ПНЯ. В данном исследовании также не учитывали потенциальное влияние гестагенного компонента ЗГТ на симптомы эстрогенодефицита, которое могло отражаться на показателях удовлетворенности лечением.
Главным преимуществом проведенного исследования являются данные, полученные непосредственно от пациенток в условиях реальной клинической практики, которые представляют ценную информацию для клиницистов и исследователей.
Заключение
Женщины с ПНЯ нуждаются в особом подходе при врачебном консультировании, который подразумевает психологическую поддержку, разъяснение общих и частных вопросов относительно заболевания, возможных отдаленных последствий эстрогенодефицита для здоровья, целей и длительности лечения, а также активное выявление, изучение и тщательный анализ жалоб, которые могут свидетельствовать о недостаточной компенсации дефицита эстрогенов на фоне приема ЗГТ.
Полученные в ходе работе результаты о высоком проценте неудовлетворенных терапией пациенток и сохраняющихся симптомах дефицита эстрогенов на фоне приема ЗГТ свидетельствуют о необходимости пересмотра подходов к тактике ведения пациенток с ПНЯ.



