В Российской Федерации (РФ) в настоящее время более 30 млн женщин старше 45 лет. Ежегодно более 1 млн женщин вступают в менопаузу [1]. Средний возраст наступления менопаузы у женщин в РФ составляет 51 год (абсолютное большинство женщин проходят этот период в возрасте 45–55 лет) [2]. Поскольку продолжительность жизни женщин значительно возросла за последние 50 лет и будет увеличиваться, то практически треть своей жизни женщины будут проводить в постменопаузе [3].
Менопауза – стойкое прекращение менструаций, обусловленное возрастным снижением гормональной активности и «выключением» репродуктивной функции яичников. Дата наступления менопаузы оценивается ретроспективно – спустя 12 месяцев отсутствия менструации [2]. По данным масштабного международного исследования «Восприятие перехода к менопаузе» (Women’s perception of the menopause transition), включившего более 7000 пациенток из разных стран мира, большинство женщин старше 45 лет связывают свои проблемы со здоровьем с менопаузой [4]. Более 90% женщин с менопаузой испытывают физические симптомы (вазомоторные симптомы/приливы жара/озноб, потливость, головные боли, сердцебиения и другие) и примерно 55% испытывают психологические симптомы (раздражительность, нарушения сна, когнитивные нарушения и др.) [4].
Наступление менопаузы тесно связано с риском проявления нарушений со стороны сердечно-сосудистой, опорно-двигательный и нервной систем. В клинической практике специалисты различных профилей, в частности акушеры-гинекологи, сталкиваются с коморбидными пациентками старше 40 лет. Именно поэтому важно сделать акцент, что в период перименопаузы и ранней постменопаузы целесообразно своевременно выявлять патогномоничные симптомы менопаузы, а также рассматривать возможные опции для профилактики и снижения последующих рисков, тем самым повышая качество жизни женщины и способствуя увеличению ее продолжительности.
Возраст наступления менопаузы. Почему важно своевременно обращать внимание на симптомы у женщин старше 40 лет?
На возраст наступления менопаузы влияют различные факторы – социально-экономические, этнические, экологические. Согласно мировой и национальной статистике, около 70% женщин в этом возрастном диапазоне испытывают один или более климактерических симптомов [2]. Средний возраст наступления менопаузы во всем мире составляет приблизительно 48,8 года [2]. Это означает, что возникающие климактерические симптомы (приливы жара, озноб, раздражительность, расстройство сна, утомляемость, набор веса и т.д.) нарушают качество жизни женщины на пике ее карьеры и семейной жизни.
Поскольку основные хронические заболевания (метаболические нарушения, включая ожирение и диабет, сердечно-сосудистые заболевания (ССЗ), остеопороз, хронический артрит, деменция и рак) возникают у женщин через 10–15 лет после начала менопаузы, существует большая возможность повлиять на траекторию этих рисков путем внедрения превентивных мер в перименопаузе [2, 3, 5], которые могут иметь существенное позитивное влияние на продолжительность и качество жизни женщин.
Помимо своевременного лечения климактерических симптомов, раннее внедрение превентивных стратегий для потенциальных хронических заболеваний приобретает еще большее значение и важность именно в период перименопаузы. Хотя термин «перименопауза» был предложен лишь в 2014 г., на сегодняшний день ведущие негинекологические профильные общества особенно отмечают важность этого периода и подчеркивают важность терапевтического вмешательства в это время [6–9].
Значимость профилактики потенциальных рисков должна первостепенно стоять у женщин с преждевременной недостаточностью яичников (ПНЯ), ятрогенной менопаузой и ранней менопаузой. Эти женщины подвергаются повышенному риску расстройств со стороны сердечно-сосудистой и центральной нервной систем, если они не получают заместительной (менопаузальной) гормональной терапии [9–14].
Симптомы менопаузы. На что стоит обратить внимание клиницисту?
В РФ показатель осознанности и осведомленности среди женщин о тягостных симптомах менопаузы недостаточен. Несмотря на то что около 80% женщин в нашей стране испытывают один или более климактерических симптомов, к врачу обращаются лишь 30% женщин [4]. Гинекологу важно выявлять жалобы у женщин старше 45 лет на нерегулярный менструальный цикл, приливы, потливость, раздражительность, набор массы тела (в среднем на 20–25% за последние несколько лет), это дает возможность своевременно корригировать эстрогенодефицит и тем самым улучшить самочувствие женщины [5].
У женщин с тяжелыми симптомами менопаузы наблюдаются неблагоприятный кардиометаболический профиль и гиперактивность симпатической нервной системы по сравнению с женщинами, у которых эти симптомы отсутствуют [15]. Вегетативная дисфункция увеличивает вариабельность сердечного ритма, что может привести к одышке при физической нагрузке [16]. В наблюдательном исследовании «Инициатива во имя здоровья женщин» (Women’s Health Initiative, WHI) у женщин с тяжелыми проявлениями приливов и ночной потливости риск развития сахарного диабета при последующем наблюдении был на 48% выше [15]. Кроме того, у них имеются признаки нарушения функции эндотелия и усиления субклинического атеросклероза по сравнению с женщинами без вазомоторных симптомов. Вазомоторные симптомы средней и тяжелой степени ассоциированы с высоким риском развития метаболических нарушений и артериальной гипертонии – такой вывод был получен исследователями при 15-летнем наблюдении женщин с менопаузальными симптомами [17, 18].
Дефицит эстрадиола как потенциальный фактор риска развития сердечно-сосудистых и метаболических нарушений
У женщин со своевременной менопаузой повышенный риск ССЗ обусловлен последствиями самой менопаузы, а точнее, дефицита эстрогенов, ассоциированного с изменением композиционного состава тела и развитием висцерального ожирения, дислипидемией, эндотелиальной дисфункцией, нарушением толерантности к глюкозе, а также проявлениями климактерического синдрома. Эстрогены в течение первой половины жизни женщины оказывают плейотропный кардиопротективный эффект, но после наступления менопаузы, вследствие развившегося дефицита эстрогенов, их защитный эффект прекращается и риски ССЗ заметно возрастают [7].
Многие из последствий гормональной перестройки в постменопаузе ассоциированы с повышенным риском ССЗ. Распространенность ишемической болезни сердца увеличивается с возрастом. Основной причиной органического поражения миокарда является атеросклероз коронарных артерий (КА) [7]. Повышение уровня липопротеинов низкой плотности (ЛПНП), триглицеридов и холестерина (ХС) способствует развитию атеросклероза [18, 19]. У женщин уровень ЛПНП возрастает после 35 лет и дополнительно повышается на 10–15% в условиях дефицита эстрогенов [7, 20]. Повышенные уровни триглицеридов и ЛПНП также характерны для женщин с избыточной массой тела [21]. Изменения липидного профиля способствуют тромбообразованию и снижают фибринолитическую активность крови. Антиатерогенный эффект эстрогенов состоит в ускорении распада ЛПНП, повышении уровня липопротеинов высокой плотности (ЛПВП), снижении уровня ХС и антиоксидантном действии. Эстрогены улучшают сосудистый кровоток, увеличивают секрецию простациклинов. Действуя подобно антагонистам кальция, они снижают резистентность сосудов [18].
У женщин с нарушениями сна (уменьшение продолжительности сна, снижение качества сна, бессонница) в постменопаузе повышен риск развития метаболического синдрома (МС) [22, 23], наблюдается увеличение толщины комплекса интима-медиа сонной артерии и формирования бляшек в сонной артерии, кальцификации КА, повышается жесткость артериальной стенки [22].
Депрессия в постменопаузе ассоциирована с повышением кальцификации КА, увеличенной смертностью от ССЗ и общей смертностью [24].
По данным Российского наблюдательного исследования «Эпидемиология сердечно-сосудистых заболеваний (ЭССЕ-РФ)», частота артериальной гипертензии (АГ) у женщин в возрасте 35–44 лет составляет 28,5%, однако уже к 45–54 годам этот показатель увеличивается вдвое – 51,7%, а к 55–64 годам достигает 75,4% [25]. С началом менопаузального перехода продукция эндогенного эстрадиола снижается. Так как он обладает определенными вазодилатирующими свойствами, с возрастом уровень артериального давления (АД) увеличивается. Учитывая внешние факторы, это способно привести к риску развития АГ. Дебют АГ у женщин нередко сопровождается манифестацией метаболических нарушений, возникающих в период менопаузального перехода [26].
Влияние дефицита эстрадиола на пищевое поведение женщины
Эстрадиол, как один из важнейших половых стероидов, регулирует гомеостатическое питание у женщин путем уменьшения потребления пищи и увеличения затрат энергии. К примеру, снижение потребления пищи у женщин во время фолликулярной фазы является следствием анорексигенного действия эстрадиола. Эстрадиол действует на уровне коры, гипоталамуса и ствола головного мозга [27]. Анорексигенное и термогенное действие эстрадиола можно объяснить геномными и негеномными механизмами. Эту ситуацию можно также экстраполировать на период менопаузы – снижение уровня эстрадиола, которое наблюдается в этот период, влечет за собой увеличение потребления пищи и снижение энергетических затрат [28].
Показано, что более низкие уровни эстрадиола влияют на повышение аппетита и изменение в большую сторону порций еды.
Снижение выработки эстрадиола ведет к повышенной активации сигналов в желудочно-кишечном тракте (ЖК-сигналы). Эти сигналы активируют афферентные нейроны блуждающего нерва и передают сигнал о «недостатке пищи» в ствол головного мозга. Те, в свою очередь, передают сигнал в гипоталамус. Так формируется цепочка, которая контролирует пищевое поведение (рис. 1).
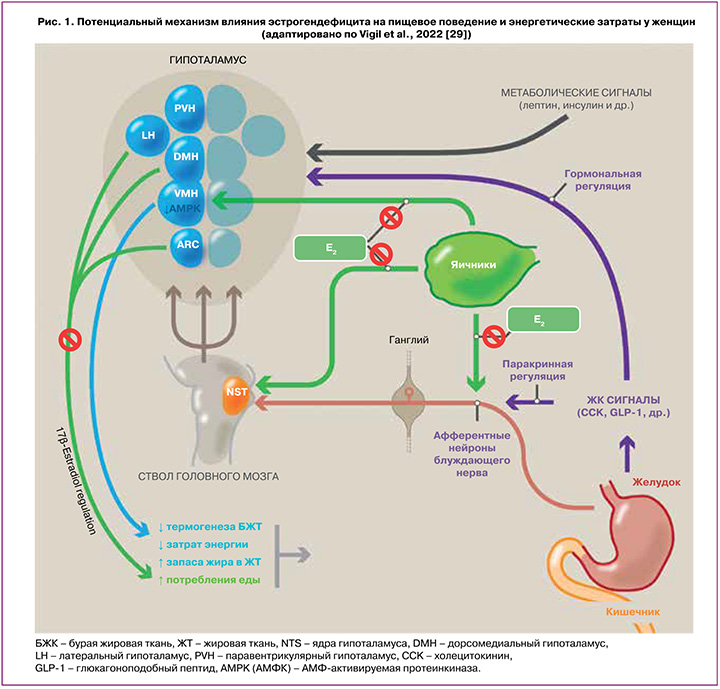
Снижение уровня эстрадиола уменьшает и его анорексигенное действие на уровне ядер гипоталамуса, тем самым увеличивается желание в потреблении пищи. Вдобавок к этим эффектам желание «переедания» повышают и метаболические сигналы. Уменьшение термогенных эффектов эстрадиола сопровождается изменением и жировой ткани. Происходит ее перераспределение – бурая жировая ткань регрессирует, снижается ее термогенная активность, а белая жировая ткань начинает ускоренно запасать липиды [30–37].
Снижение возможности потратить увеличенное число калорий от переедания приводит к развитию ожирения, а также системной и церебральной инсулинорезистентности [38].
За 4 года до наступления менопаузы у женщин наблюдается перераспределение жировой и мышечной тканей (рис. 2). На фоне снижения уровня эстрадиола идет параллельное увеличение абдоминального жира.
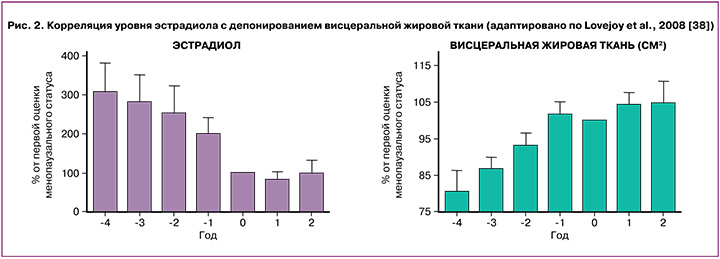
У женщин в пери- и ранней постменопаузе наблюдается увеличение массы тела в среднем на 20–25% [28, 38]. Висцеральная жировая ткань продуцирует воспалительные цитокины, такие как фактор некроза опухоли-α, интерлейкин-6 и ретинолсвязывающий белок-4. Отток свободных жирных кислот в печень увеличивает выработку активных форм кислорода [39].
Ожирение тесно связано с увеличением риска развития депрессии, которая, в свою очередь, усиливает потребление пищи, лишает сна и снижает физическую активность [40, 41]. Ожирение по висцеральному типу способствует увеличению деменции, однако этот риск может быть ослаблен на фоне приема эстрадиола [42, 43]. Лечение вазомоторных и иных симптомов эстрогенодефицита эффективно с помощью менопаузальной гормональной терапии (МГТ) [43–47]. Предпочтительно использовать эстрадиол в качестве эстрогенного компонента, а также метаболически нейтральные гестагены в составе комбинированной МГТ с минимальным риском развития венозных тромбоэмболических осложнений (ВТЭО), например дидрогестерон или препараты прогестерона. Именно раннее начало МГТ может способствовать снижению риска развития болезни Альцгеймера, в то время как поздняя инициация лечения (60 лет и более), наоборот, этот риск повышает [48].
Дополнительные регулярные физические упражнения (до 150 минут умеренных нагрузок) также оказывают позитивный эффект на вазомоторные симптомы и качество жизни [49–51]. Важно не упускать из внимания пациенток с ПНЯ и вовремя консультировать их по вопросам выбора гормональной терапии для поддержания физического и ментального здоровья. В повседневной клинической практике комбинированные оральные контрацептивы (КОК) и МГТ назначают данной категории женщин. Однако следует подчеркнуть, что доказаны позитивные эффекты МГТ в отношении метаболического статуса и повышения костной массы. Это предопределяет данный вид терапии как предпочтительный [2, 51].
Гормональный дисбаланс в период менопаузального перехода: почему важно обращать внимание на андрогены?
Только очень небольшая доля общего количества тестостерона (0,7–1,0%) циркулирует в плазме крови в свободном (биологически активном) виде. Основное количество тестостерона связано с белками крови: до 25% находится в соединении с альбумином и до 70–75% – с глобулином, связывающим половые гормоны (ГСПГ). Под воздействием ферментов из тестостерона образуются и другие гормоны – эстрадиол, дигидротестостерон. Еще одним важным гормоном является дегидроэпиандростерона сульфат (ДГЭА-С). В физиологических условиях концентрация ДГЭА-С в организме превышает содержание других стероидных гормонов. Помимо тестостерона и ДГЭА-С слабой андрогенной активностью обладают гормоны-предшественники – андростендион, дегидроэпиандростерон [52–54].
Скорость выработки андрогенов постепенно снижается у женщины начиная с 20–30 лет и не зависит от факта наступления менопаузы. По сравнению с резким падением уровня эстрогенов, свойственного периодам пери- и постменопаузы, снижение уровня андрогенов идет более плавно. Таким образом можно отметить, что скорость выработки андрогенов в пери- и постменопаузе снижается в меньшей степени, учитывая постоянный вклад надпочечников в пул циркулирующих половых гормонов [55].
На фоне преобладающих инволютивных процессов в яичниках снижается выработка эстрадиола. Вместе с этим одновременно снижаются и уровни ГСПГ, из-за последующего снижения взаимодействия эстрогена с печенью. Такое изменение приводит к увеличению циркулирующих в плазме крови уровней свободных андрогенов [55]. Соотношение андрогенов и эстрогенов увеличивается, что приводит к созданию среды относительной гиперандрогении.
Именно роль андрогенов является одним из наиболее рассматриваемых вопросов менопаузы в настоящее время. Важно не просто снизить уровень относительной гиперандрогении, а найти баланс между всеми гормонами. Рассмотрим подробнее роль андрогенов в этот период жизни женщины.
У женщин до и после наступления менопаузы, особенно при наличии ожирения, секреция андрогенов повышает резистентность к инсулину. Избыточное производство инсулина при этом стимулирует яичники вырабатывать андрогены [55]. Можно отметить, что именно снижение уровня ГСПГ связано с аномальной резистентностью к инсулину, так как снижается уровень основного проводника, который связывает андрогены, поэтому их свободное количество в крови возрастает. В клинической практике это может быть отмечено легким ростом волос на лице (гирсутизм), проявлением алопеции (выпадение волос на голове) [56]. Здесь очень важно найти баланс – усилия должны быть направлены не столько на снижение уровня андрогенов за счет антиандрогенных гестагенов, сколько на увеличение уровня эстрогенов и закономерное увеличение ГСПГ.
Важно учитывать свойства ряда гестагенов, которые обладают выраженным антиандрогенным действием, что может привести к гипоандрогении. Если относительная гиперандрогения возникла в перименопаузе, то целесообразно восстановить баланс эстрогенов, не затрагивая андрогенный профиль за счет селективности гестагена, – например, рассмотреть вопрос назначения фиксированной комбинации перорального эстрадиола и дидрогестерона с целью повышения уровня эстрогенов и снижения андрогенного влияния. Но если проявления гиперандрогении выражены и возникли впервые после наступления менопаузы, нельзя исключить наличие андрогенной продуцирующей опухоли яичников или надпочечников (встречаемость не более 8%), что требует дополнительного обследования и при подтверждении опухоли – хирургического вмешательства [57].
Влияние андрогенов на симптомы генитоуринарного менопаузального синдрома и сексуальную функцию
Снижение выработки андрогенов негативно влияет на прогрессирование структурных и функциональных изменений мочеполового тракта. Потеря кислотности во влагалище повышает риск развития восходящей инфекции мочевого пузыря, гиперактивности мочевого пузыря или рецидивирующих инфекций мочевыводящих путей [58]. Имеются данные, что у женщин в постменопаузе с более высокими уровнями андростендиона и тестостерона атрофия влагалища была снижена [59].
Сексуальное поведение, настроение и эмоциональное состояние модулируются половыми гормонами на протяжении всей жизни женщины. В период пери- и постменопаузы спад концентрации андрогенов негативно влияет на самочувствие женщины, особенно на снижение сексуального возбуждения [60]. Независимо от возраста, после наступления менопаузы сексуальное желание не снижается. Но распространенные симптомы дефицита эстрогенов и андрогенов, такие как низкое либидо (40–50%), сухость влагалища (25–30%) и диспареуния (12–45%), симптомы генитоуринарного менопаузального синдрома значительно снижают женскую сексуальную функцию [61].
Влияние андрогенов на костную и мышечную ткани
Рецепторы андрогенов экспрессируются в остеобластах и остеоцитах. Это свидетельствует о прямом влиянии андрогенов на мышечную и скелетную активность. В позднем репродуктивном периоде уменьшение концентрации свободного тестостерона сказывается на снижении минеральной плотности костной ткани (МПКТ) (снижение на 1% и более в год). В ходе анализа женщин в возрасте от 67–94 лет эндогенный общий тестостерон позитивно влиял на МПКТ шейки бедра и поясницы [62]. Данные обсервационного исследования «Инициатива во имя здоровья женщин» (Women’s Health Initiative, WHI) показали, что более высокие концентрации свободного тестостерона были ассоциированы с более низким числом переломов независимо от концентрации эстрадиола или ГСПГ [63].
Влияние андрогенов на сердечно-сосудистую систему
Ключевые механизмы, которые влияют на связь снижения андрогенов со снижением сосудистого здоровья, – окислительный стресс и воспаление. Пока андрогены циркулируют в крови и не снижают своих референсных порогов у женщин в репродуктивном возрасте, они опосредованно влияют на уменьшение активности перекисных радикалов и воспалительных процессов [64].
На фоне снижения уровня андрогенов повышается содержание активных форм кислорода, которые негативно влияют на клеточные структуры (нарушается работа цитоплазмы, митохондрий и пероксисом (окисление липидов)), кроме того, окислительные формы провоцируют повышенную продукцию медиаторов воспалительных процессов (TNF-α, NF-κβ, IL-10), дополнительно снижается выработка оксида азота (NO). Медиаторы воспалительных процессов нарушают эндотелиальную функцию, повышается жесткость сосудов (разрушение эластина, увеличение в составе коллагена, последующая кальцификация). Это ведет к функциональным изменениям в гладкомышечной ткани, тонус гладкомышечных миоцитов повышается. Образовавшаяся жесткость крупных артерий повышает АД, что способно привести к формированию АГ, усиливает риск повреждения стенки сосудов (эндотелия), а также атерогенные и тромбогенные риски. Помимо того, что тестостерон оказывает положительное влияние на функцию сосудистого эндотелия, он также обладает вазодилататорным действием [65]. Исследование показало, что среди женщин старше 70 лет без сердечно-сосудистых ишемий в анамнезе у участниц с низким уровнем тестостерона вероятность возникновения ишемического сердечно-сосудистого события была примерно в два раза выше в течение среднего наблюдения 4,4 года [66].
Сбор симптомов дефицита андрогенов у женщин
Андрогенное действие определяется количественным уровнем андрогенов, присутствующих в кровообращении, степенью их связывания с белками, степенью взаимного превращения в другие андрогены и эстрогены, а также биологической активностью и сродством связывания андрогенов с андрогенными рецепторами. Симптоматика дефицита андрогенов у женщин может быть схожей с проявлениями различных соматических и психологических состояний, которые могут сосуществовать во время менопаузы, но, несмотря на эти трудности, несколько симптомов были приписаны именно дефициту андрогенов у женщин. Наиболее распространенными клиническими признаками дефицита андрогенов являются снижение сексуальной мотивации, сексуальных фантазий, сексуального удовольствия, сексуального возбуждения. Малые критерии дефицита андрогенов определяются как ухудшение качества жизни (подавленное настроение, раздражительность, утомляемость), бессонница, депрессивные симптомы, головная боль. Все эти признаки и симптомы могут быть многофакторными [67, 68]. Наиболее частыми состояниями, связанными с гипоандрогенией у женщин, являются гипоталамо-гипофизарные нарушения, отсутствие или недостаточность яичников, надпочечниковая недостаточность, терапия глюкокортикоидами, введение экзогенных эстрогенов в комбинации с антиандрогенными гестагенами. Поскольку большинство признаков дефицита андрогенов могут быть приписаны другим соматическим или психологическим состояниям, связанным со старением, данное состояние зачастую не диагностируется или неправильно истолковывается. Помимо клинической картины, для диагностики важно измерение уровня свободного тестостерона. Методом оценки этого показателя является равновесный диализный анализ [67]. Несмотря на клиническую значимость андрогенной недостаточности у женщин, на сегодняшний день все еще отсутствует достаточное количество данных, а также одобренных клинических протоколов по ведению женщин в данном состоянии.
Роль менопаузальной гормональной терапии в лечении климактерического состояния у женщины
Во всем мире общепризнанной терапией первой линии для терапии климактерических состояний является МГТ [2, 69–79]. Данный вид терапии доказал свою эффективность в снижении вазомоторных и иных климактерических проявлений в широком числе рандомизированных плацебо-контролируемых исследований. При наличии одного и более климактерических симптомов у женщин старше 45 лет целесообразно рассмотреть назначение МГТ.
История данной терапии берет свое начало из 1940-х гг. в США, когда из мочи беременных кобыл был впервые синтезирован конъюгированный эквин эстроген (КЭЭ), который активно назначали женщинам с вазомоторными симптомами в постменопаузе. КЭЭ показал свою эффективность, однако данный вид эстрадиола является наименее безопасным с точки зрения онкологических и сердечно-сосудистых рисков [78].
В настоящий момент назначение МГТ четко регламентировано [2]. В руках практикующих акушеров-гинекологов есть ряд инструментов, которые позволяют избегать потенциально опасных ситуаций при назначении МГТ – клинические рекомендации «Менопауза и климактерическое состояние у женщины», Российские критерии приемлемости МГТ, а также алгоритмы применения МГТ [2, 9, 78].
МГТ противопоказана женщинам с высоким риском развития ИБС с сопутствующими заболеваниями, которые остаются неконтролируемыми, включая АД ≥180/110 мм рт.ст., общий холестерин >310 мг/дл и триглицериды >400 мг/дл. Однако при контролируемых показателях АД и липидного спектра в пределах нормы можно рассмотреть назначение МГТ [7, 78]. МГТ также противопоказана пациентам с ишемическим инсультом в анамнезе. Кроме того, противопоказания к назначению МГТ включают необъяснимое вагинальное кровотечение, рак молочной железы в анамнезе, эстроген-чувствительный рак эндометрия, позднюю кожную порфирию, деменцию и активное заболевание печени или желчного пузыря [2, 9, 78].
При абсолютных противопоказаниях к назначению МГТ целесообразно рассмотреть альтернативные методы терапии, например, фитоэстрогены. Хотя данный вид терапии по эффективности и уступает МГТ, имеются данные о благоприятном эффекте на снижение вазомоторных проявлений [2, 79].
Различные гормонозаместительные препараты одобрены для лечения эстрогендефицитных состояний. Считается, что добавление прогестагена повышает некоторую эффективность МГТ, однако драйвером этой эффективности все же первостепенно является эстроген. При выборе МГТ необходимо учитывать профиль безопасности эстрогенов и гестагенов, входящих в состав, так как данная терапия должна назначаться на протяжении длительного времени. Показано, что несвоевременная отмена МГТ снижает потенциальные благоприятные эффекты МГТ на сердечно-сосудистую и костную системы [7, 9, 72, 76, 77, 80–85].
МГТ назначается в рамках «терапевтического окна – в возрасте до 60 лет и длительности постменопаузы не более 10 лет. Почему сформировалось данное ограничение? Согласно данным исследований Hodis et al., при наличии сформировавшихся коронарных атеросклеротических бляшек у пожилых женщин пероральный эстроген индуцирует MMP-9 и другие воспалительные факторы, что приводит к их нестабильности из-за расщепления участков бляшек, что в итоге ведет к их разрыву и тромбозу. Разрыв бляшки и тромбоз не наблюдаются у молодых женщин, поскольку не существует субстрата для действия MMP-9 с меньшим количеством атеросклеротических бляшек [18, 86] (рис. 3).
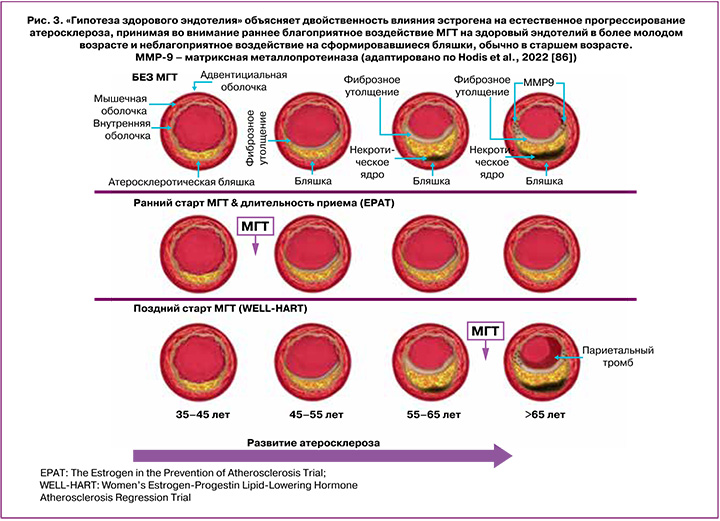
На сегодняшний день набирает популярность концепция «своевременного» старта. Раннее и своевременное назначение МГТ (комбинации эстрадиола и дидрогестерона) может быть рекомендовано женщинам при наличии 1 и более симптомов менопаузы при стойкой аменорее 6 месяцев и более. Важно учитывать свойства гестагена в составе МГТ. Необходимо, чтобы гестагенный компонент не уменьшал, а потенцировал благоприятные эффекты эстрогена [9, 76]. С этой целью рекомендуется остановить выбор на высокоселективных гестагенах с минимальным влиянием на метаболические процессы. Дидрогестерон – высокоселективный гестаген с повышенным сродством к прогестероновым рецепторам. Он не уменьшает благоприятное влияние эстрадиола, а также сохраняет баланс эндогенных андрогенов в женском организме [87]. Комбинация эстрадиол/дидрогестерон снижала частоту и выраженность приливов уже через 3 недели применения в сравнении с плацебо [88].
Кроме того, благоприятный профиль безопасности дидрогестерона показан в ведущих национальных и мировых клинических рекомендациях [2, 9, 68, 69, 70, 71, 78]. Согласно российским критериям по МГТ, комбинация эстрадиола и дидрогестерона – единственная пероральная МГТ с доказанным профилем безопасности в отношении рисков ВТЭО вне зависимости от дозирования, индекса массы тела и возраста пациенток [9].
Заключение
Абсолютное большинство женщин во всем мире сталкиваются с проблемами менопаузы. Поскольку общая продолжительность жизни женщины возросла и будет продолжать увеличиваться, врачу-клиницисту важно своевременно и грамотно оказать консультирование с целью потенциального снижения возраст-ассоциированных рисков. Необходимо формировать правильное понимание состояния «менопауза», предоставлять актуальную информацию об особенностях переходного периода с целью повышения качества и благополучия жизни каждой женщины, профилактики потенциальных рисков и целесообразности своевременного назначения МГТ. Среди всех видов МГТ наибольший интерес уделяется комбинации эстрадиола и дидрогестерона, так как данный тип МГТ позволяет достичь необходимого гормонального баланса и эффективно снижать менопаузальные проявления, не добавляя дополнительных рисков для здоровья, что особенно важно при длительном ведении пациенток.



