В настоящее время около 20% беременных женщин подвергаются операции кесарева сечения (КС) [1]. В большинстве регионов мира этот показатель выше и продолжает увеличиваться, достигая 40,5% в некоторых странах [2]. По данным Росстата, в Российской Федерации в 2005 г. частота КС составила 17,9%, в 2020 г. – 30,3% [3]. По данным В.И. Краснопольского и соавт. [4] частота КС в некоторых крупных перинатальных центрах России достигает 40% и более.
Дефект рубца на матке (РМ) может быть причиной нарушений менструальной функции, хронической тазовой боли, вторичного бесплодия. Во время беременности наиболее серьезными клиническими состояниями, связанными с РМ, являются эктопическая беременность в рубце, врастание и предлежание плаценты, разрыв матки. В связи с этим, особую актуальность приобретает оценка состояния РМ вне беременности и возможность на основании нее прогнозировать течение последующей беременности и родов.
Дефект (истончение) рубца следует определять, как истончение зоны рубца, по сравнению с прилежащим интактным миометрием. Дефекты рубца могут быть с образованием ниши или без таковой [5].
Под нишей понимают выявляемое при ультразвуковом исследовании (УЗИ) анэхогенное углубление со стороны полости матки в области рубца после КС глубиной не менее 2 мм, по данным некоторых авторов – 3 мм и даже 5 мм [6]. Чаще всего термин «ниша» употребляется в случае отсутствия плавного изменения толщины миометрия в зоне дефекта, при этом имеются более отвесные, нередко «подрытые» края.
На сегодняшний день самыми распространенными и наиболее доступными являются ультразвуковые методы исследования: трансвагинальное УЗИ и эхогистеросальпингография (ЭхоГСГ) с использованием контрастных сред. В качестве контрастных сред применяются физиологический раствор, соноконтрастные растворы и гели. Предложены многочисленные варианты оценки состояния РМ, включающие помимо определения ширины, протяженности, глубины, локализации дефекта, толщины остаточного миометрия (ТОМ) в зоне рубца, также описание формы дефекта, наличия затеков, измерение объема ниши, степени (индекса) истончения и т.д., от которых зависит дальнейшая тактика ведения пациентки. Описаны возможности 2D и 3D УЗИ, компьютерного моделирования формы ниши при ЭхоГСГ. Преимуществами 2D УЗИ являются распространенность и доступность метода, возможность быстрой подготовки и обучения специалистов. 3D УЗИ позволяет получить трехмерное изображение, выполнить компьютерное моделирование и более точно оценить форму и объем ниши. ЭхоГСГ за счет наполнения полости матки и ниши контрастным раствором позволяет детально оценить ТОМ, форму и края ниши, наличие затеков и ответвлений, а также проводить автоматизированное определение объема ниши с помощью специальных компьютерных программ. Помимо определения состояния рубца, ЭхоГСГ позволяет оценить проходимость маточных труб, что особенно важно для пациенток, заинтересованных в планировании беременности [6–14]. Однако единой точки зрения относительно выбора метода диагностики, а также общепринятой методики измерения дефектов РМ после КС на сегодняшний день нет.
Важным в методическом аспекте стало исследование Delphi [6], в котором приняли участие 20 экспертов, наиболее опытных в области изучения дефектов РМ после КС и имеющих публикации по данной теме в рецензируемых журналах. В результате проведенного мета-анализа литературы, а также слепого перекрестного опроса, авторы пришли к консенсусу относительно методики выявления и описания дефектов РМ, а также особенностей их измерения при УЗИ. Экспертами группы Delphi была признана высокая информативность ЭхоГСГ, ее преимущества в определении формы дефекта, визуализации краев ниши, однако ЭхоГСГ не была рекомендована в качестве обязательного исследования при дефектах РМ после КС. В то же время, многочисленные публикации о диагностической ценности ЭхоГСГ свидетельствуют не только о хорошей информативности метода, но и о его высокой воспроизводимости, хотя и отмечается некоторое различие измерений параметров РМ между УЗИ и ЭхоГСГ.
Приняв за принципиальную основу методику из исследования Delphi [6], целью нашей работы стало повышение эффективности оценки состояния РМ после операции КС основании сравнения различных ультразвуковых методов исследования.
Материалы и методы
Данное сравнительное исследование проводилось на базе ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Министерства здравоохранения Российской Федерации (НМИЦ АГиП). В группу исследования были включены 65 пациенток с РМ после операции КС (после последнего КС прошло более 1 года), заинтересованных в повторной беременности. Критериями включения являлись: возраст пациенток – от 18 до 45 лет; планирование беременности; истончение РМ после операции КС по данным УЗИ (ТОМ менее 5 мм); подписанное информированное согласие на участие в исследовании. Критериями исключения явились: возраст до 18 лет и старше 45 лет; острые воспалительные заболевания органов малого таза; тяжелые сопутствующие соматические заболевания; злокачественные новообразования.
Всем пациенткам на 1-м этапе амбулаторно вне специализированного исследовательского центра было выполнено стандартное УЗИ (сУЗИ) органов малого таза различными специалистами на ультразвуковых аппаратах разного класса в пролиферативную фазу на 5–11-й день менструального цикла.
Для дальнейшего диагностического поиска на втором и третьем этапах в условиях НМИЦ АГиП выполнялись экспертное УЗИ (эУЗИ) органов малого таза и ЭхоГСГ.
эУЗИ выполнялось женщинам в пролиферативную фазу на 5–11-й день менструального цикла с помощью аппарата Samsung WS80А Elite (Samsung Medison, Ю. Корея) трансвагинальным датчиком с частотой 7,5 МГц. Исследования проводились специалистами отделения ультразвуковой и функциональной диагностики НМИЦ АГиП, имеющими стаж работы в области акушерства и гинекологии более 10 лет (более 10 000 исследований) и значительный опыт исследований РМ после КС. Проводилось стандартное описание топографии и анатомических особенностей внутренних половых органов. Отдельно проводилось измерение параметров РМ согласно методике, принятой в исследовании Delphi [6]. Измерялись: максимальные длина и глубина ниши (в сагиттальной плоскости); минимальная ТОМ в зоне рубца (в сагиттальной плоскости, перпендикулярно серозной оболочке от верхнего внутреннего контура дефекта до серозной оболочки, при этом эндометрий и серозная оболочка не включались в измерение); максимальная ширина ниши (в поперечной плоскости); толщина интактного миометрия (ТИМ) – толщина передней стенки матки рядом с верхним краем ниши (в сагиттальной плоскости). Расстояние между нишей и пузырно-маточной складкой, а также расстояние между нижним краем ниши и наружным зевом шейки матки нами не фиксировались (эти параметры не входят в обязательно рекомендуемые по данным исследования Delphi). В то же время мы сочли необходимым ввести дополнительно еще один параметр – расположение рубца относительно внутреннего зева (минимальное расстояние от внутреннего зева до ближайшего края ниши, в сагиттальной плоскости), поскольку он наиболее точно описывает «цервикализацию», т.е. низкое расположение рубца. Последние три параметра более важны для хирурга в качестве дополнительных «навигационных» данных во время операции.
Комплексное УЗИ, включающее 2 этапа (трансвагинальное эУЗИ, аналогично описанному выше, и непосредственно за ним – ЭхоГСГ) проводилось на 7–11-й день менструального цикла на ультразвуковом сканере WS80A (Samsung Medison, Ю. Корея) трансвагинальным датчиком с частотой 7,5 МГц. С целью сравнительной оценки двух методов исследования, измерение параметров РМ производилось двумя независимыми исследователями последовательно в режиме реального времени в каждом случае. Первый исследователь – специалист с опытом работы 15 лет, специализирующийся на проведении ЭхоГСГ (более 300 исследований ЭхоГСГ). Второй исследователь – специалист с опытом работы 25 лет, но имеющий незначительный опыт выполнения ЭхоГСГ. Полученные первым и вторым исследователями результаты были неизвестны друг другу до окончания измерений.
Методика проведения ЭхоГСГ заключалась в следующем. Пациентки проходили предварительное лабораторное обследование: мазок на флору и анализ крови на гепатит В и С, сифилис, ВИЧ. В качестве контрастной среды использовали анэхогенный контраст (0,9% раствор хлорида натрия). После проведения первого этапа исследования (трансвагинального УЗИ) производилась установка зеркала Куско, обнажение шейки матки, обработка влагалища и шейки матки раствором антисептика (октенисепт), установка в цервикальном канале мягкого баллонного катетера 6600 Angiotech (5 Fr) и его фиксация за счет раздувания баллона, введение теплого 36,6°С стерильного 0,9% раствора хлорида натрия в полость матки в объеме 10–20 мл, позволяющем достигнуть достоверного ее контрастирования под контролем трансвагинальной эхографии в режиме реального времени; оценка прохождения контраста по маточным трубам; описание топографии и анатомических особенностей внутренних половых органов, измерение параметров РМ по алгоритму Delphi. В конце процедуры катетер из полости матки удалялся.
Статистический анализ
Статистическая обработка и анализ данных были выполнены с помощью программного обеспечения Microsoft Excel 2010 и STATISTICA Application v.10.0. Для оценки нормальности распределения данных использовался критерий Колмогорова–Смирнова и Шапиро–Уилка. Данные с нормальным распределением представлены как среднее (стандартное отклонение). Для сравнения полученных данных использовался критерий Стьюдента. Согласованность различных измерений, полученных двумя методами, а также двумя независимыми исследователями, анализировалась с помощью построения графиков Блэнда–Альтмана. При проверке статистических гипотез значимым считался уровень значимости р<0,05.
Результаты
Средний возраст пациенток составил 34,0 (3,9) года и колебался от 29 до 43 лет. 51 пациентке в анамнезе было выполнено 1 КС, 11 пациенткам – 2 КС, 3 пациенткам – 3 КС. На момент исследования у всех женщин после последнего КС прошло более одного года. У 67,7% пациенток (44 человека) предыдущее КС было выполнено в экстренном порядке, у 32,3 % (21 человек) – в плановом порядке.
Наиболее частыми клиническими проявлениями дефекта РМ являлись скудные кровянистые выделения из половых путей: у 51 пациентки после менструации (от 2 до 20 дней, в среднем по 7 дней); у 5 пациенток до менструации (в среднем по 2 дня); у 3 пациенток в середине менструального цикла (в среднем по 3,5 дня). Также наряду с вышеуказанными жалобами 7 пациенток отмечали отсутствие наступления беременности при регулярной половой жизни без контрацепции более 1 года, а 4 пациентки – альгоменорею, возникшую после КС. Бессимптомное течение отмечалось у 6 пациенток.
При сравнительном анализе данных сУЗИ и эУЗИ были выявлены статистически значимые различия при измерении ТОМ, ширины и глубины ниши, и не были выявлены статистически значимые различия при измерении длины ниши, ТИМ и расположения рубца относительного внутреннего зева. (табл. 1).
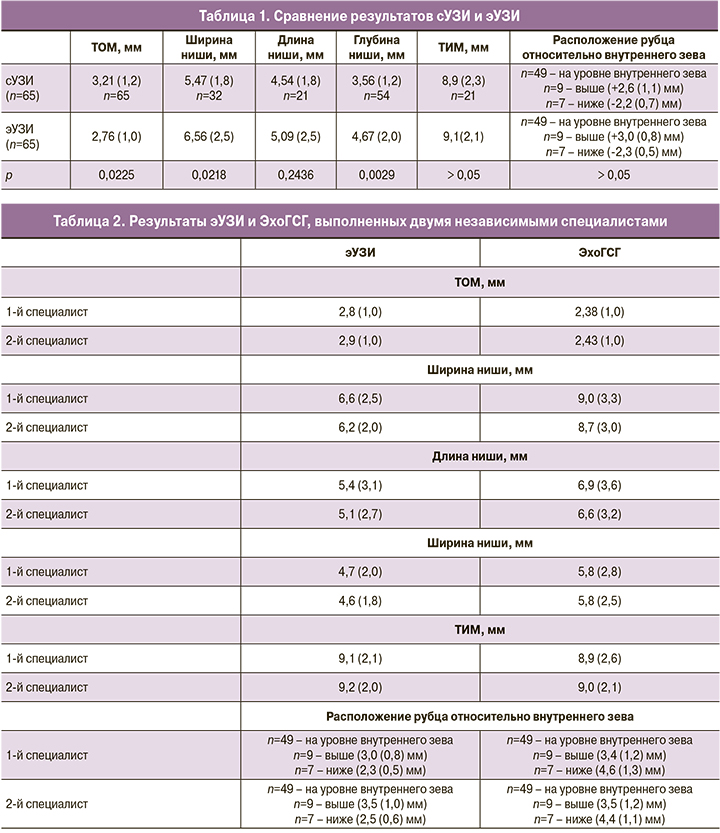
Следует отметить, что при анализе заключений сУЗИ, выполненных на амбулаторном этапе, в абсолютном большинстве случаев измерение параметров РМ не носило полный характер. Чаще всего измерялись ТОМ и глубина ниши, тогда как ширина и длина ниши были измерены менее, чем у половины пациенток. Остальные показатели не фигурировали ни в одном из заключений (табл. 1).
По данным эУЗИ в 7 случаях рубец располагался в области верхней трети шейки матки, в 9 случаях – в области нижней трети стенки матки, в остальных случаях – в проекции внутреннего зева. У 4 пациенток были выявлены 2 рубца после 2 КС, у 1 пациентки были выявлены 2 рубца после 3 КС, у остальных пациенток определялся только 1 рубец, вне зависимости от количества выполненных КС в анамнезе.
Результаты измерений параметров РМ, полученные двумя независимыми специалистами при эУЗИ и ЭхоГСГ, представлены в таблице 2.
Для сравнения результатов двух методов исследования (эУЗИ и ЭхоГСГ) был проведен анализ средних значений определяемых параметров РМ по результатам измерений обоих специалистов (рис. 1–4.)
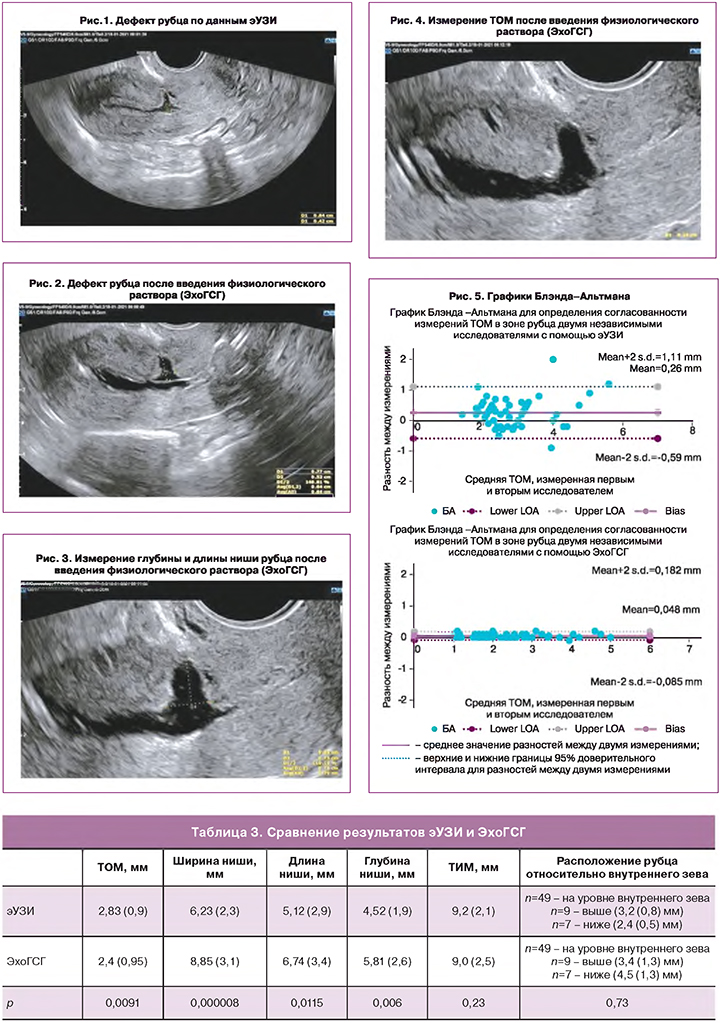
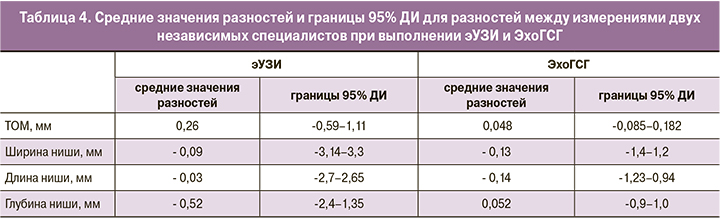
При сравнительном анализе данных эУЗИ и ЭхоГСГ были выявлены статистически значимые различия в измерении ТОМ, ширины, длины и глубины ниши; не выявлены статистически значимые различия, как при измерении ТИМ, так и в расположении рубца относительно внутреннего зева (табл. 3).
С целью оценки согласованности измерений одних и тех же параметров специалистами с разным уровнем подготовки в рамках каждого метода исследования (эУЗИ и ЭхоГСГ) был проведен t-тест Стьюдента для независимых переменных, который не выявил статистически значимых различий. В связи с этим был использован анализ Блэнда–Альтмана. Были вычислены средние значения разностей между измерениями двух независимых специалистов, а также верхние и нижние границы 95% доверительного интервала (ДИ) для разностей между измерениями двух исследователей (табл. 4). Чем ближе к «0» были расположены средние значения разностей, и чем меньше была ширина 95% ДИ, тем более однородными являлись измерения.
Поскольку основополагающее значение для принятия решения о необходимости хирургической коррекции РМ имеет величина ТОМ, на основании полученных данных были построены графики Блэнда–Альтмана для определения согласованности измерений именно этого показателя (рис. 5).
При анализе графиков Блэнда–Альтмана было выявлено, что средняя разность между значениями, полученными первым и вторым исследователем как при эУЗИ, так и при ЭхоГСГ, была приближена к 0, что свидетельствовало о хорошей согласованности измерений. Однако, в большей степени обращал на себя внимание тот факт, что разности между результатами, полученными при эУЗИ, имели более широкий 95% ДИ, по сравнению с данными, полученными при ЭхоГСГ, что свидетельствовало о бóльшем разбросе результатов при выполнении эУЗИ и, соответственно, более выраженной согласованности и однородности результатов при использовании ЭхоГСГ.
Полученные данные в дальнейшем были подтверждены во время выполнения гистероскопии и/или лапароскопии.
Обсуждение
В современном мире отмечается тенденция к повышению частоты КС, что связано, как с расширением показаний к оперативному родоразрешению, так и с повышением числа первородящих женщин позднего репродуктивного возраста. Широкая распространенность и не имеющая тенденции к снижению частота КС обусловливают возросший в последнее время интерес к проблеме РМ после КС. При этом достаточно много исследований посвящены не только оценке состояния РМ во время беременности и в родах, но и выявлению дефектов рубца после КС вне беременности, а также различным методам их коррекции. Заключения специалистов ультразвуковой диагностики зачастую являются основанием для проведения хирургического вмешательства; при этом основным параметром, влияющим на принятие решения о выполнении метропластики, является ТОМ и, чуть реже, длина, ширина и глубина ниши или индекс истончения ТОМ/ТИМ. Также проведение метропластики зависит от расположения РМ относительно внутреннего зева. Поскольку от точности и согласованности измерения данных параметров напрямую зависит принятие решения о необходимости хирургического вмешательства, целью нашей работы явилось повышение эффективности оценки состояния РМ после операции КС с помощью ультразвуковых методов исследования.
Полученные нами результаты выявили несоответствие оценки состояния рубца по данным сУЗИ и эУЗИ, что особенно важно для определения дальнейшей тактики ведения пациенток, а также определения показаний и выбора метода оперативного лечения. Более подробный анализ выявил ряд серьезных системных нарушений.
Во-первых, следует отметить, что в абсолютном большинстве заключений сУЗИ, выполненных на амбулаторном этапе различными специалистами, измерения параметров РМ не носили полный характер. Чаще всего измерялись ТОМ и глубина ниши, тогда как ширина и длина ниши были измерены менее, чем у половины пациенток, а остальные показатели не фигурировали ни в одном из заключений. Данный факт свидетельствует об отсутствии общепринятой методики исследования РМ после КС
Во-вторых, нами была обнаружена статистически значимая разница в измерении ТОМ, ширины и глубины ниши, заключавшаяся в «завышении» толщины рубца и «занижении» параметров ниши на амбулаторном этапе диагностики. Обнаруженные нами различия могут быть обусловлены отсутствием единой методики измерения параметров РМ. Вероятнее всего, «завышение» величины ТОМ обусловлено включением в измерение серозного слоя и участков фиброза, а возможно и эндометрия, тогда как эти слои не рекомендованы для регистрации. Также, возможно, имело место измерение ТОМ не перпендикулярно серозной оболочке. К тому же на качество измерений могло повлиять проведение исследований на аппаратах разного класса, различный уровень подготовки специалистов, а также отсутствие у них опыта исследования РМ после КС. Baranov А. et al. [7] в своем исследовании отмечают высокую важность формирования такого навыка даже у опытных специалистов ультразвуковой диагностики, что отражается на точности диагностики. Кроме того, в заключениях сУЗИ нередко фигурировал термин «несостоятельный рубец на матке», о неприемлемости которого мы упоминали ранее [5].
В то же время, следует отметить высокую согласованность во времени проведения исследования – всеми специалистами определение состояния РМ проводилось в 1 фазу с 5-го по 11-й дни менструального цикла.
Таким образом, первая часть нашего исследования показала значимые различия в оценке состояния РМ после КС по данным сУЗИ и эУЗИ.
Следующей задачей исследования явилось сравнение точности диагностики дефектов РМ специалистами с разным стажем работы и опытом при применении единой методики исследования посредством трансвагинального эУЗИ и ЭхоГСГ, а также сравнение этих двух методов между собой на основании сопоставления характеристик РМ.
Полученные нами результаты свидетельствуют о высокой согласованности измерений между независимыми специалистами, как при трансвагинальной эхографии, так и при ЭхоГСГ. Статистически значимых различий не было получено ни в одном параметре, хотя при ЭхоГСГ разброс полученных значений был меньше, чем при УЗИ. Один из исследователей не имел большого опыта проведения ЭхоГСГ, при этом им отмечалась высокая четкость изображения, что облегчало выполнение измерений всех параметров РМ и влияло на их точность. Это подтверждают данные Monteagudo А., Regnard С., Osser О., Baranov А. [7–10], свидетельствующие о более четкой визуализации краев ниши при ЭхоГСГ. Так, по данным Baranov A. et al. [7] была выявлена высокая корреляция между измерениями ТОМ и ТИМ независимыми экспертами, как при УЗИ (коэффициент корреляции составил 0,87 и 0,82 соответственно), так и при ЭхоГСГ (коэффициент корреляции составил 0,96 и 0,85 соответственно). При этом авторы отмечали, что наибольшей согласованностью отличалось определение ТОМ с помощью ЭхоГСГ.
Полученные нами результаты свидетельствуют о высокой воспроизводимости методов (и эУЗИ, и ЭхоГСГ) и уменьшении частоты расхождений в измерении параметров РМ при проведении исследований в специализированном лечебном учреждении. На это, безусловно, влияют более современное оснащение, бóльший опыт специалистов, а также знание и использование ими методики измерения дефектов РМ после КС.
Наибольшая согласованность измерений была получена при ЭхоГСГ, при этом на точность измерения параметров РМ не влияла разница в опыте исследователя. Это свидетельствует о бóльшей воспроизводимости ЭхоГСГ и возможности рассмотрения ее в качестве «золотого стандарта» в диагностике дефектов РМ после КС среди ультразвуковых методов исследования.
Сравнение двух методов диагностики (эУЗИ и ЭхоГСГ) в оценке состояния РМ после КС выявило значимые различия в измерениях ТОМ, ширины, длины, глубины ниши, и не выявило различий в измерениях ТИМ и расположении рубца относительно внутреннего зева. При этом при ЭхоГСГ отмечались меньшие значения ТОМ и бóльшие значения параметров ниши, по всей видимости, связанные с некоторым растяжением ниши контрастным раствором и изменением угла измерения ТОМ.
Menada Valenzano М. et al. [11] также отмечали более значительные размеры ниши по данным ЭхоГСГ в сравнении с УЗИ.
Rasheedy R. et al. [12] отметили, что ТОМ в зоне рубца по данным ЭхоГСГ была меньше, чем по данным УЗИ – 10,09 (2,74) мм и 11,18 (2,50) мм соответственно (r=0,914). Также отмечались бóльшая ширина и глубина ниши по данным ЭхоГСГ и отсутствие различий между методами в измерении ТИМ.
В проспективном когортном исследовании Antila-Langsjö R. et al. [13] провели сравнительную оценку двух методов (УЗИ и ЭхоГСГ с использованием физиологического раствора в качестве контрастной среды) в диагностике дефектов рубца после КС. В результате глубина и ширина ниши при ЭхоГСГ были больше, чем при УЗИ, как и средние значения ТОМ – 3,7 мм и 3,3 мм, соответственно.
Сходная тенденция была отмечена и в исследовании Baranov А. et al. [7] – ТОМ так же, как и ТИМ при ЭхоГСГ была больше, чем при УЗИ – 5,6 мм и 4,8 мм соответственно; и 8,9 мм и 8,5 мм соответственно.
В то же время, Osser O.V. et al. [10] выявили бóльшую длину и ширину ниши по данным ЭхоГСГ и отсутствие различий между методами в измерении ТОМ.
Столь разные результаты исследований, полученные при сравнении двух методов диагностики в определении одних и тех же параметров, могут свидетельствовать лишь об одном – отсутствии единой методики измерений, особенно на начальных этапах изучения данного состояния. По мере накопления опыта все больше исследователей отмечают меньшие значения ТОМ при ЭхоГСГ, по сравнению с УЗИ, что может быть обусловлено лучшей визуализацией наиболее тонких участков рубца при заполнении ниши контрастом. Данный факт следует учитывать при интерпретации данных различных методов исследования с целью определения показаний для хирургической коррекции дефектов РМ.
Заключение
Таким образом, проведенное нами исследование показало широкие диагностические возможности ультразвуковых методов исследования в определении состояния РМ после КС. Большинство разногласий в заключениях специалистов ультразвуковой диагностики обусловлено отсутствием единой методики измерений. В связи с этим, приобретает огромное значение стандартизация исследований РМ после КС.
Исследование Delphi, обобщившее опыт двадцати признанных экспертов в ультразвуковой диагностике, на наш взгляд предлагает самый четкий алгоритм и методику измерений РМ после КС. Следование принципам, изложенным в данных рекомендациях, позволит стандартизировать все УЗИ (и эхографию, и ЭхоГСГ) и снизить частоту расхождений в измерениях одних и тех же параметров разными специалистами.
При выявлении подозрения на дефект РМ после КС на амбулаторном этапе целесообразно направить пациентку на обследование в специализированное медицинское учреждение. эУЗИ (выполненное специалистом, имеющим опыт измерений дефектов РМ, на аппарате экспертного класса с использованием критериев Delphi) позволяет с высокой точностью определить степень дефекта РМ после КС.
Важно отметить, что в сомнительных случаях, а также для решения вопроса о необходимости хирургического лечения и его объеме предпочтительно выполнять ЭхоГСГ, обладающую высокой воспроизводимостью и предоставляющую хирургу дополнительную «навигационную» информацию о состоянии зоны дефекта.
Дальнейшие исследования в этом направлении, а также проспективные исследования состояния РМ во время беременности и в родах необходимы для разработки современной классификации дефектов РМ после КС.



