За последнее время отмечена стойкая тенденция к более позднему или осознанно отложенному деторождению среди пациенток репродуктивного возраста, что приводит к увеличению частоты различной гинекологической патологии у данной категории пациенток [1].
В России доля бесплодных браков колеблется от 8 до 17,5%, при этом половину среди всех форм бесплодия составляет маточная форма [2].
Как известно, основой патологических процессов, поражающих матку как орган-мишень, является воздействие ряда этиологических факторов: инфекционного, приводящего к развитию хронического эндометрита, что наиболее часто встречается при трубно-перитонеальном бесплодии; дисгормонального, ассоциированного с развитием гиперпластических процессов при эндокринном бесплодии, миомы матки и эндометриоза; сочетанных, ведущих к формированию полипов и внутриматочных синехий [3]. Тем не менее причинно-следственные связи влияния на фертильность миомы матки, полипов эндометрия, хронического эндометрита и ряда других заболеваний остаются неуточненными.
Различная внутриматочная патология наблюдается у 25% пациенток с бесплодием [4]. В последние годы рекомендуется проведение гистероскопии при двух и более неудачных попытках экстракорпорального оплодотворения (ЭКО). При этом в ходе гистероскопии выявляются полипы эндометрия, хронический эндометрит, внутриматочная перегородка, внутриматочные синехии, субмукозная миома матки, которые ранее не были определены при других методах обследования [5, 6]. Частота выявления своевременно или неточно диагностированных заболеваний полости матки у пациенток с повторными безуспешными программами ВРТ составляет от 18 до 50% [4, 6].
В ряде исследований указывается на нецелесообразность рутинной гистероскопии для подтверждения наличия внутриматочной патологии [7]. В то же время необходимость проведения гистероскопии и хирургических внутриматочных манипуляций при субмукозной миоме матки, полипах эндометрия, маточной перегородке как эффективных способах преодоления бесплодия доказана в других исследованиях [8–10]. Так, отмечено увеличение частоты наступления беременности в программе ЭКО после удаления полипов до 51%, после удаления субмукозной миомы матки – до 63%, после рассечения синехий – до 51% [4, 11, 12].
Цель исследования: определить структуру внутриматочной патологии у женщин с бесплодием, готовящихся к проведению программы ЭКО, и оценить значение малоинвазивных внутриматочных вмешательств в отношении результативности последующей программы ЭКО.
Материалы и методы
В исследование были включены 600 пациенток, планирующих реализацию репродуктивной функции в программе ЭКО, обратившихся в отделение вспомогательных технологий в лечении бесплодия им. проф. Б.В. Леонова (руководитель – д.м.н. Калинина Е.А.) ФГБУ НМИЦ АГиП им. академика В.И. Кулакова для проведения программы ЭКО. Всем пациенткам в рамках подготовки к программе ЭКО проводилось клинико-лабораторное обследование в соответствии с Приказом МЗ от 30.09.2012 г. №107н «О порядке использования вспомогательных репродуктивных технологий, противопоказаниях и ограничениях к их применению». Все пациентки соответствовали критериям включения (возраст от 18 до 40 лет, нормальный овариальный резерв, наличие внутриматочной патологии, 2 и более неэффективные программы ЭКО в анамнезе, информированное согласие на участие в исследовании).
Всем пациенткам на 5–8-й день менструального цикла были проведены лечебно-диагностическая гистероскопия в гинекологическом отделении (руководитель – д.м.н., профессор, академик РАН Адамян Л.В.) ФГБУ НМИЦ АГиП им. В.И. Кулакова и последующее морфологическое исследование эндометрия в 1-м патолого-анатомическом отделении (руководитель отделения – д.м.н., профессор А.И. Щеголев).
Гистероскопия проводилось во всех случаях в условиях внутривенной анестезии по стандартной методике с использованием жестких диагностических гистероскопов Hopkins II (Karl Storz GmbH & Co., Германия) с наружным диаметром 5 мм. Полость матки осматривали при наполнении ее стерильным физиологическим раствором хлорида натрия. Подача раствора осуществлялась с помощью помпы Hamou Endomat (Karl Storz GmbH & Co., Германия). Гистероскопия у всех пациенток сочеталась с диагностическим выскабливанием эндометрия и последующим гистологическим исследованием соскобов. При резектоскопии использовали гистерорезектоскоп Karl Storz с наружным диаметром 8 мм, с оптикой 00 и 120 градусов, монополярный ток мощностью 60 Вт в режущем режиме. В качестве среды расширения – 5% раствор глюкозы, создающий оптимальные условия для хорошей визуализации и обладающий диэлектрическими свойствами.
При гистологическом исследовании проводилась фиксация макропрепарата в течение 24 часов в 10% нейтральном растворе формалина; после соответствующей обработки образцов по общепринятой методике они заключались в парафин. Срезы толщиной 5 мкм, подготовленные на роторных микротомах, окрашивали гематоксилином-эозином. Готовые препараты исследовали в световом микроскопе NIKON ECLIPSE 50i при увеличении от ×50 до ×400 с использованием цифрового фотоаппарата марки OLYMPUS 501.
Проведен анализ клинико-анамнестических данных и результатов программы ЭКО после проведения гистероскопии у 351 пациентки (исключив из анализа пациенток с атипической гиперплазией и раком эндометрия), которые были разделены на следующие группы: 1-я группа (n=140) – пациентки с хроническим эндометритом, 2-я группа (n=116) – пациентки с гиперпластическими процессами эндометрия, 3-я группа (n=95) – пациентки с внутриматочной патологией (миома, перегородка, синехии, аденомиоз).
Пациенткам, включенным в исследование, было проведено лечение бесплодия в протоколе ЭКО (ЭКО+ИКСИ) с контролируемой стимуляцией яичников и переносом в полость матки эмбрионов или в цикле с переносом в полость матки ранее криоконсервированных эмбрионов (криопротокол). Программа ЭКО проводилась по стандартному протоколу с препаратами антагониста гонадотропин-рилизинг-гормона. Стимуляция функции яичников проводилась с применением рекомбинантного фолликулостимулирующего гормона. Триггер овуляции вводился при наличии лидирующих фолликулов диаметром 17 мм и более. В качестве триггера овуляции использовался препарат хорионического гонадотропина. Перенос 1 бластоцисты хорошего качества (по классификации D. Gardner и W.B. Schoolcraft) осуществляли на 5-е сутки после проведения трансвагинальной пункции яичников. При подъеме уровня хорионического гонадотропина в сыворотке крови через 14 дней после переноса эмбриона в полость матки регистрировали биохимическую беременность, а при визуализации плодного яйца в полости матки через 21 день после переноса эмбриона – клиническую беременность.
Статистический анализ
Статистический анализ полученных данных производили с использованием программного обеспечения MS Office Excel и Statistica 10.0 (США). Для определения нормальности распределения использовали критерий Колмогорова–Смирнова. Данные с нормальным распределением представлены как среднее значение (стандартное отклонение), для их сравнения использовали параметрический t-критерий Стьюдента. Номинальные данные описывались с указанием абсолютных значений и процентных долей. Сравнение номинальных данных проводилось при помощи критерия χ2. Различия считались статистически значимыми при р<0,05.
Результаты
По данным гистологического исследования (табл. 1) у 36% обследованных женщин был выявлен нормальный по морфологическому строению эндометрий, у 42,7% выявлена доброкачественная патология эндометрия: у 23,3% – хронический эндометрит, у 18,3% – гиперпластические процессы эндометрия: полипы эндометрия и/или железистая гиперплазия (ЖГЭ), у 5,5% женщин выявились атипическая гиперплазия и рак эндометрия. У 15,9% выявлена внутриматочная патология (субмукозная миома матки 0 и I типа до 1,5 см, неполная внутриматочная перегородка, занимающая менее 1/3 полости матки, синехии I–II степени, аденомиоз очаговый или диффузный I–II степени).

Нами проведен углубленный анализ клинико-анамнестических данных и результатов лечения 351 пациентки с различной внутриматочной патологий.
Средний возраст составил 32,0 (0,7) года и статистически не различался по группам: в 1-й группе – 32,5 (0,7) года, во 2-й – 31,4 (0,8), в 3-й группе – 32,1 (0,65) года. При этом важно отметить, что 58% пациенток были в возрасте 30 лет и старше.
Жалобы на бесплодие предъявляли все пациентки, у 22% пациенток это было единственной жалобой. Изменение характера менструальной кровопотери отмечено большинством пациенток (41%): скудные менструации или укорочение менструации до 1–3 дней – у 10% больных, обильные менструации – у 31% больных. Болезненные менструации отмечали 12%, боли в нижних отделах живота, не связанные с менструацией, – 17%, диспареунию – 14,1% пациенток. Жалобы больных по группам были статистически однородны.
Частота перенесенных и сопутствующих заболеваний не различалась между группами.
Менархе в среднем наступило в 12,7 (0,2) года. Длительность менструального цикла – 29,2 (0,6) дня, продолжительность менструаций – 5,2 (0,1) дня. Продолжительность менструаций менее 3 дней отметили 10% больных, обильные менструации – 31%, болезненные менструации – 12% больных.
У всех пациенток, включенных в исследование, отмечены нарушения репродуктивной функции (табл. 2). При анализе данных, представленных в таблице 2, выявлено преобладание частоты вторичного бесплодия (61%). Невынашивание беременности на различных сроках отмечено в анамнезе у 27,6% пациенток. Средняя продолжительность бесплодия составила 5,8 (0,6) года, нарушение репродуктивной функции более 5 лет отмечали 147 (42%) женщин, из них более половины случаев были в группе хронического эндометрита (53%).
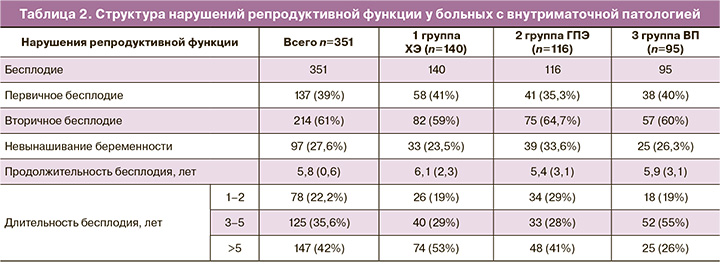
У 214 пациенток с вторичным бесплодием ранее наступившие беременности в 15,2% случаев завершились артифициальными абортами, в 6,1% были внематочные беременности, отмечен высокий процент самопроизвольных потерь беременностей на различных сроках (50,5%). Родами завершились лишь 22% беременностей. Необходимо отметить, что осложнения после абортов или родов отмечены у 37,6% женщин: эндометрит (после аборта или родов) – у 23%, послеродовое кровотечение (ручное обследование, кюретаж послеродовой матки) – у 14,2%.
Более чем половине пациенток (210 из 351, что составило 59,8%) ранее было проведено лечение бесплодия с использованием ВРТ, которое оказалось неэффективным. Одну неудачную попытку ВРТ имели только 18,8%, остальные пациентки (41%) имели 2 и более неэффективные попытки в анамнезе. Средний показатель количества попыток ВРТ составил 2,9 (0,8), неудачных попыток – 2,2 (0,5). Необходимо отметить, что 35% пациенток имели потери беременностей, наступивших после программы ВРТ, на различных сроках.
Анализ данных о перенесенных инфекциях, передаваемых половым путем, и неспецифических воспалительных заболеваниях влагалища показал, что только около трети пациенток не имели в анамнезе инфекций, передающихся половым путем (ИППП). Наличие ИППП отметили 63% женщин, среди которых наиболее часто были хламидиоз (17,9%) и уреаплазмоз (24%).
У большинства пациенток (62%) имело место наличие хронического сальпингоофорита.
Наружный генитальный эндометриоз (НГЭ) был у 27,9% больных, преимущественно I–II ст. (12,5%).
Гиперпластические процессы эндометрия в анамнезе были у 77,8% больных, большее число этих пациенток относилось ко 2-й группе. При этом часть пациенток (14%) имели как полипы, так и гиперплазию эндометрия.
У 132 (37,6%) женщин была выявлена миома матки, однако к моменту проведения данного исследования показаний для проведения дополнительных оперативных вмешательств не было (интрамуральная или субсерозная миома матки малых размеров).
Важным, на наш взгляд, явился анализ перенесенных гинекологических операций, в особенности внутриматочных вмешательств. Различные оперативные вмешательства на органах репродуктивной системы перенесли 58,1% женщин, при этом большая часть из них – несколько оперативных вмешательств, выполненных различными доступами (168 пациенток из 204, что составило 82%). Основными показаниями к операциям были: бесплодие (трубно-перитонеальный фактор), наружный генитальный эндометриоз, миома матки, кисты яичников, внутриматочная перегородка, внутриматочные синехии, кисты яичников и гиперпластические процессы эндометрия и эндоцервикса, а также абортивное течение беременности.
Суммарно было проведено 1127 гинекологических операций: большая их часть была выполнена эндоскопическими (лапароскопическим или гистероскопическим) доступами – 63,6% случаев, лапаротомия – в 12,9% случаев, внутриматочные вмешательства без гистероскопии – в 23,6%.
Необходимо отметить, что у всех пациенток (n=351) были в анамнезе внутриматочные вмешательства (в общей сложности – 625), при этом 1 внутриматочное вмешательство – в 27,8% случаев, 2 внутриматочных вмешательства – в 46,6%, 3 и более внутриматочных вмешательств – в 25,6% случаев. То есть большинство (72,2%) внутриматочных вмешательств носили повторный характер, средний показатель количества внутриматочных вмешательств в анамнезе составил 2,5 (0,4).
Всем 351 пациенткам было проведено оперативное лечение, объем которого зависел от вида внутриматочной патологии (табл. 3).
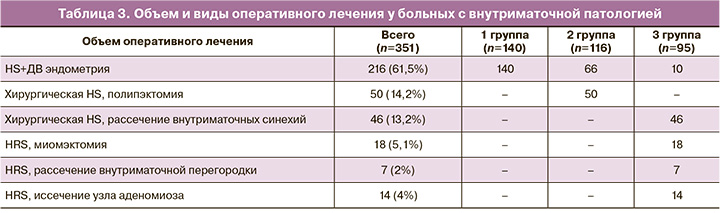
Гистероскопия и диагностическое выскабливание эндометрия/биопсия эндометрия были проведены у 61,5% пациенток, хирургическая гистероскопия или гистерорезектоскопия были проведены у 38,5%. Осложнений во время и после операций не было.
В послеоперационном периоде пациенткам проводилось восстановительное лечение в зависимости от выявленной внутриматочной патологии. Всем пациенткам проводилась антибиотикопрофилактика во время операции и в раннем послеоперационном периоде. Пациенткам с гиперплазией эндометрия проводили гормонотерапию в течение 3–6 месяцев (гестагены). Пациенткам после гистерорезектоскопии, миомэктомии назначалась антибиотикопрофилактика в сочетании с ранней восстановительной физиотерапией. Пациенткам с хроническим эндометритом была проведена циклическая антибиотикотерапия в сочетании с отсроченной физиотерапией (3 м.ц.). Циклическая гормонотерапия на фоне отсроченной физиотерапии проводилась пациенткам с внутриматочными синехиями. При наличии аденомиоза проводили терапию агонистами гонадотропин-рилизинг-гормона (3 месяца) в сочетании с ранней восстановительной физиотерапией.
По окончании курса лечения проводилось контрольное УЗИ на 5–7-й день менструального цикла.
Результаты восстановления репродуктивной функции оценены в течение 1 года после проведения комплексного лечения при использовании методов ВРТ. Пациенткам, включенным в исследование, проводилось лечение бесплодия в программе ЭКО в цикле стимуляции функции яичников с переносом нативных эмбрионов в полость матки или криопротокол. Перенос эмбрионов в цикле стимуляции использовался у 217 (62%) из 351 пациенток, в криопротоколе – у 134 (38%).
Беременность наступила у 178 пациенток из 351, что составило 50,7%: в 1-й группе беременность наступила у 40,7%, во 2-й группе – у 48,3%, в 3-й группе – у 68% пациенток. Внематочные беременности отмечены у 7,3% пациенток. Родами завершилось 53,3% беременностей. Потери беременности отмечены в 39,3% случаях. Кесарево сечение было методом родоразрешения в 72% случаях, самопроизвольные роды – в 28% случаях. Исходы беременностей по группам представлены в таблице 4.
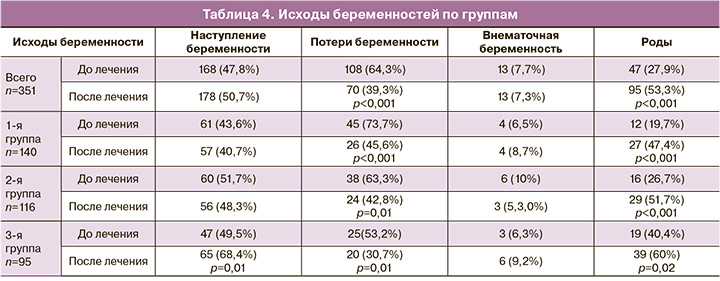
У пациенток с внутриматочной патологией при анализе исходов беременностей, наступивших после проведенного лечения, отмечено статистически значимое различие в частоте потерь беременности до и после лечения: уменьшение частоты потерь беременности в целом в 1,5 раза среди включенных в исследование 351 пациентки (64,3% и 39,3% соответственно, p<0,001); статистически значимое увеличение частоты родов по сравнению с аналогичным показателем до лечения в 2 раза (27,9% и 53,3% соответственно, p<0,001).
Таким образом, хирургическое и последующее восстановительное лечение внутриматочной патологии у больных бесплодием способствовало уменьшению частоты потерь беременности, наступивших в результате программы ЭКО, и увеличению частоты беременностей, завершившихся родами.
Особый интерес, по нашему мнению, представляет оценка клинико-анамнестических данных и результатов лечения у группы пациенток с двумя и более неэффективными попытками ВРТ в анамнезе, а также выявление факторов риска повторных неудач. По данным нашего исследования, две и более неэффективные попытки ВРТ отмечены у 41% (144 пациентки из 351). Мы посчитали целесообразным разделить этих пациенток ретроспективно на две группы в зависимости от результатов программы ЭКО после хирургического лечения. В группу А вошли 87 пациенток с отсутствием беременности после проведенной программы ВРТ, в группу Б – 57 женщин с наступившей и подтвержденной при УЗИ беременностью в результате ВРТ.
Пациентки, включенные в исследование, получали лечение бесплодия в протоколе ЭКО (ЭКО+ИКСИ) с контролируемой стимуляцией яичников и переносом в полость матки эмбрионов или в цикле с переносом в полость матки криоконсервированных эмбрионов (криопротокол). Протокол ЭКО (ЭКО+ИКСИ) использовался у 57,4% пациенток группы А и у 52% пациенток группы Б, лечение в цикле криопротокола получали 43,7% пациенток группы А и 47,4% пациенток группы Б.
Средний возраст женщин в группе А составил 34,4 (3,9) года, женщин в группе Б – 32,1 (4,7) года (p<0,001). При сравнении групп А и Б отмечено статистически значимо большее число пациенток в возрасте 35 лет и старше в группе женщин с неэффективной попыткой ВРТ после проведенного хирургического лечения (56% и 31,6% соответственно, p<0,001).
По количественным и качественным характеристикам менструального цикла пациентки сравниваемых групп не отличались: возраст менархе составил 12,7 (1,2) года, длительность менструального цикла в среднем 28,8 (0,8) дня, продолжительность менструаций – 4,22 (1,2) дня.
Статистически значимых различий в показателях репродуктивной функции пациенток сравниваемых групп выявлено не было. Отмечено лишь статистически значимое преобладание доли женщин с первичным бесплодием в группе с неэффективной последующей программой ВРТ (49% и 32% соответственно, p=0,02).
Пациентки с повторными неудачами в программах ЭКО имели высокую распространенность гинекологических заболеваний. ИППП и воспалительные заболевания органов малого таза чаще диагностировались у пациенток с повторными неудачами в программах ЭКО (52% и 66,6%). НГЭ был третьим по частоте гинекологическим заболеванием у обследованных пациенток (46,5%). Отмечено статистически значимое преобладание доли пациенток с хроническим сальпингоофоритом (73,6% и 36% соответственно, p<0,001) и эндометриозом (53% и 36,8% соответственно, p=0,02) среди пациенток группы А по сравнению с пациентками группы Б.
На момент вступления в текущий протокол программы ВРТ каждая пациентка имела в анамнезе одно или несколько внутриматочных вмешательств, которые производились с диагностической или лечебной целью. Отмечено статистически значимое преобладание доли пациенток с 3 и более внутриматочными вмешательствами в анамнезе в группе с неудачной попыткой ЭКО (64,4% и 46% соответственно, p=0,01), а также среднего числа внутриматочных вмешательств [3,05 (0,36) и 2,66 (0,26)], p<0,001). Следовательно, с увеличением числа (3 и более) различных внутриматочных вмешательств в анамнезе увеличивается вероятность повторных неудачных попыток ВРТ.
Операции на органах малого таза были в анамнезе у 64,12% пациенток и не различались по группам.
Длительность бесплодия включенных в исследование пациенток на момент обращения в среднем составила 5,04 (0,4) года для пациенток группы А и 5,25 (0,52) года для пациенток группы Б. Частота наступления беременности после программ ЭКО составляла 5,5% в расчете на процедуру переноса эмбрионов (5,38% для пациенток группы А и 5,71% для пациенток группы Б), при этом ни одна из наступивших беременностей не завершилась родами.
По перенесенным в анамнезе соматическим заболеваниям и оперативным вмешательствам пациентки не отличались.
В рамках подготовки к программе ВРТ всем пациенткам с повторными неудачами ЭКО в анамнезе проводились гистероскопия и биопсия эндометрия. Хронический эндометрит выявлен у 25%, миома матки – у 17,4%, гиперплазия эндометрия – у 13,9%, полипы эндометрия – у 31%, внутриматочные синехии были диагностированы у 19,4%, аденомиоз – у 16%, аномалия развития матки (неполная внутриматочная перегородка) – у 4,2% женщин. Нами отмечено статистически значимое преобладание числа пациенток с выявленным при гистероскопии и биопсии эндометрия хроническим эндометритом в группе А по сравнению с группой Б (32,2% и 14% соответственно, p=0,006).
Таким образом, различная внутриматочная патология, потребовавшая гистероскопической оценки и лечения, отмечена у 58,5% женщин с бесплодием. Хирургическое и последующее восстановительное лечение внутриматочной патологии у больных бесплодием способствовало уменьшению частоты потерь беременности, наступивших в результате программы ЭКО, и увеличению частоты беременностей, завершившихся родами.
По данным нашего исследования, две и более неэффективные попытки ВРТ отмечены у 41%. Факторами, ассоциированными с высокой вероятностью повторных неудач ВРТ у пациенток с внутриматочной патологией, являются:
- возраст женщины при вступлении в программу ВРТ старше 35 лет;
- хронический сальпингоофорит, НГЭ и хронический эндометрит;
- наличие 3 и более различных внутриматочных вмешательств в анамнезе.
Обсуждение
Анализ структуры выявленной внутриматочной патологии у женщин с бесплодием, готовящихся к проведению программы ЭКО, по данным нашего исследования, показал преобладание хронического эндометрита, который отмечен в 23,3% случаев, внутриматочной патологии (субмукозная миома, внутриматочная перегородка, синехии и аденомиоз) – в 15,9%, полипов эндометрия – в 13,3% случаев. Полученные нами данные согласуются с ранее проведенными работами, в которых также подтверждена высокая частота выявления различной внутриматочной патологии и патологии эндометрия у больных бесплодием [12–16].
Гистероскопия обладает более высокой чувствительностью и специфичностью в выявлении внутриматочной патологии в сравнении с трансвагинальным ультразвуковым исследованием, при этом неоспоримым преимуществом гистероскопии является возможность не только диагностировать различную внутриматочную патологию, но и провести ее одновременное лечение (принцип «see-and-treat»). В ходе проведенного нами исследовании подтверждено повышение частоты наступления беременности после гистероскопии в циклах ЭКО, так, гистероскопия (диагностическая и/или оперативная) и последующее восстановительное лечение внутриматочной патологии способствовали в 1,5 раза уменьшению частоты потерь беременности и увеличению частоты беременностей, завершившихся родами, что совпадает с данными, приведенными в метаанализе A. Di Spiezio Sardo и соавт. [15], и данными крупных зарубежных рандомизированных контролируемых исследований [17, 18]. На наш взгляд, необходимо включение гистероскопии в обследование пациенток с бесплодием, особенно у пациенток с неэффективными программами ЭКО в анамнезе, что позволяет своевременно диагностировать и устранять внутриматочную патологию и дает возможность повысить результативность лечения бесплодия.
Заключение
Таким образом, гистероскопическая оценка состояния полости матки, а также гистологическое и иммуногистохимическое исследования эндометрия позволяют выявить патологические изменения эндометрия, различную внутриматочную патологию и провести при необходимости хирургическое лечение, способствующее увеличению частоты наступления беременности при использовании методов ВРТ.



