Качество гамет, в первую очередь качество ооцитов, оказывает большое влияние на исходы программ вспомогательных репродуктивных технологий (ВРТ), влияя на способность эмбриона к развитию и имплантации. О качестве ооцита можно судить по его морфологии. Многие ооциты, полученные в циклах стимуляции яичников, имеют различные морфологические аномалии, или дисморфизмы [1], которые можно увидеть после денудации ооцитов в световой микроскоп при проведении процедуры интрацитоплазматической инъекции сперматозоидов (ИКСИ). Морфологической оценке качества ооцитов на практике придается мало значения, хотя наличие дисморфизмов оказывает существенное влияние на исходы программ ВРТ. Аномальные агрегаты гладкого эндоплазматического ретикулума (ГЭР) – это нарушение морфологии ооцитов в виде появления в цитоплазме полупрозрачных вакуолеподобных образований [2, 3]. Данная аномалия встречается только в зрелых ооцитах, полученных в циклах стимуляции функции яичников [4]. Аномальные агрегаты состоят из крупных скоплений трубочек ГЭР [2, 3]. Основными функциями эндоплазматического ретикулума являются хранение и перераспределение кальция, участие в механизмах накопления энергии, синтеза липидов и триглицеридов, а также синтеза плазматических и ядерных мембран [5].
Результаты исследований агрегатов ГЭР на параметры эмбриогенеза и исходы программы ВРТ на данный момент противоречивы. В работах многих авторов было показано негативное влияние агрегатов ГЭР на частоту оплодотворения, качество полученных эмбрионов, наступление беременности, а также здоровье детей [4, 6]. По этой причине две исследовательские группы, Alfa Scientists in reproductive medicine и Европейское общество репродукции человека и эмбриологии (ESHRE), рекомендуют отказаться от оплодотворения ооцитов с агрегатами ГЭР. По данным мультицентрового обсервационного исследования, среди 138 европейских центров от оплодотворения ооцитов с агрегатами ГЭР отказались 13,8%. Тем не менее, у некоторых пациенток невозможно получить морфологически нормальные ооциты, что вынуждает использовать в программах ВРТ ооциты с данной патологией. В связи с этим в 54% европейских центров такие ооциты оплодотворяются, но перенос эмбрионов осуществляется только в случае отсутствия других эмбрионов достаточного качества [7]. Российских рекомендаций по оплодотворению аномальных ооцитов не существует, по этой причине ооциты с агрегатами ГЭР используют в циклах экстракорпорального оплодотворения (ЭКО) наравне с морфологически нормальными ооцитами.
На сегодняшний день невозможно предотвратить и спрогнозировать появление агрегатов ГЭР в цитоплазме ооцита, так как причины, факторы риска и механизмы их развития остаются недостаточно изученными. В работах некоторых авторов на появление данной аномалии оказывали влияние уровни антимюллерова гормона (АМГ) и эстрадиола в сыворотке крови, а также применение для стимуляции функции яичников более высокой начальной и суммарной дозы гонадотропинов [4, 6, 8, 9].
Цель исследования: оценить влияние агрегатов ГЭР в цитоплазме ооцитов на эмбриологические характеристики и клинические исходы программ ВРТ, а также выявить их клинические предикторы.
Материал и методы исследования
В проспективное когортное исследование были включены 162 супружеские пары с бесплодием различного генеза, нормальным кариотипом, отсутствием противопоказаний к проведению ВРТ и подписанным информированным согласием на участие в исследовании. Все пациентки были разделены на 2 группы: группа 1 – женщины с агрегатами ГЭР в цитоплазме ооцитов, группа 2 – женщины с морфологически нормальными ооцитами. Критерием отнесения пациенток в группу с дисморфизмами было наличие 100% ооцитов с патологией, в контрольную группу – наличие 100% нормальных ооцитов. Критериями исключения явилось наличие тяжелой формы патозооспермии у мужчины (концентрация сперматозоидов менее 100 000/мл, наличие менее 4% морфологически нормальных сперматозоидов по строгим критериям Крюгера, а также наличие азооспермии). Другими критериями исключения служили развитие синдрома гиперстимуляции яичников средней или тяжелой степени в данном цикле ЭКО, а также другие причины и осложнения, требующие отмены переноса эмбрионов в изучаемом цикле. Перед включением в протокол ЭКО все женщины были обследованы согласно Приказу Минздрава России от 30.08.12 №107н «О порядке использования вспомогательных репродуктивных технологий, противопоказаниях и показаниях к их применению».
Стимуляция функции яичников проводилась по протоколу с антагонистами гонадотропин рилизинг-гормона (ГнРГ) с применением рекомбинантного ФСГ или комбинированного препарата рекомбинантного ФСГ и ЛГ. Триггер овуляции вводился при наличии лидирующих фолликулов в яичниках диаметром 17 мм и более. В качестве триггера овуляции использовали человеческий хорионический гонадотропин (ЧХГ) в дозе 8000–10 000 МЕ, а при риске развития синдрома гиперстимуляции яичников (при наличии более 15 доминантных фолликулов в обоих яичниках в день назначения триггера овуляции) – агонист ГнРГ в дозе 0,2 мг или сочетание агониста ГнРГ с низкими дозами ЧХГ (1500 МЕ).
Поддержка лютеиновой фазы индуцированного цикла у всех пациенток проводилась по стандартному протоколу с назначением натурального микронизированного прогестерона интравагинально в дозе 600 мг в сутки после трансвагинальной пункции яичников. При этом если в качестве триггера овуляции был использован агонист ГнРГ, или сочетание агониста ГнРГ с ЧХГ в дозе 1500 МЕ, для поддержки лютеиновой фазы назначали также эстрадиола валерат 6 мг/сутки и препарат ЧХГ (хорагон 1500 МЕ).
Очищение ооцитов от клеток кумулюса осуществляли как энзимным, так и механическим путем; зрелые клетки на стадии МІІ культивировали отдельно от незрелых. Морфологическая оценка ооцитов проводилась эмбриологом во время проведения процедуры ИКСИ, после оплодотворения ооциты культивировались в отдельных каплях. Оценка оплодотворения проводилась через 16-18 часов после проведения ИКСИ. Нормальное оплодотворение регистрировали при наличии двух пронуклеусов в цитоплазме ооцита. Морфологическую оценку качества развивающихся эмбрионов проводили на 3-и сутки культивирования, в качестве критериев оценки использовали скорость дробления, симметрию бластомеров, а также наличие фрагментации в отдельных бластомерах. Перенос эмбрионов в полость матки осуществляли на 4-е или 5-е сутки культивирования. При наличии подъема уровня сывороточного ЧХГ через 14 дней после переноса эмбрионов в полость матки регистрировали биохимическую беременность, а при визуализации плодного яйца в полости матки через 21 день после переноса – клиническую беременность.
 Для статистического анализа использовался пакет статистических программ Statistica 10 (США). Расчет объема выборки был основан на данных литературы о частоте наступления беременности в программах ВРТ у пациенток с агрегатами ГЭР в цитоплазме ооцитов [10]. Первичной конечной точкой явилось скорректированное отношение шансов (ОШкор) развития ооцитов с агрегатами ГЭР в зависимости от выявленных факторов риска. Вторичной конечной точкой явилось ОШкор наступления клинической беременности в изучаемых группах. Статистический анализ проводился с применением χ2-теста для оценки частотных показателей, t-теста для сравнения непрерывных величин, а также многофакторного регрессионного анализа (логистической регрессии) для расчета ОШкор. Корреляционный анализ проводился с использованием непараметрического корреляционного критерия Спирмена. Различия между статистическими величинами считали статистически значимыми при уровне достоверности р<0,05.
Для статистического анализа использовался пакет статистических программ Statistica 10 (США). Расчет объема выборки был основан на данных литературы о частоте наступления беременности в программах ВРТ у пациенток с агрегатами ГЭР в цитоплазме ооцитов [10]. Первичной конечной точкой явилось скорректированное отношение шансов (ОШкор) развития ооцитов с агрегатами ГЭР в зависимости от выявленных факторов риска. Вторичной конечной точкой явилось ОШкор наступления клинической беременности в изучаемых группах. Статистический анализ проводился с применением χ2-теста для оценки частотных показателей, t-теста для сравнения непрерывных величин, а также многофакторного регрессионного анализа (логистической регрессии) для расчета ОШкор. Корреляционный анализ проводился с использованием непараметрического корреляционного критерия Спирмена. Различия между статистическими величинами считали статистически значимыми при уровне достоверности р<0,05.
Исследование было одобрено этическим комитетом ФГБУ НЦАГиП им. акад. В.И. Кулакова Минздрава России.
Результаты
При оценке клинико-анамнестических характеристик не было выявлено статистически значимых различий по возрасту (34,2±5,6 года в группе 1 и 33,8±5,4 года в группе 2, p=0,7962) и индексу массы тела пациенток (в группе 1 – 22,7±2,8 кг/м2, в группе 2 – 23,5±4,4 кг\м2, p=0,5678). Социально-экономические характеристики (уровень образования, семейное положение, наличие или отсутствие работы) не различались в группах сравнения. Женщины обеих групп не отличались по менструальной функции, соматической заболеваемости и наличию вредных привычек, хотя в группе женщин с агрегатами ГЭР было погранично значимо большее число курящих женщин (4 человека, 7,3%) по сравнению с группой контроля (2 человека, 1,9%) (р=0,0846).
Пациентки с агрегатами ГЭР чаще имели в анамнезе хламидийную инфекцию – 9 пациенток (16,4%) в группе 1 и 4 пациентки (3,8%) в группе 2 (р=0,0500) и рецидивирующий генитальный герпес (ГГ) – 5 женщин из группы 1 (9,1%) и 2 женщины (1,9%) из группы 2 (р=0,0476). Все пациентки, имевшие в анамнезе хламидийную инфекцию, получали антибактериальную терапию с последующим лабораторным контролем излеченности. ГГ у всех пациенток протекал типично в виде периодических рецидивов (везикулярные высыпания на наружных половых органах и промежности) со средним числом рецидивов (6,3±1,2) в течение года. Диагноз был верифицирован с помощью исследования мазков с очага поражения в момент рецидива. Последний рецидив отмечался в среднем за 1,5±0,5 месяца до вступления в программу ЭКО. Все пациентки получали терапию препаратами ацикловира короткими курсами в период обострения ГГ. Условием вступления в программу ЭКО было отсутствие клинических проявлений ГГ на момент начала стимуляции суперовуляции.
Две группы пациенток значимо не различались по наличию в анамнезе таких гинекологических патологий, как эндометриоз, хронический сальпингоофорит, миома матки, синдром поликистозных яичников, заболевания шейки матки.
Акушерский анамнез, причина и длительность бесплодия, а также количество проведенных циклов ЭКО/ИКСИ в анамнезе не различались в группах сравнения.
При оценке лабораторных данных пациенток не было выявлено значимых различий в показателях клинического и биохимического анализа крови, гемостазиограммы и общего анализа мочи в группах сравнения. При анализе гормонального профиля, определяемого однократно на 3-й день менструального цикла у каждой пациентки, статистически значимых различий в уровнях АМГ, ФСГ, ЛГ, пролактина, соматотропного гормона, тиреотропного гормона, свободного тироксина, эстрадиола, 17-ОН-прогестерона и дегидроэпиандростерон-сульфата выявлено не было. Уровень тестостерона был погранично значимо ниже в группе 1 (1,3±0,7 нмоль/л) по сравнению с группой 2 (1,6±0,9 нмоль/л, р=0,0830).
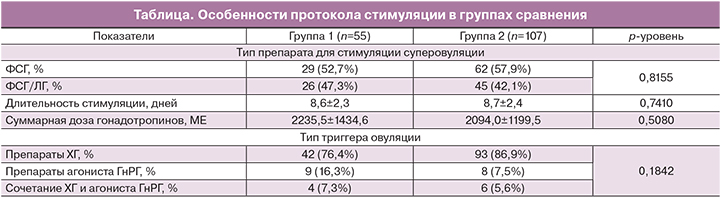
При оценке возможного влияния на развитие дисморфизмов ооцитов ятрогенных факторов было выявлено, что частота назначения различных препаратов для стимуляции функции яичников (ФСГ или ФСГ/ЛГ) не различалась в группах сравнения. Также на морфологию ооцитов не повлияли длительность стимуляции функции яичников и суммарная доза гонадотропинов (таблица).
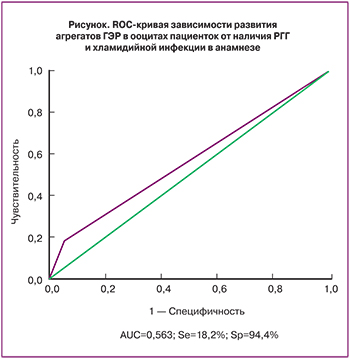
Таким образом, на риск развития агрегатов ГЭР в ооцитах в однофакторном анализе оказывали влияние такие факторы как курение, уровень тестостерона, наличие рецидивирующего ГГ и хламидийной инфекции в анамнезе. В созданной модели с помощью метода логистической регрессии было выявлено, что значимое влияние на развитие агрегатов ГЭР в ооцитах оказывало лишь наличие рецидивирующего ГГ и хламидийной инфекции в анамнезе. ОШкор появления ооцитов с агрегатами ГЭР у пациенток в циклах ЭКО в зависимости от наличия хламидийной инфекции в анамнезе и/или рецидивирующего ГГ составило 3,7 (95% ДИ 1,3; 10,9). В данной модели площадь под кривой (AUC – англ. – area under the curve) составила 56,3% (рисунок). Созданная модель обладала низкой чувствительностью (Se=18,2%), но высокой специфичностью (Sp=94,4%).
При оценке параметров фолликулогенеза и оогенеза были выявлены статистически значимые различия между группами. Число фолликулов в день назначения триггера овуляции было выше у пациенток с агрегатами ГЭР в цитоплазме ооцитов и составило 10,3±5,6 в группе 1 и 8,4±4,9 в группе 2 (р=0,0393). В результате у пациенток в группе 1 было получено больше ооцит-кумулюсных комплексов (7,6±4,7 в группе 1 и 5,8±3,6 в группе 2, р=0,0158) и зрелых ооцитов (6,6±4,2 в группе 1 и 4,9±3,4 в группе 2, р=0,0077).
Всего в циклах стимуляции было получено 946 зрелых ооцитов на стадии МII, из них 317 ооцитов с агрегатами ГЭР в цитоплазме и 629 морфологически нормальных клеток. С помощью метода логистической регрессии было оценено влияние числа полученных зрелых ооцитов на развитие агрегатов ГЭР. Указанная переменная была представлена в виде бинарной величины с определением порога отсечки (10 ооцитов), при которых созданная модель была максимально достоверной. ОШ появления ооцитов с агрегатами ГЭР при получении более 10 ооцитов у пациенток в циклах ЭКО составило 3,3 (95% ДИ 1,1; 9,8).
Частота оплодотворения ооцитов статистически значимо различалась между группами пациенток. В группе 1 нормально оплодотворился 261 ооцит (82,3%), а в группе 2 – 556 ооцитов (88,4%) (р=0,0103).
В группах сравнения производилась оценка доли эмбрионов разных классов (А, В и С) на 3-и сутки культивирования, а также доли эмбрионов, остановившихся в развитии на раннем этапе культивирования. Из полученных зигот эмбрионов класса А было 115 (44,1%) в группе 1 и 365 (65,7%) в группе 2 (р?0,0001), эмбрионов класса В было 104 (39,9%) в группе 1 и 152 (27,3%) во группе 2 (р=0,0003), а эмбрионов класса С – 32 (12,2%) и 29 (5,2%) (р=0,0018) в группах 1 и 2 соответственно. Число эмбрионов, остановившихся в развитии, оставило 10 (3,8%) в группе 1 и 10 (1,8%) в группе 2 (р<0,0001).
После переноса эмбрионов биохимическая беременность наступила у 7 (12,7%) пациенток группы 1 и у 44 (41,1%) пациенток группы 2 (р=0,0002). Клиническая беременность наступила у 7 (12,7%) пациенток группы 1 и 43 (40,2%) пациенток группы 2 (р=0,0003). Таким образом, беременность наступала в 4,6 раза реже у женщин с агрегатами ГЭР ооцитов (грубое отношение шансов, ОШгр=4,6; 95% ДИ=1,9; 11,1). Помимо морфологии ооцитов, на частоту наступления беременности оказывало влияние число полученных зрелых ооцитов. ОШкор наступления клинической беременности при наличии агрегатов ГЭР в цитоплазме ооцитов составило 4,1 (95% ДИ 1,7; 9,9).
Частота самопроизвольных прерываний беременностей была выше у пациенток при наличии дисморфизмов ооцитов. Было диагностировано 16 потерь беременности в сроке до 12 недель гестации: 3 – в группе 1 (42,9% от общего числа беременностей в этой группе) и 7 – в группе 2 (16,3% от общего числа беременностей в этой группе) (р<0,0001). ОШгр потери беременности в I триместре при наличии аномальных ооцитов составило 3,9 (95% ДИ=0,45; 28,01).
Обсуждение
В настоящее время процедура ЭКО становится все более востребованной при лечении бесплодных пар. Следовательно, возрастает потребность в развитии методов диагностики и прогноза данного метода. Определение морфологии полученных ооцитов может стать значимым и широкодоступным способом прогнозирования исхода программ ЭКО.
В ходе проведенного нами исследовании были выявлены факторы риска появления агрегатов ГЭР в ооцитах и проведена оценка влияния данной аномалии на вероятность оплодотворения, качество полученных эмбрионов, а также частоту наступления беременности и ранних репродуктивных потерь.
Наше исследование показало, что наличие рецидивирующего ГГ или хламидийной инфекции в анамнезе увеличивает риск появления аномальных ооцитов у пациенток. При этом другие гинекологические заболевания, акушерский анамнез, гормональный статус, а также особенности стимуляции функции яичников не влияют на образование аномальных ооцитов. Кроме того, было показано, что при получении у пациентки более 10 зрелых ооцитов увеличивается вероятность появления агрегатов ГЭР.
Ни в одном предшествующем исследовании на данный момент не была обнаружена связь между наличием в анамнезе рецидивирующего ГГ и хламидийной инфекции и появлением агрегатов ГЭР в ооцитах. Возможный механизм влияния пока не установлен. Известно, что липополисахаридный комплекс бактерий увеличивает секрецию интерлейкина 6 ооцит-кумулюсным комплексом у коров и частоту остановки развития ооцита на стадии мейоза по Toll-like receptor 4-опосредованному пути [11]. Возможно, по этому пути происходят нарушения, приводящие к появлению ооцитов с агрегатами ГЭР.
Вирус простого герпеса (ВПГ) 1-го и 2-го типов чаще встречается у пациенток с бесплодием, чем у здоровых женщин. Известно негативное влияние ВПГ 1-го и 2-го типов на имплантацию эмбриона по причине повышенной активности цитотоксических клеток иммунной системы. Также в литературе описана гибель эмбрионов при контакте с инфицированным эндометрием. На данный момент влияние рецидивирующего ГГ на качество ооцитов изучено мало. ВПГ инфицирует все органы, иннервируемые пудендальным нервом, в том числе яичники. В литературе описано, что ВПГ оказывает повреждающее воздействие на геном инфицированной клетки, снижает ее синтетическую активность и негативно влияет на функцию микрофиламентов [12–14]. Данные нарушения могут приводить к появлению агрегатов ГЭР в ооцитах пациенток, а также препятствовать оплодотворению ооцитов.
Нами было выявлено снижение эффективности циклов ЭКО у женщин с аномальными ооцитами. Ооциты с агрегатами ГЭР имели меньшую частоту оплодотворения. Эмбрионы, полученные из аномальных ооцитов, были более низкого качества, и среди них было больше непригодных к переносу в полость матки по сравнению с эмбрионами из нормальных ооцитов. В парах с агрегатами ГЭР у пациенток наблюдалась меньшая частота наступления биохимической и клинической беременности. У пациенток с аномальными ооцитами клиническая беременность наступала в 4,1 раза реже, а частота ранних репродуктивных потерь была в 3,8 раза выше.
Заключение
Таким образом, в результате проведенного исследования было доказано существенное негативное влияние агрегатов ГЭР на исходы программ ВРТ, а также выявлены факторы риска возникновения данной патологии. Несомненно, данная проблема требует дальнейшего изучения, поиска причин и механизмов возникновения данного дисморфизма, создания оптимальной тактики ведения пациенток с патологией ооцитов.



