Впервые эндопротезирование молочных желез было выполнено в 1962 г. в США Френком Джероу и Томасом Крониным, пластическими хирургами. Значение силиконовых имплантов в эстетической и реконструктивной хирургии в настоящее время тяжело переоценить. Ежегодно в мире проводится около 2 миллионов операций с эндопротезированием молочных желез. По данным Американского общества пластической хирургии (ASPS), за 2018 г. в США было выполнено 313 785 аугментаций молочных желез, 83 2116 реконструкций молочных желез с использованием имплантов. Импланты нашли широкое применение при гипоплазии молочных желез, выраженном птозе после кормления, врожденных аномалиях развития, а также при одномоментной или отсроченной реконструкции после мастэктомий. Со времен первой аугментации молочных желез поменялось несколько поколений имплантов. В настоящее время наиболее часто используют текстурированные силиконовые импланты с гелевым наполнителем. Безопасность и эффективность имплантов, представленных на сегодняшний день, находится под контролем FDA (Управление по контролю за пищевыми продуктами и лекарственными веществами, США). Однако, несмотря на безопасность современных силиконовых имплантов, сохраняется вероятность возникновения осложнений после эндопротезирования молочных желез. К наиболее распространенным специфическим осложнениям относят: возникновение капсулярной контрактуры, разрыв импланта, косметические деформации, пролежни.
Для визуализации имплантов молочных желез используют такие методы, как маммография, ультразвуковое исследование (УЗИ), магнитно-резонансная томография (МРТ) и компьютерная томография (КТ). Чувствительность и специфичность КТ-маммографии в диагностике разрыва импланта молочной железы составляет 98,4% и 98,9%, в то время как рентгеновской маммографии – 7,7% и 94,8%, УЗИ – 21,5% и 71,8%, а МР-маммографии – 77,0% и 80,4% соответственно [1]. Разрывы импланта могут быть экстракапсулярными и интракапсулярными.
Однако по мере использования безопасность эндопротезов была подвергнута сомнению, в том числе из-за местных и системных побочных реакций.
Местные реакции: разрыв имплантата, утечка геля через оболочку, фрагментация эластомеров, фиброз и контрактура капсулы – изучены достаточно хорошо.
Системное воздействие силикона, в первую очередь возможные системные реакции соединительной ткани, сдвиги иммунологической реактивности и развитие аутоиммунных заболеваний до сих пор остаются предметом дискуссий; получаемые данные противоречивы. Начиная с 1984 г. различные авторы описали у носителей силиконовых имплантатов широкий спектр аутоиммунных заболеваний в когортах разной численности пациентов (3–11 800), среди них: ревматоидный артрит, системная красная волчанка, полимиозит и склеродермия, синдром Шегрена, смешанное заболевание соединительной ткани. Относительный риск возникновения всех известных системных аутоиммунных заболеваний соединительной ткани составил 1,25 (95% доверительный интервал 1,08–1,41) [2].
Клиническое наблюдение
Пациентка Т., 1971 г.р., из анамнеза известно, что в 2002 г. по поводу гипоплазии и птоза молочных желез после лактации пациентке выполнена двусторонняя аугментационная маммопластика текстурированными силиконовыми имплантами McGhan 300 см3 (рис. 1).
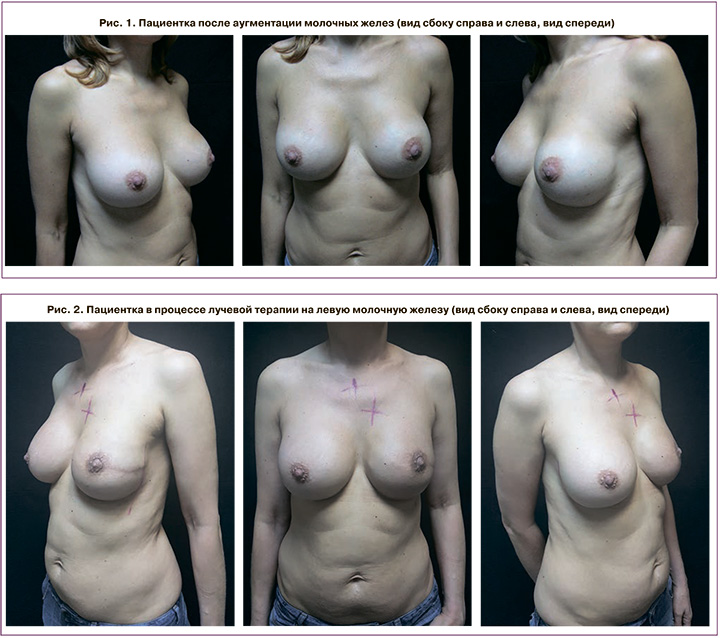
В октябре 2017 г. у пациентки диагностирован рак левой молочной железы IIА стадии pT1N1MoG2, люминальный тип В, Her2-негативный. На первом этапе 28.11.2017 г. в МНИОИ им. П.А. Герцена больной выполнена радикальная подкожная мастэктомия слева с одномоментной реконструкцией эндопротезом Рolyteсh Replicon 20736-445.
Диагностика рака молочных желез у пациентки не отличалась от пациенток без аугментации молочной железы и основана на маммографии, УЗИ молочных желез, биопсии и иммуногистохимии (ИГХ) опухолевого узла [3].
При плановом гистологическом исследовании № АГ 14291-309/оп: опухолевый узел 1,5×0,8×1,3 см представлен инфильтративным раком молочной железы без признаков специфичности, 2 степени злокачественности (7 баллов). В краях резекции – без опухолевого роста. В 1 из 8 исследованных лимфатических узлов – метастаз рака без признаков специфичности, с выходом за пределы капсулы узла; в остальных – гистиоцитоз синусов, очаговое жировое замещение лимфоидной ткани. ИГХ ER 8, PR 8, Her2/neu 0, Ki67 38 % – люминальный тип В, Неr2-негативный. Решением консилиума с участием хирурга, химиотерапевта и радиолога пациентке рекомендовано лечение: адъювантная химиотерапия по схеме 4АС+4Т, дистанционная лучевая терапия на область левой молочной железы РОД 2,5 Гр, СОД 50 Гр-экв, на пути регионарного лимфооттока РОД 2,5 Гр, СОД 45 Гр-экв. (рис. 2), гормональная терапия тамоксифеном (по настоящее время).
В мае 2019 г. пациентка обратилась в МНИОИ им. П.А. Герцена в связи с появлением боли в левой молочной железе. Объективно деформирован контур левой молочной железы: клиническая ситуация расценена как капсулярная контрактура III степени по Бейкеру (рис. 3); для лечения контрактуры выполнено хирургическое лечение, а именно, замена полиуретанового импланта на текстурированный.
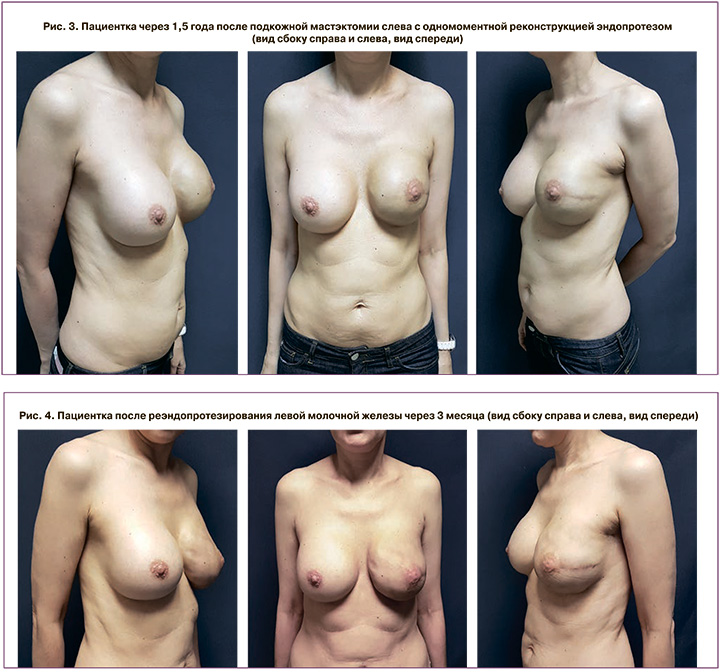
26.06.2019 выполнена замена эндопротеза левой молочной железы на эндопротез Mentor CPG 332 495cc.
Интраоперационно диагностирована гематома в области реконструированной левой молочной железы в объеме 100 мл, иссечена капсула эндопротеза. После замены импланта и удаления гематомы пациентка консервативно лечилась дициноном в течение 5 дней. Вид пациентки после реэндопротезирования левой молочной железы – достигнут хороший косметический результат (рис. 4).
По данным обследования от 23 сентября 2019 г. на ПЭТ-КТ диагностирована деформация импланта правой молочной железы, местами с нарушением целостности. Рекомендовано УЗИ молочных желез. На момент исследования ПЭТ-КТ с 18F-ФДГ очагов патологического метаболизма неопластического характера не выявлено (рис. 5).
Пациентка обратилась в МНИОИ им. П.А. Герцена. Жалоб не предъявляла. При осмотре: молочные железы симметричные; на коже обеих молочных желез послеоперационные рубцы: справа – горизонтальный рубец в области субмаммарной складки; слева – горизонтальный рубец в области субмаммарной складки и периареолярный рубец с продолжением по границе наружных квадрантов. При пальпации обеих молочных желез узловые образования не определяются. В обеих подмышечных областях увеличенные лимфатические узлы не пальпируются.
УЗИ молочных желез от 24.09.2019: в подмышечных лимфатических узлах – без патологии. В правой молочной железе – эндопротез с дефектами целостности в разных местах в пределах ложной капсулы. Заключение: картина нарушения целостности протеза правой молочной железы в нескольких местах (рис. 6).
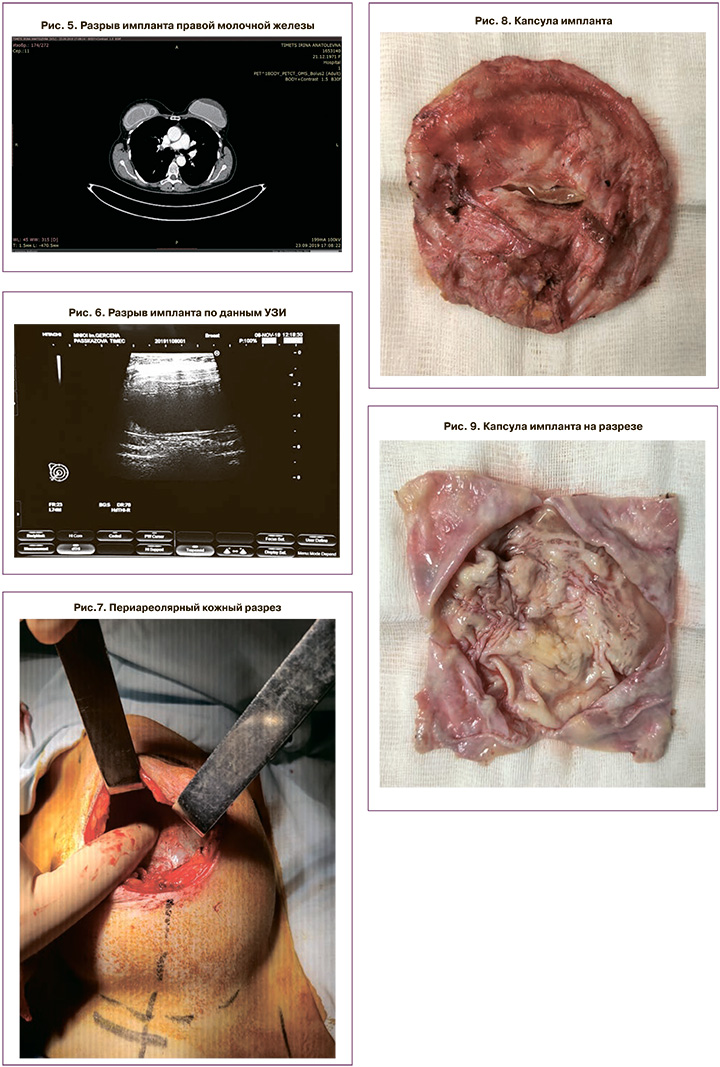
11.11.2019 г. пациентке выполнена замена импланта правой молочной железы на Mentor 330 сс СРG 312.
Кожный разрез – периареолярный для лучшего доступа к импланту (рис. 7).
При ревизии: имплант установлен субмускулярно; целостность капсулы импланта не нарушена, отсутствует экстракапсулярный выход гелевого содержимого импланта. Имплант удален в пределах капсулы (рис. 8–9).
Рассечена капсула импланта, в результате чего отмечен выход гелевого содержимого, весь гель удален. Выполнена капсулэктомия (рис. 9). Субумускулярно установлен текстурированный силиконовый имплант. В послеоперационном периоде не отмечено осложнений. Пациентка выписана на 4-е сутки после операции.
Обсуждение
Таким образом, за 2 года пациентке выполнено три хирургических вмешательства на молочных железах, ранее аугментированных: 1) подкожная мастэктомия слева с эндопротезированием, 2) замена эндопротеза слева из-за возникновения капсулярной контрактуры после лучевой терапии, 3) замена эндопротеза справа из-за разрыва импланта.
С помощью имплантов разного объема удалось добиться симметрии молочных желез. Косметический эффект хороший – с хирургической точки зрения и отличный – по мнению пациентки (рис. 10). Пациентка реабилитирована в социальном плане после лечения рака левой молочной железы; в настоящее время данных за рецидив и отдаленное метастазирование не выявлено.
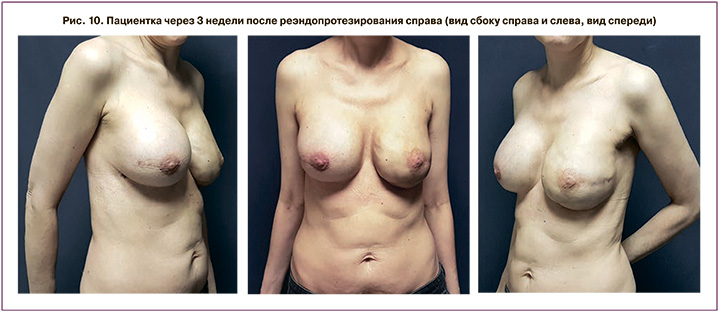
По данным литературы, частота возникновения разрывов силиконовых имплантов варьирует от 10 до 14%. Однако нет стандартизированной системы отчетности для регистрации данного осложнения [4]. В 2017 г. опубликован широкий обзор разрывов имплантов молочных желез (Mentor, Allergan, Silimed), по данным которого частота возникновения разрывов после аугментации варьировала от 1,1 до 11,6%, от 2,8 до 35,4% – после реконструкции молочных желез [5]. К вероятным этиологическим факторам относят травматизацию (прямая травма груди и грудной стенки, использование компрессионной техники при выполнении рентгеновской маммографии), спонтанный разрыв в результате «старения» импланта, повреждение импланта во время операции.
Таким образом, данное клиническое наблюдение является примером, при котором у пациентки на фоне аугментации молочных желез в анамнезе, с одной стороны, диагностирован рак молочной железы; план лечения был комплексным, с включением операции, химиотерапии, лучевой терапии и гормонотерапии. В процессе наблюдения через 1,5 года диагностирована капсулярная контрактура импланта III степени, для лечения которой необходима была замена импланта молочной железы, а в последующем был диагностирован разрыв импланта контралатеральной молочной железы, выполнена замена импланта на имплант.
Заключение
В заключение необходимо отметить необходимость динамического наблюдения женщин с аугментацией молочных желез, выполненной с эстетической точки зрения, прежде всего, для исключения рака молочной железы. При этом комплекс диагностических методов не отличается от пациенток без аугментации и включает УЗИ молочных желез, маммографию. А также после аугментации молочных желез необходимо включать в процесс обследования и использовать для диагностики разрыва импланта МРТ молочных желез; данный метод является ведущим для выявления разрывов импланта. А также МРТ молочных желез дифференцирует экстракапсулярный и интракапсулярный разрыв импланта, и, соответственно, влияет на выбор хирургической тактики, а именно, возможности замены импланта одномоментно или необходимости двухэтапной реконструкции молочной железы.



