Частота заболеваний репродуктивной системы женщин увеличивается ежегодно [1–4]. Наряду с этим продолжают расти и показатели онкологических диагнозов в гинекологической структуре заболеваний. Так, с 2011 г. по 2016 г. в России количество случаев рака матки выросло с 204 764 до 250 527 [3, 5, 6].
Высокие темпы роста патологии матки и эндометрия заставляют искать новые подходы к ранней эффективной диагностике гинекологических заболеваний, которые позволят с минимальными затратами и в короткие сроки точно верифицировать диагноз и начать необходимое лечение [2, 7, 8]. Развитие гиперплазии эндометрия ассоциируют с воздействием различных факторов, которым подвергается женщина в течение всей жизни, однако выделяют наиболее значимые предикторы. Возраст и наличие различных заболеваний, как гинекологических (миома матки), так и экстрагенитальных (ожирение, гипертоническая болезнь), увеличивают риск развития данной патологии. Наличие новообразований яичников сочетается с гиперплазией эндометрия в 19,6% случаев, с эндометриозом – в 15,3% [7]. Перенесенные гиперпластические процессы эндометрия без адекватной терапии рецидивируют в 10,0% случаев.
По мнению некоторых авторов, периоды менопаузального перехода и постменопаузы являются «уязвимыми» возрастными периодами для гиперпластических процессов эндометрия, которые выявляются до 62,5% в структуре гинекологических заболеваний [5, 9, 10]. Женщины с гиперплазией эндометрия в 31,5% случаев имеют эндокринные заболевания (синдром поликистозных яичников, дисфункцию щитовидной железы и гипофиза) [11].
В связи с вышеизложенным, раннее выявление гиперплазии эндометрия на сегодняшний день актуально.
Цель исследования: определить клинико-анамнестические факторы развития гиперплазии эндометрия на основании анализа результатов гистероскопии и морфологии аспиратов.
Материалы и методы
Исследование проводилось на базе ГАУЗ «Кемеровская городская клиническая больница №4», г. Кемерово, одобрено комитетом по этике и доказательности медицинских исследований ФГБОУ ВО КемГМУ МЗ РФ (Приказ МЗ РФ от 19.06.2003 г. № 266), с информированным добровольным согласием женщин.
Дизайн: проспективное когортное исследование (2019–2021 гг.). В исследование включены 900 пациенток в возрасте от 20 до 70 лет, которым произведены гистероскопия и морфологическое исследование аспиратов. Количество женщин было ограничено сроком и критериями невключения в исследование.
Показаниями для гистероскопии явились нарушения менструального цикла невыясненной этиологии, обнаруженный или заподозренный патологический процесс при ультразвуковом исследовании. Диагноз гиперплазии эндометрия устанавливался на основании визуализации полости матки при проведении гистероскопии с последующим взятием аспирата из полости матки путем мануальной вакуумной аспирации и патологоанатомического исследования.
Для классификации гиперплазии эндометрия использовали классификацию Всемирной организации здравоохранения (2014 г., оставленную без изменений в редакции 2020 гг.) [1]. Из 900 пациенток, I группу составили 440 женщин с гистероскопически и морфологически подтвержденной гиперплазией эндометрия; из них у 414/490 (94,1%) была гиперплазия эндометрия без атипии, у 26 (5,9%) – гиперплазия эндометрия с атипией. Во II группу вошли 460 женщин без подтвержденной гиперплазии эндометрия. Результаты патологоанатомического исследования у женщин II группы представлены эндометрием фазы пролиферации в 92,4% случаев, фиброзированной стромой – в 7,6%.
Критерии включения в I (основную) группу: женщины в возрасте от 20 до 70 лет включительно с подтвержденной гиперплазией эндометрия гистероскопически и морфологически.
Критерии включения во II (контрольную) группу: женщины в возрасте от 20 до 70 лет включительно без подтвержденной гиперплазии эндометрия гистероскопически и морфологически.
Критерии невключения в исследование: женщины моложе 20 лет и старше 70 лет, имеющие в настоящее время беременность, острое аномальное маточное кровотечение, наличие диагноза «гиперплазия эндометрия» в течение последних 5 лет, либо состоящие на диспансерном учете с диагнозом «гиперплазия эндометрия», с момента его установления менее 5 лет, синдром поликистозных яичников, дисфункции щитовидной железы и гипофиза, онкологические заболевания любой локализации, принимающие в настоящее время любую гормональную терапию, отказ от участия в исследовании.
Для определения численности групп использовалась формула Лера для относительных величин (определяет размер каждой сравниваемой группы):
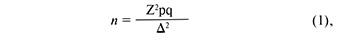
где n – объем выборки; Z – коэффициент, доверительная вероятность = 1,96; p – доля респондентов с наличием исследуемого признака; q=1-p – доля респондентов, у которых исследуемый признак отсутствует; ∆ – предельная ошибка выборки.
При этом доверительная вероятность исследования выбрана 95%, доверительный интервал – 5%. Согласно литературным источникам, распространенность гиперплазии эндометрия среди женского населения составляет от 5,0 до 10,1% [1, 12]. Генеральная совокупность респонденток – прикрепленного к ГАУЗ КГКБ №4 женского населения в возрасте 20–70 лет – составляет 39 850 женщин. Таким образом, требуемый размер выборки составил 140 пациенток. Численность фактически набранных нами пациенток превышала необходимый размер выборки.
Статистический анализ
Статистическая обработка данных проведена с использованием пакета прикладных программ Microsoft Office Excel 2013 (академическая лицензия Open License 62007606) и IBM SPSS Statistiсs Base Campus Edition Campus Value Unit License v. 24 (лицензионный договор № 20160805-1 от 30.08.2016 с ЗАО «Predictive Solutions»).
Проверка на нормальность распределения проводилась с использованием критерия Колмогорова–Смирнова с поправкой Лиллиефорса.
Так как группы имеют распределение, отличное от нормального, для анализа количественных данных в двух независимых выборках использовался критерий Манна–Уитни при уровне значимости p<0,05.
Количественные данные представлены медианой (Ме) и интерквартильным размахом (25-й и 75-й квартили) [Q1; Q3].
Для представления качественных признаков использовали относительные показатели (абс., %). Для оценки качественных параметров в 2 группах пациенток был применен χ2 Пирсона или точный критерий Фишера в зависимости от минимального предполагаемого числа.
Для признаков, имеющих статистически значимые различия, проводились оценка шансов с 95% доверительным интервалом (ОШ 95% ДИ) для каждого фактора (уровень значимости р<0,05), а также определение меры связи между номинальными признаками.
Факторы оценены на взаимодействие и коллинеарность, отобраны наиболее значимые. Отбор из большого количества признаков осуществлялся пошаговым подходом – последовательной оценкой значимости факторов.
Установленные клинико-анамнестические факторы у женщин с гистероскопически и морфологически подтвержденной гиперплазией эндометрия легли в основу раннего выявления данной патологии. При создании компьютерной программы использовали бинарную лoгистическую регрессию.
Для всех факторов гиперплазии эндометрия вычислялись регрессионные коэффициенты. С помощью статистики Вальда определялась значимость выявленных факторов. Вероятность наличия гиперплазии эндометрия рассчитывали по формуле:
p=1/1+е-z (2),
где р – вероятность наличия гиперплазии эндометрия; e – экспонента = 2,852; z – зависимая переменная.
Для вычисления зависимой переменной z использовалась формула:
z=а+ b1x1+ b2x2+ b3x3+…+ bixi (3),
где a – константа; bi – регрессионные коэффициенты; xi – независимые переменные.
Вероятность наличия гиперплазии эндометрия p изменяется в пределах от 0 до 1; вероятность считается низкой при р<0,5 (0–0,4999), высокой, если р≥0,5 (0,5–1,0), в таком случае вероятность наличия патологии сoставляет 99,0%.
Результаты и обсуждение
Проанализированы 18 клинико-анамнестических факторов: возраст женщин, характер менструальной функции, паритет, наличие гинекологических заболеваний, экстрагенитальной патологии, метод контрацепции. Возраст женщин в исследуемых группах представлен в таблице 1.

Женщины с подтвержденной гистероскопически и морфологически гиперплазией эндометрия были старше в сравнении с женщинами без подтвержденной гиперплазии эндометрия.
Распределение женщин по возрасту представлено в таблице 2. Расчеты получены с помощью χ2 Пирсона.
Подтверждение гиперплазии эндометрия при патологоанатомическом исследовании чаще было у женщин в возрасте 45–49 лет (ОШ=1,176 (95% ДИ 0,994; 1,392)) и 60–70 лет (OШ=1,432 (95% ДИ 1,227; 1,672)). Возраст женщин 25–39 лет явился фактором, снижающим вероятность гиперплазии эндометрия; при этом, чем моложе женщина, тем меньше риски развития данной патологии: 25–29 лет (OШ=0,615 (95% ДИ 0,431; 0,875)), 30–34 лет (OШ=0,662 (95% ДИ 0,511; 0,856)), 35–39 лет (OШ=0,772 (95% ДИ 0,620; 0,952)). Женщинам в постменопаузе в 2 раза чаще устанавливали диагноз «гиперплазия эндометрия» – 70% против 35% (OШ=1,432 (95% ДИ 1,227; 1,672)).
Характеристика менструального цикла пациенток на время включения в исследование отражена в таблице 3. Расчеты получены с помощью точного критерия Фишера.
Длительные менструации чаще встречались у женщин I группы – 27,0% против 12,3% женщин II группы (OШ=1,292 (95% ДИ 0,163; 1,443)).
У женщин I группы чаще наблюдались нарушения менструального цикла: обильные, частые и нерегулярные менструации (17,9%), олиго/аменорея (9,0%); в то время как у женщин во II группе – в 7,7 и 3,3% случаев соответственно (OШ=1,219 (95% ДИ 1,037; 1,433)), OШ=1,555 (95% ДИ 1,302; 1,855)).
Паритет, гинекологические и экстрагенитальные заболевания, метод контрацепции представлены в таблице 4. Для расчетов был применен χ2 Пирсона.

Медицинские (хирургические) аборты (OШ=2,358 (95% ДИ 1,882; 2,955)), диагностические выскабливания (OШ=2,358 (95% ДИ 1,882; 2,955)) и отсутствие родов в анамнезе также чаще наблюдались у женщин с гиперплазией эндометрия (OШ=0,482 (95% ДИ 0,334; 0,705)).
Отсутствие беременности снижало риск гиперплазии эндометрия (OШ=0,704 (95% ДИ 0,557; 0,890)). Вероятно, это связано с меньшим количеством женщин в возрасте до 34 лет, имеющих гиперплазию эндометрия, в основной группе по сравнению с контрольной (67 против 139) и сложившимися установками на сегодняшний день по реализации репродуктивной функции в более позднем возрасте.
У женщин I группы чаще диагностировались гинекологические заболевания, такие как доброкачественные новообразования яичников (OШ=1,369 (95% ДИ 1,123; 1,656)), лейомиома матки (OШ=1,371 (95% ДИ 1,198; 1,569)), аденомиоз (OШ=6,0 (95% ДИ 2,052; 17,562)), бесплодие (OШ=6,271 (95% ДИ 3,623; 10,873)). У женщин I группы в сравнении с женщинами II группы в 2 раза чаще встречалась ранее перенесенная гиперплазия эндометрия (OШ=5,446 (95% ДИ 4,007; 7,402)), несмотря на то, что при лечении гиперпластического процесса проводилась гормональная терапия согласно клиническим рекомендациям [1].
Женщины I группы чаще имели экстрагенитальную патологию. Среди экстрагенитальных заболеваний преобладали гипертоническая болезнь (OШ=1,752 (95% ДИ 1,242; 2,481)), ожирение (OШ=2,123 (95% ДИ 1,402; 3,153)), сахарный диабет 2 типа (OШ=3,063 (95% ДИ 1,603; 5,862)). Диффузная кистозная мастопатия у женщин I группы встречалась в 2,5 раза чаще в сравнении с женщинами контрольной группы (OШ=3,022 (95% ДИ 1,861; 4,894)).
Женщины основной группы реже использовали в качестве метода контрацепции комбинированные оральные контрацептивы – в 3,6% случаев против 9,1% (OШ=0,382 (95% ДИ 0,212; 0,681)), отдавая предпочтение барьерным методам (презервативам и прерванному половому акту).
В результате анализа клинико-анамнестических факторов выявлены статистически значимые предикторы. Модифицируемыми факторам риска гиперплазии эндометрия являются длительность (более 8 дней), характер (обильность, регулярность) менструации, отсутствие родов, наличие медицинских (хирургических) абортов, диагностических выскабливаний; такие гинекологические заболевания, как лейомиома матки, доброкачественные новообразования яичников, гиперплазия эндометрия в анамнезе, аденомиоз, бесплодие; экстрагенитальные заболевания – гипертоническая болезнь, сахарный диабет 2 типа, ожирение, диффузная кистозная мастопатия. Немодифицируемым фактором является возраст женщины на момент постановки диагноза. Однако женщины до 39 лет, принимающие комбинированные оральные контрацептивы, имеют меньший риск развития гиперплазии эндометрия.
На основании полученной информации была разработана компьютерная программа с использованием метода логистической регрессии для выделения группы риска наличия гиперплазии эндометрия. Значимость вышеописанных предикторов ранжировалась с помощью статистики Вальда и показала следующие результаты: наиболее значимым является возраст, затем ожирение, наличие аденомиоза, гиперплазии эндометрия в анамнезе, длительность менструации, соматических заболеваний – сахарного диабета 2 типа, гипертонической болезни, прием комбинированных оральных контрацептивов, диффузная кистозная мастопатия. Все коэффициенты значимы по критерию Вальда и оказывают влияние на возникновение гиперплазии эндометрия (табл. 5).
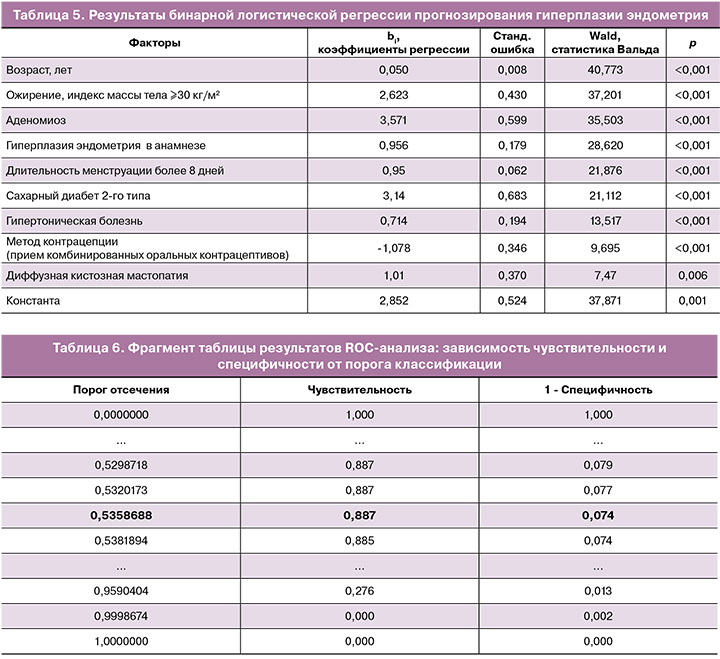
Исходя из значений регрессионных коэффициентов, все предикторы имеют прямую связь с вероятностью наличия гиперплазии эндометрия.
Вероятность наличия гиперплазии эндометрия определялась по формулам (2) и (3) с помощью рассчитанных регрессионных коэффициентов. Используя полученные константы и коэффициенты регрессии bi из таблицы и формулы (2) и (3), получили уравнение:
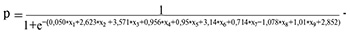
Подставляя в уравнение значение хi (независимые переменные), получаем вероятность наличия гиперплазии эндометрия (зависимая переменная): Возраст – х1 (лет); Ожирение – х2 (0 – отсутствует, 1 – имеется); Аденомиоз – х3 (0 – отсутствует, 1 – имеется); Гиперплазия эндометрия в анамнезе – х4 (0 – отсутствует, 1 – имеется); Длительность менструации более 8 дней – х5 (дней); Сахарный диабет 2-го типа – х6 (0 – отсутствует, 1 – имеется); Гипертоническая болезнь – х7 (0 – отсутствует, 1 – имеется); Метод контрацепции (прием комбинированных оральных контрацептивов) – х8 (0 – отсутствует, 1 – имеется); Диффузная кистозная мастопатия – х9 (0 – отсутствует, 1 – имеется).
С помощью метода ROC-анализа и построения ROС-кривой оценено качество созданной модели. Процент правильной классификации модели общего неблагоприятного исхода (наличия гиперплазии эндометрия) составил 96,4%, AUC=0,964, p<0,001 (рисунок).

Общий оптимальный порог отсечения в созданной модели при проведении ROС-анализа составил р>0,535 (табл. 6).
Процент верной переклассификации (точности модели) составил 91,1%, чувствительность – 88,7%, специфичность – 92,6%. Приведенные показатели демонстрируют высокую валидность модели.
Использование данной диагностической модели подразумевает внесение данных о женщине в компьютерную программу для последующего расчета наличия гиперплазии эндометрия. Компьютерная программа «Клинико-анамнестические факторы ранней диагностики гиперплазии эндометрия» подана на регистрацию в Федеральную службу по интеллектуальной собственности (Москва).
Планируется тестирование разработанной модели на независимой выборке.
Данная модель не может быть использована для женщин младше 20 лет и старше 70 лет с наличием синдрома поликистозных яичников, дисфункцией щитовидной железы и гипофиза, онкологических заболеваний, принимающих в настоящее время гормональные препараты, беременных.
Обсуждение
Несмотря на широкий спектр диагностических процедур, выявление гиперплазии эндометрия на ранних стадиях остается не всегда возможным. Чаще специалисты не проводят ультразвуковое исследование органов малого таза на первичном амбулаторном приеме, либо женщины в ряде случаев не предъявляют жалоб, принимая нарушение менструального цикла за норму. В связи с этим увеличивается период до установления диагноза гиперплазии эндометрия с момента ее возникновения. Медицинскими обществами разрабатываются простые и в то же время эффективные диагностические методы для выявления заболеваний, в том числе и гиперплазии эндометрия. Исследование, проведенное нами, включило комплексную оценку значительного количества клинико-анамнестических факторов риска развития гиперплазии эндометрия, среди которых есть как модифицируемые, так и немодифицируемые. Некоторые установленные предикторы гиперплазии эндометрия подтверждаются данными и других авторов [1, 13, 14]. Однако комплексная оценка предикторов не проводилась и не позволяла оценить воздействие факторов в совокупности на развитие гиперплазии эндометрия. Полученные данные легли в основу разработки компьютерной программы «Клинико-анамнестические факторы ранней диагностики гиперплазии эндометрия», которая позволит специалистам первичного звена выявлять группу риска развития гиперплазии эндометрия среди женского населения без применения инструментальных диагностических методик.
Заключение
Таким образом, программа, основанная на определении клинико-анамнестических факторов, может быть рекомендована к применению для раннего выделения группы риска женщин от 20 до 70 лет с гиперплазией эндометрия, дифференцированного подхода к их наблюдению и своевременного проведения профилактических и лечебных мер.



