Преиндукция родов (ПР) – мероприятия, направленные на созревание шейки матки при отсутствии или недостаточной ее готовности к родам. Индукция родов (ИР) – индуцирование родовой деятельности при достижении зрелости шейки матки с целью родоразрешения через естественные родовые пути [1].
Частота ИР в мире имеет тенденцию к увеличению за последние годы и на 2019 г. в США составляет 29,4% [2], в Европе – от 6,8 до 33% [3].
Несмотря на широкую распространенность данной процедуры, все еще остается большое количество вопросов, по которым нет согласия в научной литературе. Cовременное мировое научное сообщество не может дать однозначного определения успешной и неудачной ИР.
Так, говоря о понятии неуспеха ИР, одни авторы берут за критерий продолжительность латентной фазы родов, используя интервал 15 ч в качестве порогового значения [4]. В других исследованиях было высказано мнение, что достижение активной фазы родов следует рассматривать как меру успешной ИР [5].
Согласно Lin M.G. et al., неудачная индукция определяется невозможностью достичь открытия шейки матки >4 см в течение 12–18 ч от начала введения окситоцина после вскрытия плодного пузыря [6]. Тем не менее большинство авторов считают уместным рассматривать непосредственно результат, а не процесс, и предлагают считать родоразрешение через естественные родовые пути в качестве основного исхода успешной ИР [7, 8].
Spong C.Y. et al. в своей публикации обозначают неудачную ИР в виде отсутствия достижения регулярной родовой деятельности (схватки каждые 3 минуты) и изменений по шейке матки после 24 ч от введения окситоцина [9].
Известным фактором успешной ПР является изначальная готовность родовых путей, которую обычно оценивают по шкале Бишоп [10, 11]. Компоненты шкалы Бишоп отражают физиологические изменения, происходящие в шейке матки незадолго до родовой деятельности. Шейка матки, состоящая из волокнистой соединительной ткани, во время беременности подвергается интенсивному ремоделированию, что обеспечивает большую эластичность перед родами. Множество факторов, в том числе матриксные металлопротеиназы, гиалуроновая кислота, простагландины и механическое давление со стороны предлежащей части плода, увеличивают содержание воды, снижают концентрацию коллагена и реструктурируют коллаген и внеклеточный матрикс, обеспечивая размягчение, сглаживание и расширение шейки матки [12].
Сильным предиктором успешной ПР является паритет родов. Feghali M. et al. в своем исследовании показали, что у повторнородящих беременных женщин с индукцией родов выше частота родоразрешений через естественные родовые пути по сравнению с первородящими [13, 14]. Не менее значимым является индекс массы тела (ИМТ) беременной, коррелирующий с успехом преиндукции. Известно, что ожирение снижает эффективность преиндукции, а также увеличивает продолжительность родов [14]. Многочисленные ретроспективные исследования постоянно показывают, что частота кесарева сечения у женщин с ожирением после ИР составляет 40% [15].
Трансвагинальное ультразвуковое измерение длины шейки матки перед индукцией широко изучалось в прогнозировании успешной преиндукции. Pandis G.K. et al. в своем исследовании сообщили, что данный метод является полезным предиктором влагалищных родов в течение 24 ч после инициации преиндукции [16]. В литературе описаны исследования, указывающие на преимущество ультразвукового исследования длины шейки матки над шкалой Бишоп в прогнозировании успеха ПР [17–20].
В дополнение к трансвагинальному измерению длины шейки матки была предложена эластография для количественной оценки эластичных свойств или мягкости шейки матки при прогнозировании исхода родов [21, 22].
В нескольких исследованиях (Lockwood C.J. et al. [23], Garite T.J. et al. [24], Crane J.M.G. et al. [25]) оценивали роль фетального фибронектина в прогнозировании успеха ИР и получили противоречивые результаты. Фетальный фибронектин представляет собой гликопротеин, обнаруживаемый во внеклеточном матриксе, окружающем вневорсинчатый трофобласт. Предполагается, что обнаружение фетального фибронектина во влагалище перед родами обусловлено изменениями плодных оболочек в нижнем сегменте матки, происходящими одновременно с процессами ремоделирования шейки матки до начала родовой деятельности. Нарушение хориодецидуального слоя приводит к утечке фетального фибронектина через шейку матки во влагалище. Следовательно, обнаружение этого белка в цервиковагинальных выделениях связано с близостью начала родов.
Kiss H. et al. в своем исследовании пришли к выводу о том, что определение фетального фибронектина является маркером изменений в шейке матки и плодных оболочек, поэтому может использоваться в качестве предиктора успеха ИР [26]. Такие же результаты получили Garite T.J. et al. [24] и Adedeji M.O. et al. (2023) [27], которые сообщают, что обнаружение фетального фибронектина во влагалище предсказывает успешную индукцию родов, независимо от оценки степени зрелости шейки матки по шкале Бишоп. Тем не менее ряд авторов (Sciscione A. et al. [28], Droulez A. et al. [29], Ojutiku D. et al. [30] и Roman A.S. et al. [31]) получили противоположные результаты, не обнаружив прогностической ценности в определении фетального фибронектина.
Фосфорилированный белок, связывающий инсулиноподобный фактор роста-1 (phIGFBP-1), синтезируется в децидуальной оболочке. Высокий уровень этого белка в цервико-вагинальной жидкости связан с созреванием шейки матки и повышенным риском преждевременных родов, поэтому постулируется, что phIGFBP-1 может также помочь в прогнозировании успешной ИР [32], что и показали результаты исследований, проведенных Riboni F. et al. (2012) [33] и Rathore A. et al. (2021) [34].
Гликопротеин активин А регулирует такие биологические функции, как клеточная дифференцировка, пролиферация, ремоделирование и морфогенез. Функция активина А заключается в стимуляции высвобождения простагландинов и интерлейкина-6 из клеток амниона, что подтверждает его роль в родовой деятельности [35]. Funghi L. et al. оценивали уровень активина А в материнской сыворотке и экспрессию плацентарной мРНК у 64 женщин со спонтанным началом родов и индуцированными родами. Ими было обнаружено, что активин А материнской сыворотки при пороговом значении >4643 нг/мл может прогнозировать успешную ИР с площадью под ROC-кривой 0,858 (95%, ДИ 0,714–0,947) [36]. Özdemir B.G. et al., опираясь на исследование, выявившее корреляцию между объемом надпочечников плода и преждевременными родами, предположили, что данный метод сможет стать одним из предикторов успеха ИР, что и подтвердили в своем исследовании. Авторы показали, что в группе успешной ИР объем надпочечников был значимо выше по сравнению с группой неуспешной индукции [37].
Кроме вышеизложенных факторов, помогающих предсказать успех преиндукции, имеется такой фактор, как время. Известно, что у женщин, подвергающихся ИР, процесс созревания родовых путей и установления регулярной родовой деятельности может занять больше времени, особенно если индукция начинается с незрелой шейки матки, чем у женщин, роды которых начались самопроизвольно. Исходя из этого, необходимо учитывать, что предоставляя большее время и располагая большим терпением в отношении подготовки женщины к родоразрешению, мы повышаем шансы на успешную ПР [14].
Исследования по предикторам успешной ПР основаны на использовании разных методов, потому они часто несопоставимы. Недостатками имеющихся предикторов являются противоречивость данных, низкая прогностическая ценность, необходимость привлечения смежных специалистов; поэтому по-прежнему существует потребность в разработке новых инструментов прогнозирования для облегчения принятия обоснованных решений, оптимизации ресурсов и минимизации потенциальных рисков неудачи.
В России широко распространена преиндукция мифепристоном, но относительно него нет научных работ, в которых изучались бы предикторы успеха преиндукции.
В связи с изложенным целью исследования явилось определить предикторы успеха ПР/ИР при использовании мифепристона.
Материалы и методы
Нами проведено ретроспективное исследование в ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России. Было проанализировано 5000 электронных историй родов с 2016 по 2023 гг.
Критериями включения являлись: возраст женщин от 18 до 45 лет, одноплодная беременность, головное предлежание, доношенный срок беременности, «незрелые» родовые пути, ПР/ИР с использованием мифепристона.
Критерии невключения: многоплодная беременность, наличие тяжелых экстрагенитальных заболеваний и осложнений беременности (преэклампсия, HELLP-синдром, антифосфолипидный синдром), пороки развития плода, плановое кесарево сечение, самопроизвольное начало родовой деятельности.
Из общего количества проанализированных историй родов в исследование были включены 236, впоследствии разделенные на 2 группы: 1-я группа – беременные женщины, «ответившие» на ПР достижением полной зрелости шейки матки (оценка по шкале Бишоп 8 и более баллов) или развитием регулярной родовой деятельности в течение первых 24 ч после однократной дозы мифепристона 200 мг per os (n=116); 2-я группа – беременные женщины, которым потребовалось продолжение подготовки к родоразрешению с использованием второй дозы мифепристона и/или применением дополнительных методов ПР (n=120).
С целью определения предикторов успеха изучали особенности наступления и течения беременности (токсикоз, угроза прерывания беременности и преждевременных родов, бессимптомная бактериурия, анемия, гестационная тромбоцитопения, отеки беременных, ОРВИ, новая коронавирусная инфекция (SARS-CoV-2), многоводие, маловодие, курение во время беременности, внутрипеченочный холестаз, гестационная артериальная гипертензия, гестационный сахарный диабет), антропометрические данные пациенток (рост, вес, ИМТ), прием лекарственных препаратов (дидрогестерон, микронизированный прогестерон, низкомолекулярные гепарины, ацетилсалициловая кислота), зрелость родовых путей по шкале Бишоп, течение родов и послеродового периода (продолжительность родов, метод родоразрешения, кровотечение), а также исходы для новорожденных (оценка по шкале Апгар, масса, длина и окружность головы новорожденного).
Все пациентки перед ПР были обследованы. Показаниями к преиндукции послужили: анатомически узкий таз (n=69), тенденция к перенашиванию беременности (n=80), гестационный сахарный диабет (ГСД) (n=36), хроническая артериальная гипертензия (ХАГ) (n=5), гестационная артериальная гипертензия (ГАГ) (n=10), маловодие (n=5), тенденция к рождению крупного плода (n=27), крупный плод (n=25), маловесный плод к сроку гестации (n=3), внутрипеченочный холестаз беременных (n=2). В ряде наблюдений у одной и той же пациентки на момент ПР имелось более 1 показания.
Преиндукцию и последующую ИР проводили согласно клиническим рекомендациям [1].
Подготовку родовых путей к родам начинали при «незрелой» шейке матки (от 0 до 5 баллов по шкале Бишоп); родовозбуждение проводили при достижении «зрелых» родовых путей (от 8 баллов и выше по шкале Бишоп).
Преиндукцию при «незрелой» шейке матки начинали с приема одной таблетки мифепристона 200 мг. В случае «ответа» на первую таблетку в виде достижения степени зрелости родовых путей 8 баллов и выше по шкале Бишоп либо появления регулярной родовой деятельности данную категорию женщин относили к 1-й группе. В случае необходимости дальнейшей ПР с целью достижения «зрелых» родовых путей использовали дополнительные методы преиндукции, которые в зависимости от клинической ситуации включали прием второй таблетки мифепристона 200 мг, интрацервикальную установку баллонного расширителя, применение гигроскопических расширителей Dilapan S, интрацервикальное введение динопростона 0,5 мг. С целью родовозбуждения проводили амниотомию. На все методы и этапы ПР/ИР было получено информированное добровольное согласие в письменном виде.
В качестве первичного изучаемого исхода было определено достижение полной зрелости шейки матки (8 баллов по шкале Бишоп) и начало родовой деятельности в течение 24 ч от приема мифепристона. В качестве вторичного изучаемого исхода были определены: процент операции кесарева сечения, влагалищных родоразрешающих операций в исследуемых группах и перинатальные исходы.
Проведение исследования одобрено локальным этическим комитетом ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России.
Статистический анализ
Статистический анализ проводили с использованием программы StatTech v. 3.1.4 (ООО «Статтех», Россия).
Количественные показатели оценивались на предмет соответствия нормальному распределению с помощью критерия Шапиро–Уилка (при числе исследуемых менее 50) или критерия Колмогорова–Смирнова (при числе исследуемых более 50). Количественные показатели, имеющие нормальное распределение, описывались с помощью средних арифметических величин (M) и стандартных отклонений (SD), границ 95% доверительного интервала (95% ДИ). В случае отсутствия нормального распределения количественные данные описывались с помощью медианы (Me) и нижнего и верхнего квартилей (Q1–Q3). Категориальные данные описывались с указанием абсолютных значений и процентных долей. Сравнение двух групп по количественному показателю, имеющему нормальное распределение, при условии равенства дисперсий выполнялось с помощью t-критерия Стьюдента, при неравных дисперсиях выполнялось с помощью t-критерия Уэлча. Сравнение двух групп по количественному показателю, распределение которого отличалось от нормального, выполнялось с помощью U-критерия Манна–Уитни.
Сравнение процентных долей при анализе четырехпольных таблиц сопряженности выполнялось с помощью критерия хи-квадрат (χ2) Пирсона (при значениях ожидаемого явления более 10), точного критерия Фишера (при значениях ожидаемого явления менее 10). Сравнение процентных долей при анализе многопольных таблиц сопряженности выполнялось с помощью критерия хи-квадрат Пирсона.
Построение прогностической модели вероятности определенного исхода выполнялось при помощи метода логистической регрессии. Мерой определенности, указывающей на ту часть дисперсии, которая может быть объяснена с помощью логистической регрессии, служил коэфициент R2 Найджелкерка.
Для оценки диагностической значимости количественных признаков при прогнозировании определенного исхода применялся метод анализа ROC-кривых. Разделяющее значение количественного признака в точке cut-off определялось по наивысшему значению индекса Юдена.
Результаты
Сравнение двух групп показало их сопоставимость по возрасту – 31 (5,1) год в обеих группах (р=0,32), весу – 73,0 (64,0; 79,0) кг против 73,0 (65,8; 81,0) кг (р=0,39) и росту – 167 (163; 170) см против 168 (161; 170) см (р=0,46). Значения медиан ИМТ также не имели различий в двух группах: 26 (23; 29) кг/м2 и 26 (24; 28) кг/м2 (р=0,42). Имелись статистически значимые различия по паритету родов: медиана 1-й группы составила 0 (0; 1) и 2-й – 0 (0; 0) (р=0,029).
Было произведено сравнение обеих групп по отягощенному соматическому (ХАГ, ожирение, субклинический гипотиреоз, заболевания желудочно-кишечного тракта и мочеполовой системы) и гинекологическому анамнезу (наличие в анамнезе выкидышей, неразвивающихся беременностей, бесплодия), которое не выявило статистически значимых отличий. Наличие в анамнезе аборта показало значимые различия между двумя сравниваемыми группами: 14/116 (12,1%) против 5/120 (4,2%) (р=0,031; 95% ДИ 1,099–9,070) (табл. 1).
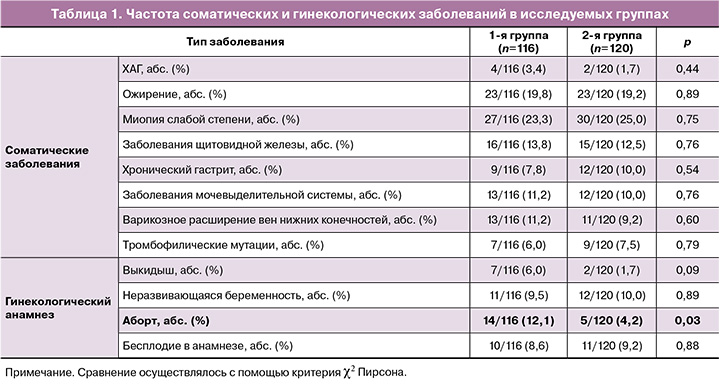
В течение настоящей беременности имелись особенности, обращающие на себя внимание статистически значимыми отличиями групп, а именно: по перенесенным ОРВИ: в 1-й группе 24/116 (20,7%) и 43/120 (35,8%) во 2-й группе (р=0,010) (ОШ=0,467; 95% ДИ 0,261–0,838); перенесенной новой коронавирусной инфекции: 16/116 (13,8%) против 7/120 (5,8%) (р=0,039; 95% ДИ 1,021–6,534); приему дидрогестерона: 10/116 (8,6%) в 1-й группе и 24/120 (20,0%) во 2-й группе (р=0,013; ОШ=0,377; 95% ДИ 0,172–0,830); а также наличию многоводия в III триместре беременности: 17/116 (14,7%) против 6/120 (5,0%) (р=0,012; 95% ДИ 1,238–8,597) (табл. 2).
Говоря о сравнении двух групп касательно показаний к ПР, мы не обнаружили в них различий: тенденция к перенашиванию беременности в 1-й группе – 42/116 (35%), во 2-й группе – 38/120 (32,8%); анатомически узкий таз – 36/116 (30,0%) против 33/120 (28,4%); ГСД – 18/116 (15,0%) против 18/120 (15,5%); ХАГ – 2/116 (1,7%) против 3/120 (2,6%); ГАГ – в 1-й группе 4/116 (3,3%), во 2-й – 6/120 (5,2%); маловодие – 1/116 (0,8%) против 4/120 (3,4%); тенденция к рождению крупного плода – 16/116 (13,3%) в 1-й группе, 11/120 (9,5%) во 2-й; крупный плод – 16/116 (13,3%) против 9/120 (7,8%); маловесный к сроку гестации – 2/116 (1,7%) против 1/120 (0,9%); внутрипеченочный холестаз беременных – 2/116 (1,7%) против 0/120 (0%) (р>0,05).
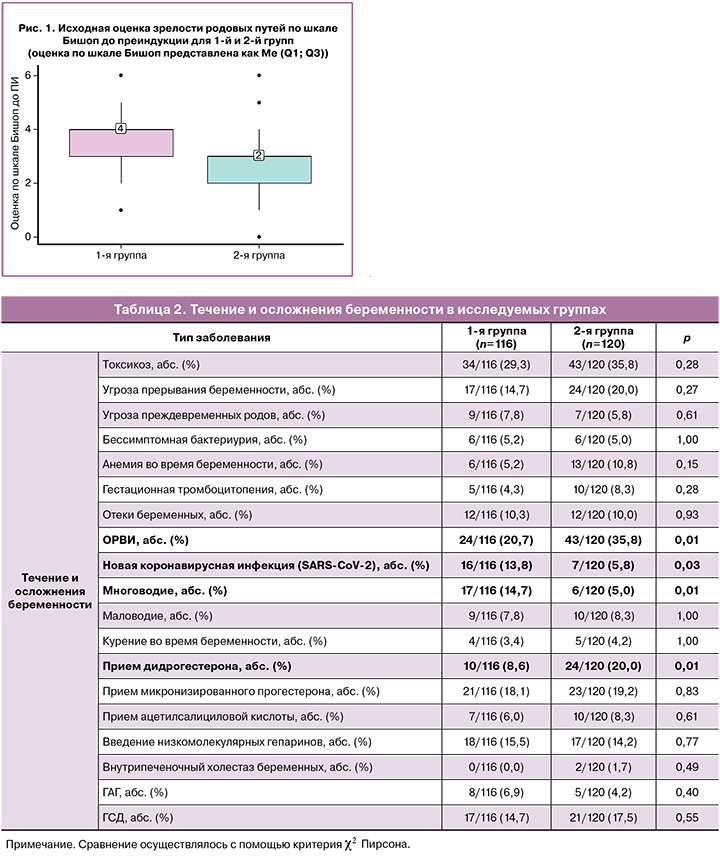
Срок инициации ПР в обеих группах был сопоставим, медиана составила 280 дней (275; 284), что соответствует 40 неделям (39,2; 40,4). Медиана срока завершения ПР – 281 день (276; 285) – 40 недель 1 день (39,3; 40,5) для 1-й группы, 282 дня (277; 286) – 40 недель 2 дня (39,4; 40,6) для 2-й. Оценка по шкале Бишоп перед началом преиндукции в 1-й группе составила 4 (3; 4), во 2-й – 3 (2; 3), что явилось статистически значимым (р<0,001) (рис. 1).
Значимые различия были выявлены в количестве дней от начала до завершения ПР: медиана в 1-й группе «ответивших» на 1 таблетку мифепристона составила 2 (2; 2), во 2-й группе – 3 (2; 3), р<0,001.
Данные, полученные о методе родоразрешения, показали, что частота родов через естественные родовые пути составила 103/116 (88,8%) в 1-й группе, 99/120 (82,5%) во 2-й группе, что не являлось статистически значимым (р=0,169). При этом отличий в продолжительности родов между двумя группами выявлено не было: медиана в 1-й группе составила 6 ч 25 мин (5,25; 7,43) против 6 ч 55 мин (5,78; 8,30) во 2-й (р=0,158). Обе группы были сопоставимы по осложнениям родов; частота кровотечений в обеих группах составила 1/116 (0,9%) и 1/120 (0,8%), р=1,00. Обращают на себя внимание статистически значимые различия групп по произведенной эпизиотомии в связи с угрозой разрыва промежности: в 1-й группе 20/116 (17,2%), во 2-й – 43/120 (35,8%), р=0,001. Отличий по послеродовой кровопотере в исследуемых группах также выявлено не было – 250 (170; 300) мл и 250 (200; 312) мл, р=0,30.
Частота родоразрешения путем операции кесарева сечения не отличалась в исследуемых группах и составила 13/116 (11,2 %) в 1-й группе и 21/120 (17,5 %) во 2-й группе. Показания к кесареву сечения в большинстве наблюдений были сопоставимы, кроме случаев клинически узкого таза, которые составили 3/116 (2,6%) и 13 (10,8%) соответственно (р=0,01).
Частота оперативных влагалищных родоразрешений путем вакуум-экстракции плода между двумя исследуемыми группами также не показала значимых различий – 4/116 (3,4%) против 4/120 (3,3%) соответственно, р=1,00.
Во всех наблюдениях родились живые доношенные дети с медианой оценки по шкале Апгар 8 (8; 8) баллов на 1-й минуте (р=0,87) и 9 (9; 9) баллов на 5-й минуте (р=0,11) в обеих группах.
Масса тела новорожденных различалась и составила 3490 (422) (95% ДИ 3412–3567) г в 1-й группе и 3596 (375) (95% ДИ 3528–3663) г во 2-й группе, р=0,04. Параметры длины и окружности головы новорожденных обеих групп не имели отличий. Также не было различий по полу новорожденных.
Была разработана прогностическая модель для определения вероятности успешной ПР в зависимости от показателей: «Паритет родов», «Многоводие» и «Оценка по шкале Бишоп до начала преиндукции» методом бинарной логистической регрессии.
В регрессионный анализ в качестве зависимой переменной (переменной отклика) включался признак – беременные, кто ответил/не ответил на ПР/ИР. В качестве независимых (предикторных) были включены значимые переменные: «Паритет родов» (значения 0, 1, 2), «Многоводие» (значения 0, 1), «Оценка по шкале Бишоп до начала преиндукции» (значения 1, 2, 3, 4).
Одномерный анализ (логистическая регрессия) проведен 3 раза для каждой из переменных. Использована функция glm языка программирования R. Параметр «Паритет родов» показал значимость p-value<0,03. Параметр «Многоводие», показал значимость на уровне p-value=0,017. Параметр «Оценка по шкале Бишоп до начала преиндукции» показал высокую значимость на уровне p-value=0,001.
Независимые переменные были проверены на коллинеарность, что представлено в таблице 3. Коэффициент корреляции независимых переменных не превышал 0,17, и они были включены в регрессионную модель.
Процесс отбора признаков в соответствии с их значимостью (вкладом в модель) проводился путем пошагового включения.
Число наблюдений составило 236. Наблюдаемая зависимость, использование которой возможно с целью прогнозирования успешного ответа на ПР мифепристоном, описывается уравнением:
P=1/(1+e-z)×100%,
z =-3,776+0,561Xпаритет родов+1,514Xмноговодие+
+0,889Xоценка по шкале Бишоп до преиндукции,
где P – вероятность успеха ПР, Xпаритет родов – N данных родов по счету, Xмноговодие – многоводие (0 – нормальное количество вод, 1 – многоводие), Xоценка по шкале Бишоп до преиндукции – оценка по шкале Бишоп до ПР.
Полученная регрессионная модель является статистически значимой (p<0,001).

При множественном регрессионном анализе были использованы четыре независимых переменных, описанных выше. Коэффициенты регрессии и значение p для каждой переменной приведены в таблице 4.
Для проверки возможности нулевых значений коэффициентов по критерию Вальда была использована функция wald.test библиотеки aod (язык R). Для переменных «Паритет родов»+«Многоводие» Chi-squared test: χ2=6,6, df=2, P(>χ2)=0,036. Для переменных «Оценка по шкале Бишоп до преиндукции» Chi-squared test: χ2=33,9, df=2, P(>χ2)=0,004 Так как p-значение меньше 0,05, можно отклонить нулевую гипотезу теста Вальда.
При увеличении показателя «Паритет родов» на 1 шансы успеха преиндукции увеличивались в 1,57 раза. При оценке показателя «Многоводие» шансы успешной преиндукции увеличивались в 4,22 раза. При увеличении показателя оценки по шкале Бишоп до преиндукции на 1 шансы успешной преиндукции увеличивались в 2,16 раза (табл. 4).
При оценке зависимости вероятности успешной ПР от значения логистической функции P с помощью ROC-анализа была получена кривая, представленная на рисунке 2.
Площадь под ROC-кривой составила 0,771±0,032 с 95% ДИ 0,708–0,833. Полученная модель была статистически значимой (р<0,001).
Пороговое значение логистической функции P в точке cut-off, которому соответствовало наивысшее значение индекса Юдена, составило 0,561. «Ответ» на 1 таблетку мифепристона (1-я группа) прогнозировался при значении логистической функции P выше данной величины или равном ей. Чувствительность и специфичность модели составили 64,2 и 75,8% соответственно.
Прогностическая ценность положительного результата составила 72,6, прогностическая ценность отрицательного результата – 67,9.
Обсуждение
В данном исследовании были изучены возможные предикторы, способствующие успешной ПР, а также сокращающие интервал времени для подготовки к родоразрешению. За основу успеха ПР в нашем исследовании мы брали одну из двух отправных точек: достижение «зрелых» родовых путей по шкале Бишоп (8 баллов и выше) либо возникновение регулярной родовой деятельности в течение/через 24 ч от приема первой таблетки мифепристона 200 мг.
Зрелость шейки матки является известным предиктором успеха/неуспеха ИР [38, 39]. Однако в настоящее время в доступной нам литературе мы не обнаружили исследований, в которых определено значение индекса Бишоп, при котором ожидается быстрый ответ на преиндукцию мифепристоном. Проведенное нами исследование показало, что таким значением является 4 балла.
Нами была выявлена взаимосвязь между паритетом родов и успешной преиндукцией: у повторнородящих женщин успех преиндукции значимо выше. Эти данные подтверждаются в ряде исследований [40, 41].
Труднообъяснимой находкой нашего исследования является факт связи аборта в анамнезе и успеха преиндукции. Тогда как связи между эффективностью преиндукции и неразвивающейся или внематочной беременностью не было выявлено.
Также дискуссионным является факт корреляции между перенесенными во время беременности ОРВИ, а также новой коронавирусной инфекции и ответом на преиндукцию родов. Учитывая отсутствие подробных данных о возбудителях, продолжительности и тяжести течения ОРВИ у беременных женщин, вошедших в исследование, дать убедительное пояснение корреляции между перенесенными ОРВИ и более длительной ПР, а также более высокой частотой применения дополнительных методов подготовки шейки матки не представляется возможным.
Полученные результаты показали, что перенесенная новая коронавирусная инфекция во время беременности сочеталась со скорым ответом на преиндукцию после однократного применения мифепристона. Можно предположить, что SARS-CoV-2, инициируя воспалительный каскад в организме матери, способствует выработке цитокинов, что приводит к активации миометрия, с одной стороны, и снижению уровня прогестерона, с другой, тем самым инициируя родовую деятельность [42, 43].
Нами было выявлено отсутствие зависимости между применением микронизированного натурального прогестерона на ранних сроках беременности с целью профилактики и лечения угрожающего выкидыша и более сложной и долгой схемой ПР; тогда как женщины, получавшие дидрогестерон на тех же сроках беременности, показали обратное. То есть в группе женщин, которым проведено лечение дидрогестероном на раннем сроке беременности, эффективность ПР была ниже. Этот факт также требует дальнейшего изучения.
Мы обнаружили заметную разницу между 1-й и 2-й группами в отношении ПР в зависимости от наличия у пациентки многоводия. Так, развитие регулярной родовой деятельности или достижение пациентками зрелости родовых путей в течение суток от начала преиндукции чаще имело место в группе беременных с многоводием. Вероятнее всего, этот механизм связан с механическим растяжением миометрия, являющимся стимулом к началу родовой деятельности посредством выработки моноцитарного хемотаксического протеина-1 (МСР-1) [44, 45].
В нашем исследовании были обнаружены отличия в необходимости проведения эпидуральной аналгезии с целью обезболивания родов между двумя группами: пациенткам 2-й группы (с более длинной и многокомпонентной ПР) статистически значимо чаще требовалось обезболивание. Данный факт можно объяснить изначально меньшей готовностью организма в целом к началу родовой деятельности, а также более длительным пребыванием беременной в стационаре и проведением нескольких этапов ПР, что отражается на психоэмоциональном состоянии беременной женщины. Данные, полученные нами, совпадают с результатами исследования Воскресенский С.Л и соавт. [46].
Выявленная в работе более высокая частота эпизиотомии в связи с угрозой разрыва промежности во 2-й группе коррелирует с меньшей оценкой по шкале Бишоп в этой группе. Вероятно, это подтверждает меньшую степень готовности организма к родам, что выражается в незрелости как тканей шейки матки, так и других тканей родового канала.
Нами были выявлены различия между группами по массе новорожденного. Была выявлена взаимосвязь между большей массой тела при рождении ребенка и менее успешной ПР. Похожие данные были получены в исследовании Kamlungkuea T. et al. (2022), которые показали, что успешные влагалищные роды после преиндукции связаны с массой плода <3500 г [47]. Вместе с тем масса тела плода оказалась менее значимым фактором по сравнению с паритетом родов, оценкой по шкале Бишоп и многоводием.
Наше исследование имеет ряд ограничений, в первую очередь обусловленных ретроспективным дизайном исследования. Данные, полученные из амбулаторных карт и историй родов, не всегда полноценно отражают всю полноту течения беременности, а также приема лекарственных препаратов. Более точные данные можно получить при проведении проспективного исследования, включающего более точную информацию об анамнезе и течении беременности у женщин.
Заключение
Исходя из вышеизложенного, предикторами более успешной и быстрой ПР в первую очередь являются изначальная оценка по шкале Бишоп, паритет родов и многоводие. Дискуссионным остается вопрос о перенесенных вирусных заболеваниях, в частности новой коронавирусной инфекции, что требует более детального изучения. Также нуждается в уточнении связь с применением препаратов прогестерона во время беременности. Наши данные показали, что женщинам, имеющим изначально более высокую оценку по шкале Бишоп, реже требовалось проведение эпидуральной аналгезии в родах и эпизиотомии по угрозе разрыва промежности, что коррелирует с более высокой степенью готовности организма к родам.



