Миома матки – наиболее часто встречаемое гинекологическое заболевание с распространенностью в репродуктивном возрасте, по данным разных авторов, от 20 до 70% [1–4]. Частота встречаемости миомы матки у беременных составляет 0,5–6% [3, 5–7] и неуклонно растет, коррелируя с ростом возраста деторождения, увеличением числа вспомогательных репродуктивных технологий, распространенностью гормональной терапии и контрацепции, а также эндокринных расстройств. Во время беременности отмечается рост миоматозных узлов, более характерный для I триместра [8]. До настоящего времени нет единой позиции в отношении выполнения миомэктомии во время операции кесарева сечения. Известен исторический факт, что впервые миомэктомию во время кесарева сечения выполнил Виктор Бонни, британский хирург-гинеколог, в 1913 г. Он произвел миомэктомию (удаление шести фибром больших размеров) 30-летней пациентке, после чего она еще трижды рожала через естественные родовые пути [9]. За прошедшие после этой публикации более 100 лет ситуация значительно не прояснилась. В настоящее время нет четких показаний, описания техник выполнения миомэктомии во время кесарева сечения. Наибольшее число русско- и англоязычных публикаций по запросу «миомэктомия во время кесарева сечения» представлены описанием клинических случаев [10–17]. Неоднозначные мнения о целесообразности миомэктомии во время кесарева сечения связаны с увеличением длительности операции, объема раневой поверхности и кровопотери, а также возможностью развития осложнений, таких как интраоперационное кровотечение, формирование межмышечных гематом операционной зоны, послеоперационные гнойно-септические осложнения, венозные тромбоэмболии, спаечная болезнь брюшной полости и отдаленных осложнений, связанных с наличием рубца на матке и влиянием его на последующую репродуктивную функцию [18–22]. Кроме того, подавляющее большинство современных врачей, имея узкую специализацию по акушерству, не обладают необходимыми хирургическими гинекологическими навыками, позволяющими расширять объем операции при необходимости до гистерэктомии.
В действующих клинических рекомендациях Министерства здравоохранения Российской Федерации «Миома матки» (2020) указано, что при родоразрешении путем операции кесарева сечения выполнять миомэктомию целесообразно лишь в случае наличия миоматозного узла, препятствующего извлечению плода [4]. Однако большинству практикующих акушеров хорошо известно, что послеродовое сокращение матки приводит к нарушению питания и ишемизации больших миоматозных узлов, субинволюции и нарушению опорожнения послеродовой матки, что отягощает течение послеродового периода. Несколько более широкие показания к миомэктомии во время кесарева сечения представлены в национальном руководстве «Акушерство» (2018), где указано, что миомэктомия во время кесарева сечения должна выполняться при наличии субсерозных узлов на тонком основании в любой доступной локализации, субсерозных узлов на широком основании (исключая нижний сегмент), при наличии крупных (более 10 см) узлов количеством не более 5, расположенных интрамурально, либо с центрипетальным ростом миоматозных узлов размерами более 10 см (не более одного узла), при хорошем доступе к узлу различной локализации, исключая интрамуральные с размерами менее 5 см [1]. Кроме того, при наличии множественной миомы матки с низким расположением узлов (шеечные, перешеечные), при малигнизации узла, подтвержденной гистологически во время операции, при необходимости одновременного удаления придатков матки (опухоли яичников, тубоовариальные образования) предписано выполнять гистерэктомию.
Что касается техники выполнения миомэктомии, для удаления интерстициальных миоматозных узлов применим способ, описанный Краснопольским В.И [23], при котором скальпелем производят линейный или овальный разрез тканей матки до визуализации капсулы узла. Последнюю также рассекают. Ткань узла фиксируют пулевыми щипцами в продольном направлении и подтягивают в рану. Производят удаление узла, ушивают ложе узла двух- или трехрядным швом. Недостатком этого способа являются повышенная кровоточивость вследствие гестационных изменений миометрия, трудоемкий гемостаз при повреждении серозной оболочки матки, риск развития спаечного процесса в месте повреждения висцерального слоя брюшины. Сложности с гемостазом увеличивают длительность операции, количество используемого шовного материала, риск ранних и отдаленных послеоперационных осложнений. В литературе описаны способы эндометриальной миомэктомии, которая проводится во время кесарева сечения со стороны полости матки [24].
К сожалению, действующие и обязательные к исполнению клинические рекомендации не дают юридической защиты врачу при расширении объема операции кесарева сечения. В этих условиях принятие решения о миомэктомии, техническое исполнение и ответственность за исход операции лежат на хирурге.
Целью нашего исследования явилась оценка возможности выполнения миомэктомии во время операции кесарева сечения разными техническими способами, влияния расширения объема операции на длительность операции, объем интраоперационной кровопотери и течение послеоперационного периода.
Материалы и методы
Исследование проводилось на базе отделения патологии беременности клиники Санкт-Петербургского государственного педиатрического медицинского университета (СПбГПМУ). Изучены протоколы операций 377 пациенток, родоразрешенных путем операции кесарева сечения, истории родов 69 родильниц с миомой матки, которые были разделены на 2 группы: 1-я группа – 24 женщины с выполненной во время операции кесарева сечения миомэктомией и 2-я группа – 45 пациенток, которым миомэктомия не выполнялась. Проанализированы истории болезни, протоколы операций, лабораторные (общеклинические, биохимические, бактериологические, гистологические) и инструментальные (ультразвуковое исследование) данные.
Статистический анализ
Статистический анализ данных проводился с использованием программы Statistica. Нормальность распределения признаков определялась на основании критерия Колмогорова–Смирнова с поправкой Лиллиефорса. Описательная статистика нормально распределенных показателей приведена в виде среднего значения (М) и стандартного отклонения (SD) в формате М (SD). Для количественных данных, не подчиняющихся нормальному распределению, применены медиана и интерквартильный интервал в формате Me (Q1; Q3). Сравнение совокупностей данных по количественным признакам при нормальном распределении производилось с использованием Т-критерия независимых выборок. Данные с асимметричным распределением анализировались с помощью U-критерия Манна–Уитни. Уровень пороговой величины р, определявший статистическую значимость, принимался за 0,05. Описательная статистика качественных данных приведена в виде абсолютных и относительных частот.
Результаты
Изучены истории родов 377 пациенток отделения патологии беременности перинатального центра клиники СпбГПМУ, которые были родоразрешены путем операции кесарева сечения в плановом порядке в 2022 г. У 69/377 (18,3%) женщин была диагностирована миома матки. Миомэктомия во время кесарева сечения была произведена у 24/377 (6,4%) пациенток. Принятие решения о необходимости миомэктомии, с учетом персонифицированных рисков, производилось коллегиально, совместно с заместителем главного врача и заведующим отделением, накануне операции или интраоперационно. В зависимости от объема операции исследуемые были разделены на 2 группы. В 1-ю группу вошли 24 пациентки, которым во время кесарева сечения была произведена миомэктомия, 2-ю группу составили 45 женщин с миомой матки, которые были родоразрешены путем операции кесарева сечения в плановом порядке без расширения объема операции до миомэктомии. Средний возраст пациенток 1-й группы составил 36,08 (4,4) года против 38,58 (5,1) года – во 2-й, р=0,048.
Оценивая более подробно группу женщин, у которых во время кесарева сечения выполнена миомэктомия, мы выявили, что у 12/24 (50%) миома матки явилась основным показанием к оперативному родоразрешению в связи с тем, что большие миоматозные узлы находились в области перешейка матки по передней и задней стенкам и препятствовали бы прохождению плода по родовым путям матери, либо за счет своих гигантских размеров потенциально привели бы к аномалиям родовой деятельности. Всего нами было удалено 39 миоматозных улов от 2 до 15 см у 24 пациенток. Анализируя локализацию удаленных узлов, установлено, что большинство из них находились на передней стенке тела матки 23/39 (59,0%), по 5/39 (12,8%) узлов были удалены из перешеечной области передней стенки и дна матки, по 3/39 (7,7%) располагались в области перешейка задней стенки и в теле задней стенки матки. По типу удаленных миоматозных узлов, согласно классификации FIGO, распределение происходило следующим образом: подавляющее большинство имело интерстициальный (тип 4; 18/39 (46,1%)) и интерстициально-субсерозный (тип 5; 14/39 (35,9%)) характер роста. Субсерозный (тип 6–7) характер имели 5/39 (12,8%) удаленных узлов. Реже удалялись узлы с интерстициально-субмукозным (тип 2–3) и интралигаментарным (тип 8) характером роста, по 1/39 (2,6%) соответственно.
В меню наших технических возможностей при удалении узлов были разные варианты. Окончательное решение принималось интраоперационно после визуальной и пальпаторной оценки узла. Миомэктомия 2/39 (5,1%) узлов была произведена до гистеротомии для извлечения плода. Это были случаи, когда большие миоматозные узлы располагались в нижнем маточном сегменте передней стенки в зоне вскрытия матки для извлечения плода. Однако, несмотря на нестандартное начало кесарева сечения, извлечение плода в этих ситуациях происходило на 4-й и на 5-й минуте от начала операции и не повлияло на оценки новорожденных по шкале Апгар при рождении. Более половины 22/39 (56,4%) миоматозных узлов удалялись типично, после вскрытия серозной оболочки матки [23]. Однако в данных ситуациях нами выполнялся сагиттальный разрез над миоматозным узлом в 2 раза меньше, чем пальпаторно определяемый размер узла. Хорошая сократительная способность матки и редуцированный размер разреза позволяет снизить число возможных осложнений, связанных с гемостазом в ране. Миомэктомия 2/39 (5,1%) узлов была произведена со стороны полости матки, так называемая эндометриальная миомэктомия. Эта техника, на наш взгляд, является наиболее удачной при интерстициально-субмукозном и интерстициальном характере роста узлов. Пластичность послеродовой матки позволяет пальпаторно выдавить миоматозный узел в выгодное для хирурга направление. Операции, выполняемые без повреждения серозной оболочки матки, выгодно отличаются в плане снижения интраоперационной кровопотери. В 13/39 (33,3%) случаях миомэктомия была выполнена трансмуральным путем. Это происходило при расположении интерстициального миоматозного узла по передней стенке матки на расстоянии не более 4 см от края разреза на матке, выполненного для производства кесарева сечения. Техническое исполнение данного вида миомэктомии происходило следующим способом: кесарево сечение производится типично поперечным разрезом в нижнем маточном сегменте. Далее визуально и пальпаторно определяется размер, положение, характер роста миоматозного узла. При расположении миоматозного узла размером более 5 см с интерстициальным характером роста (тип 3–5 по FIGO) по передней стенке матки на расстоянии не более 4 см от края гистеротомического разреза производится поперечный разрез мышцы матки в толще гистеротомического разреза, выполненного для кесарева сечения. Формируется тоннель до нижнего полюса миоматозного узла, вскрытие капсулы узла, захват узла пулевыми щипцами, энуклеация узла острым и тупым путем. Длина разреза и глубина тоннеля зависят от размеров миоматозного узла. Далее производится ушивание ложа узла и сделанного для его удаления тоннеля П-образными швами через всю толщину стенки матки, с завязыванием узлов на стороне серозной оболочки матки. Количество П-образных швов зависит от размера удаленного узла. Мы считаем, что выполнение миомэктомии трансмуральным доступом к миоматозному узлу во время кесарева сечения приводит к снижению травматизации матки, сохранению целостности серозной оболочки матки, снижению интенсивности интраоперационного кровотечения, сокращению длительности операции, количества использованного шовного материала, снижению числа интра- и послеоперационных осложнений [25].
У 11/24 (45,8%) женщин кесарево сечение с миомэктомией было дополнено другими хирургическими действиями. А именно: у 7/24 (29,2%) пациенток произведена деваскуляризация матки путем перевязки ветвей маточных артерий; по 1/24 (4,2%) случаю пришлось на овариоцистэктомию и адгезиолизис. При выполнении эндометриальной миомэктомии у одной из пациенток с целью профилактики кровотечения в раннем послеоперационном периоде мы применили маточный баллонный катетер Жуковского. У одной пациентки из группы кесарева сечения с миомэктомией была произведена гистерэктомия. Это пациентка З., 38 лет, со вторыми родами, с множественной миомой матки больших размеров с перешеечным расположением узлов. При интраоперационной ревизии выявлено, что доминантный узел № 1 размером 15 см, с интерстициальным характером роста располагался в перешеечном отделе задней стенки матки, деформировал полость матки за счет своих размеров. Ниже этого узла, визуально определяемый в шеечной зоне, ограниченно подвижный определялся миоматозный узел № 2 с субсерозным характером роста и размером около 8 см в диаметре. Интраоперационным консилиумом, учитывая высокий риск массивного интраоперационного кровотечения при миомэктомии, связанного с топографией и размерами узлов, решено произвести тотальную гистерэктомию без придатков матки.
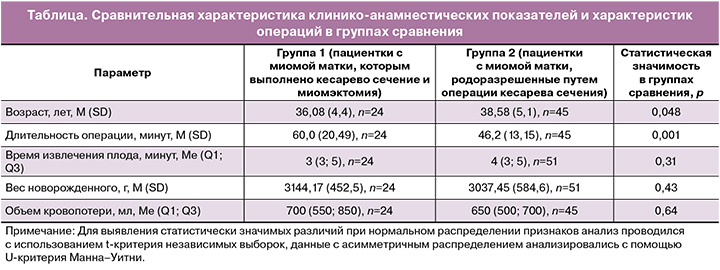
Для анализа операций и их исходов мы сравнили длительность оперативных вмешательств, время извлечения, объем кровопотери, течение послеоперационного периода пациенток группы 1 (с миомэктомией во время кесарева сечения, n=24) и группы 2 (с миомой матки и без миомэктомии во время кесарева сечения, n=45) (таблица). Установлено, что длительность операций у пациенток 1-й группы была статистически значимо выше и составила 60,0 (20,49) минут против 46,2 (13,15) во 2-й, p=0,001. Во 2-й группе было родоразрешено 6 беременных двойнями, и у 45 пациенток родился 51 ребенок. Не выявлено статистически значимых различий во времени извлечения плода от начала операции; оно составило 3 (3; 5) минут в 1-й группе и 4 (3; 5) минут – во 2-й, p=0,31. Объем интраоперационной кровопотери рассчитан как 700 (550; 850) мл в 1-й группе и 650 (500; 700) мл – во 2-й, что не имеет статистически значимых различий, p=0,64. Значимого влияния на вес и состояние новорожденных миома матки не оказала, что привело к рождению всех детей в обеих группах без гипоксии с весом 3144,17 (452,5) г в 1-й группе и 3037,45 (584,6) г – во 2-й, p=0,43. В послеоперационном периоде всем родильницам из 1-й группы назначалась антибактериальная терапия цефтриаксоном в суточной дозе 2,0 на 5 суток и профилактика венозных тромбозов препаратами низкомолекулярных гепаринов; длительность зависела от расчета риска венозных тромбоэмболий. Расширение объема операции не привело к возникновению послеоперационных осложнений; родильницы обеих групп были выписаны домой своевременно на 4–6-е сутки послеродового периода.
Заключение
Миомэктомия во время абдоминального родоразрешения при рациональном подходе к ее планированию и выполнению не приводит к росту объема кровопотери и других интра- и послеоперационных осложнений. Миомэктомия во время операции кесарева сечения должна выполняться мультидисциплинарной командой в учреждении 3-го уровня. В состав операционной бригады должны входить хирурги (владеющие техникой гистерэктомии, перевязки сосудов, наложения различных видов гемостатических швов), анестезиолог, трансфузиолог, неонатолог. В плане предоперационной подготовки необходимо тщательное обследование, включающее УЗИ, магнитно-резонансную томографию для точного топографического описания опухоли. Необходимы обсуждение с пациенткой особенностей операции, рисков и возможных интраоперационных осложнений, получение информированного согласия на выполнение кесарева сечения с расширением объема операции до гистерэктомии. Снижение рисков интраоперационной кровопотери обеспечивается предоперационной заготовкой компонентов крови для возможной гемотрансфузии, использованием кровосберегающих технологий (интраоперационная реинфузия крови), хирургических гемостатических технологий. Техника оптимизации миомэктомии зависит от локализации миоматозного узла, характера его роста, предпочтений хирурга. Миомэктомия может выполняться через операционную рану трансмурально, типичным способом со вскрытием серозной оболочки над узлом и дальнейшим вылущиванием узла, трансэндометриально. Результаты представленного исследования подтверждают возможность выполнения миомэктомии во время кесарева сечения и безопасность данного подхода, что способствует улучшению непосредственных и отдаленных результатов лечения и имеет значительную медико-экономическую эффективность.



