Проблема обильных менструальных кровотечений (ОМК) остается одной из нерешенных в практике врача-гинеколога, частота встречаемости ОМК до конца неизвестна. Анализу информации мешают различия в культурных, социальных и возрастных восприятиях «нормальной» менструации [1, 2]. ОМК считаются наиболее распространенным типом аномальных маточных кровотечений (АМК). Чрезмерная кровопотеря во время менструации оказывает отрицательное влияние на физическое, социальное, эмоциональное (анемия, болевой синдром, чувство усталости, вялости, изменение качества жизни) и/или материальное благополучие женщины и ее семьи. У женщин с ОМК риски госпитализации повышаются в 2,7 раза, вызовов скорой помощи – в 1,4 раза, амбулаторных посещений врача – в 1,3 раза по сравнению с женщинами без подобных жалоб [3].
Если говорить о статистике 2018 г., то 1 млн женщин в год обращаются за медицинской помощью в связи с АМК в Великобритании; по поводу АМК выполнено 17,8 оперативных вмешательств на 10 000 женщин репродуктивного возраста в США. При этом в 2007 г. общие годовые прямые и косвенные затраты на АМК в США превысили $37 млрд. В РФ АМК встречается хотя бы один раз в жизни более чем у половины женщин репродуктивного возраста [4–6]. Пристальное внимание к АМК (в том числе ОМК) в настоящий момент и потому, что, наряду с возрастом старше 60 лет, сахарным диабетом, системной артериальной гипертензией, ожирением, приемом тамоксифена, АМК связаны с раком эндометрия [7].
По данным FIGO (2018), почти 50% женщин с АМК не обращаются за медицинской помощью. Это, во-первых, влияет на частоту выявления патологии, во-вторых, увеличивает частоту материнской заболеваемости и смертности для беременных женщин с существующей анемией, связанной с АМК [8].
В сознании женщины наличие менструации означает фертильность и отсутствие беременности [9]. При проведении эпидемиологических исследований (n=475) был показан низкий уровень осведомленности женской популяции о проблеме ОМК. Было показано, что 41% женщин с кровопотерей более 80 мл оценивали свои менструации необильными или даже скудными, а 14% женщин, теряющих менее 20 мл менструальной крови, считали свои менструации обильными [10]. Недостаточная информированность и непонимание проблемы ограничивают обращение женщин за помощью. В настоящее время нет точных данных о достоверном количестве женщин с ОМК.
Чтобы приспособиться к ОМК, женщины (более 50%) планируют свою жизнедеятельность под менструации: носят специальное белье или одежду, используют несколько средств защиты одновременно, избегают длительного сидения и активных мероприятий в эти дни. В исследовании было показано, что социальная активность (страдают учеба или работа, занятия спортом и домашние дела) и сексуальная жизнь нарушены более чем у 2/3 женщин (n=1627) с ОМК [11]. Сама женщина с АМК или ОМК сообщает о значительном снижении качества жизни, но, с другой стороны, только 18% врачей (при этом нет зависимости от возраста, пола, опыта, места работы врача) при анонимном опросе считают изменение качества жизни важным аспектом при обсуждении проблемы АМК с пациенткой [12], что абсолютно противоречит даже определению АМК (и ОМК) согласно данным Национального института развития здравоохранения Великобритании (NICE).
Определение ОМК, предложенное NICE в 2007 г., по нашему мнению, в наибольшей степени подходит для клинической практики и является альтернативой определению, основанному на физическом измерении кровопотери, что, как показывает практика, является очень субъективным показателем. Согласно NICE, ОМК – это чрезмерная менструальная кровопотеря, которая оказывает влияние на физическое, социальное, эмоциональное и/или материальное благополучие женщины [1]. Данное определение абсолютно полностью было подтверждено в документе NICE в 2018 г. и введено в терминологию нормального и аномального кровотечения FIGO (Международная федерация акушеров и гинекологов) в этом же году [13]. В нашей клинической практике мы окончательно перестали использовать в лексике «меноррагия», «гиперменорея», «гипоменорея», «менометроррагия», «дисфункциональное маточное кровотечение», существуют только АМК, ОМК, обильное и длительное менструальное кровотечение, межменструальное кровотечение [6, 14].
Причинами ОМК могут быть как органическая, так и неорганическая патология. В 2011 г. была впервые принята «Классификационная система FIGO (PALM-COEIN) причин аномальных маточных кровотечений у небеременных женщин репродуктивного возраста» (рис. 1). В ней представлены 9 основных категорий: polyp (полип) (АМК-Р); adenomyosis (аденомиоз) (АМК-А); leiomyoma (лейомиома) (АМК-L); malignancy (малигнизация) (АМК-М) и hyperplasia (гиперплазия); coagulopathy (коагулопатия) (АМК-С); ovulatory dysfunction (овуляторная дисфункция) (АМК-О); endometrial (эндометриальное) (АМК-E); iatrogenic (ятрогенное) (АМК-I) и not yet classified (еще не классифицированное) (АМК-N).
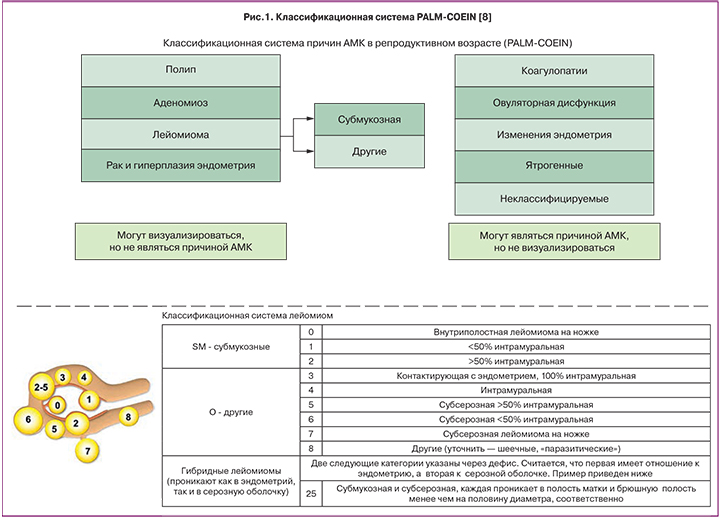
В 2018 г. эксперты FIGO изменили некоторые позиции в терминологии для нормального и аномального кровотечения [8].
Частота:
- Аменорея теперь входит в категорию частоты.
Регулярность:
- Улучшенное определение регулярности
- Нормальное изменение – 8 дней (самое короткое – самое длинное).
- Незначительная разница в зависимости от возраста.
Длительность:
- Теперь существует только 2 категории длительности менструации
- Нормальная – ≤8 дней.
- Длительная – >8 дней.
Объем и определение симптомов ОМК
- Определение NICE.
- Объем кровотечений, достаточный для того, чтобы негативно повлиять на качество жизни женщины.
Межменструальное кровотечение
- Спонтанное кровотечение, происходящее между менструациями.
- Циклическое.
- Беспорядочное.
А также была проведена коррекция в отношении классификационной системы PALM-COEIN (рис. 1) [8].
1. АМК-A. Улучшенные критерии ультразвуковой диагностики.
2. АМК-L. Определение 3 типа узла как субмукозная миома матки. Типы и отличия между узлами:
- типов 0 и 1; 6 и 7;
- типов 2 и 3; 4 и 5.
3. АМК-C. Больше не содержит АМК, связанные с препаратами, которые нарушают свертывание крови, теперь они включены в АМК-I.
4. АМК-I. Содержит АМК, связанные с любой ятрогенией, включая использование антикоагулянтов и препаратов, влияющих на овуляцию.
4. АМК-O. Введены новые диагностические пороговые изменения характеристик нормального кровотечения и цикла, описанные ранее. Не включает в себя овуляторные расстройства, связанные с лекарствами, известными или подозреваемыми в нарушении овуляции.
5. АМК-N. Название категории было изменено с «Еще не классифицированы» на «Не относятся ни к одной из категорий»
Эксперты FIGO в 2018 г. уделили отдельное внимание вопросу лекарственных средств, которые могут провоцировать АМК, и обратили внимание, насколько важен в этом вопросе сбор анамнеза [8]. Стоит обратить внимание на следующие препараты:
- препараты половых гормонов: эстрогены, прогестины и андрогены, в том числе лекарственные средства, влияющие на их синтез или являющиеся аналогами;
- нестероидные противовоспалительные средства, которые могут вызывать овуляторные расстройства;
- препараты, которые влияют на метаболизм допамина, включая фенотиазины и трициклические антидепрессанты;
- прямые оральные антикоагулянты (такие как апиксабан), считается, больше влияют на объем менструального кровотечения;
- антикоагулянт непрямого действия (варфарин).
Обсуждая вопрос важности полного сбора анамнеза пациентки, авторы документа подчеркнули важность первоначального скрининга для выявления коагулопатии у женщин с ОМК [8].
Скрининг (1-я линия) для выявления нарушений гемостаза у пациенток с ОМК должен проводиться на основании анализа данных анамнеза.
1. ОМК с менархе.
2. Одно из нижеперечисленных кровотечений:
- послеродовые;
- во время операции;
- кровотечение, связанное со стоматологическим вмешательством.
3. Два или более из следующих симптомов:
- синяки 1–2 раза в месяц;
- носовое кровотечение 1–2 раза в месяц;
- частая кровоточивость десен;
- случаи кровотечений в семейном анамнезе.
Алгоритм диагностики аномальных маточных кровотечений [8, 13]
Сбор анамнеза.
Объективизация чрезмерной менструальной кровопотери для исключения острого АМК (рис. 2, 3) [8, 13].
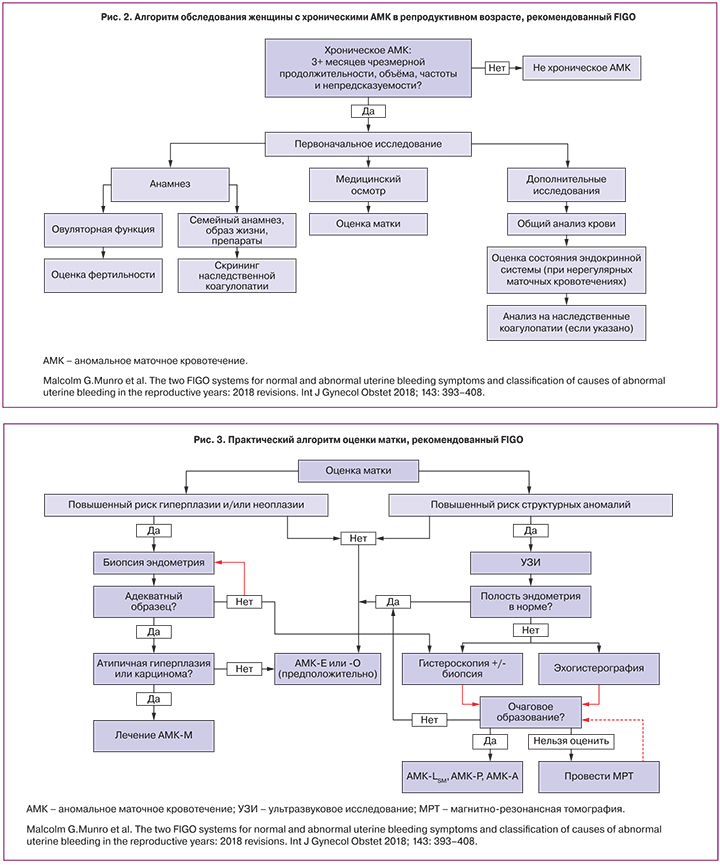
1. Установить факт кровотечения из матки (а не из влагалища, вульвы, промежности или перианальной области).
2. Исключить беременность (анализ мочи или сыворотки крови на наличие β-субъединицы ХГЧ).
3. У женщин с острым и хроническим АМК следует оценить дефицит железа; если это возможно, ферритин, а также уровни гемоглобина и/или гематокрита (предпочтителен полный анализ крови, включая тромбоциты).
4. После выявления кровотечения из матки (цервикального канала) клиницист оценивает каждый из компонентов системы PALM-COEIN.
5. Овуляторный статус. Оценка может включать (в некоторых ситуациях) измерение прогестерона в сыворотке в лютеиновую фазу. Биопсия эндометрия не рекомендуется в качестве метода определения овуляторного статуса.
6. Оценка функции щитовидной железы (при наличии клинических симптомов).
7. Показания к биопсии эндометрия (NICE 2018): постоянное межменструальное кровотечение; женщины в возрасте 45 лет и старше; неудачное или неэффективное лечение.
8. Ультразвуковой метод исследования – это диагностический инструмент первой линии для выявления структурных нарушений. Гистероскопию следует использовать в качестве диагностического инструмента, если результаты УЗИ неубедительны (например, для определения точного местоположения миоматозного узла или точного характера аномалии).
9. Магнитно-резонансная томография не должна использоваться в качестве диагностического инструмента первой линии. Является альтернативой при невозможности проведения УЗИ/гистероскопии (при врожденных аномалиях).
10. Дилатация и выскабливание (РДВ) не должны использоваться в качестве диагностической процедуры.
Не стоит забывать о факторах риска патологии эндометрия (в том числе рака эндометрия), которые могут расширить спектр диагностического поиска:
- ожирение;
- возраст >45 лет;
- отягощенный семейный анамнез по синдрому наследственного неполипозного колоректального рака (синдром Линча) [8].
Следует подчеркнуть, что биопсия эндометрия и выскабливание эндометрия без гистероскопии малоинформативны.
Определяя тактику ведения пациентки с ОМК, следует придерживаться следующих принципов:
- компенсация основного заболевания, которое может провоцировать появление ОМК, например гипофункции щитовидной железы (гипотиреоз), должна быть начата до применения любого из лекарственных средств, которые могут быть применены при ОМК;
- у женщин с анемией вследствие ОМК должна быть немедленно начата терапия препаратами железа.
Выбор терапевтической тактики в отношении ОМК основывается на клинических данных и данных анамнеза женщины:
- эффективность компенсации симптомов;
- переносимость побочных эффектов;
- соматический анамнез и/или гинекологический анамнез;
- возможный риск осложнений;
- длительность терапии;
- желание сохранить фертильность;
- приемлемость метода.
Независимо от типа ОМК, подход к выбору определенной лекарственной терапии должен зависеть от предпочтений пациентки и строго придерживаться персонифицированной медицины [10].
В случае безуспешности адекватной медикаментозной терапии следует рассмотреть варианты хирургического лечения.
Гормональные и негормональные методы терапии ОМК
Негормональные:
- нестероидные противовоспалительные средства (НПВС);
- транексамовая кислота.
Гормональные:
- прогестагены:
- внутриматочные;
- пероральные;
- комбинированные оральные контрацептивы (КОК);
- агонисты гонадотропин-рилизинг-гормона (а-ГиРГ).
Хирургические:
- аблация эндометрия;
- эмболизация маточных артерий;
- гистерэктомия;
- миомэктомия;
- гистероскопия с полипэктомией.
Рекомендации по подбору консервативной терапии, согласно Классификации доказательств и рекомендаций (Canadian Task Force on the Periodic Health Examination), следующие.
Негормональные методы терапии, такие как НПВС и антифибринолитики, могут быть эффективны для лечения тяжелых менструальных кровотечений, которые в основном являются циклическими и предсказуемыми по времени (I-A).
КОК (предпочтительно с диеногестом), ЛНГ-ВМС значимо снижают величину менструальной кровопотери и должны применяться у женщин с АМК, особенно нуждающихся в контрацепции (I-A).
Эффективность, приемлемость и качество жизни при использовании ЛНГ-ВМС сходны с таковыми при хирургическом лечении АМК, включая аблацию эндометрия и гистерэктомию (I-A).
Комбинация эстрадиола валерата с диеногестом (Э2В/ДНГ) в динамическом режиме приема обеспечивает значимое, быстрое и устойчивое снижение величины кровопотери (I-А).
Пероральные прогестины в циклическом режиме не являются эффективным методом снижения кровопотери и не должны применяться в качестве специфического метода лечения обильного менструального кровотечения (I-E).
а-ГнРГ эффективно снижают менструальную кровопотерю и могут использоваться в тех случаях, когда другие медикаментозные методы лечения потерпели неудачу или противопоказаны (I-C).
Пациенткам, получающим терапию а-ГнРГ более 6 месяцев, должна быть назначена дополнительная терапия эстрогенами, если она не была начата ранее (I-A) [10].
Гинекологами часто назначаются КОК при АМК. Действие КОК при АМК связано с подавлением секреции гонадотропных гормонов, функции яичников, ингибированием роста железистого эпителия эндометрия. Монофазные КОК применяются для проведения гормонального гемостаза в случаях острых АМК, а также для последующей противорецидивной терапии по контрацептивной схеме. Эффективность КОК при ОМК варьирует от 30 до 50% [15]. Важно отметить, что снижение кровопотери до 50% может не нормализовать показатели метаболизма железа (гемоглобин, гематокрит и ферритин). В двух исследованиях, сравнивающих ЛНГ-ВМС с КОК, содержащим ЛНГ 150 мкг/ЭЭ 30 мкг (21/7 режим) более 12 месяцев, уровни гемоглобина и ферритина значительно увеличились при использовании ЛНГ-ВМС (снижение объема кровопотери на 87,4%), но не при применении КОК (снижение объема кровопотери на 35,0%) [16, 17]. Не было отмечено положительной динамики в уровне гемоглобина и ферритина и в другом плацебо-контролируемом исследовании, оценивающем эффективность транексамовой кислоты в снижении менструальной кровопотери на протяжении 6 циклов, несмотря на значительное сокращение кровопотери (снижение среднего объема кровопотери на 40,0%) [18]. В то же время результаты 2 многоцентровых плацебо-контролируемых исследований показали высокую эффективность комбинации Э2В/ДНГ в динамическом режиме для снижения менструальной кровопотери. Прием препарата в течение 3 месяцев привел к уменьшению объема кровопотери во время менструации на 71–79%, а прием в течение 6 месяцев – суммарно на 88%, у 64% пациенток наблюдалась нормализация параметров менструального цикла [19, 20]. Данные этого исследования по уменьшению менструальной кровопотери коррелировали со значимым улучшением параметров метаболизма железа (гемоглобина, гематокрита и ферритина) и купированием таких симптомов, снижающих качество жизни женщины, как слабость и утомляемость. Ранняя пролиферация эндометрия под воздействием эстрогенов, увеличение экспрессии прогестероновых рецепторов, антипролиферативный эффект под влиянием ДНГ – это тот патофизиологический механизм, за счет которого мы получаем высокую эффективность. В 2012 г. КОК, в составе которого Э2В/ДНГ, был одобрен FDA, в 2013 г. зарегистрирован в России как лекарственное средство с показаниями: для контрацепции и лечения обильных и/или длительных менструальных кровотечений без органической патологии [21]. До сих пор Э2В/ДНГ остается единственным КОК, имеющим данное официально зарегистрированное показание в США и Европе, благодаря высокому профилю эффективности в отношении снижения менструальной кровопотери, доказанной в рандомизированных исследованиях и подтвержденной в исследованиях реальной клинической практики.
В 2018 г. были опубликованы результаты регистрационного исследования с целью оценки эффективности и безопасности Э2В/ДНГ в терапии ОМК у азиатской популяции женщин, нуждающихся в контрацепции. Было показано, что Э2В/ДНГ в динамическом режиме дозирования при тяжелой форме ОМК приводит к снижению объема менструальных выделений больше, чем плацебо (366,75 мл vs 149,14 мл соответственно, p<0,0001), причем ~52% и 12% женщин соответственно считали свое лечение «успешным». Значимое снижение кровопотери привело к повышению показателей гемоглобина и ферритина по сравнению с плацебо. Эти изменения положительно коррелировали с улучшением качества жизни женщин (снизилось количество пропусков на работе, повысилась производительность) [22]. Результаты данного исследования подтверждают ранее полученные данные в других исследованиях женщин с ОМК.
При сравнении с другими КОК было показано, что менструальные кровотечения становятся более легкими и скудными при переключении с ЭЭ-КОК на препарат Э2В/ДНГ [21]. У 5 из 10 девушек, переключившихся с ЭЭ-КОК на препарат Э2В/ДНГ, длительность кровотечения к концу исследования составляла всего 1–2 дня [23].
Обсуждая с пациенткой лечение АМК (в том числе ОМК), мы объясняем ей, что с целью уменьшения менструальной кровопотери прием препаратов должен быть длительным. Обсуждая КОК с Э2В/ДНГ, при отсутствии противопоказаний согласно ВОЗ [24], можно говорить о благоприятном профиле эффективности и безопасности препарата с целью контрацепции у девушек репродуктивного возраста, в том числе и у молодежи (18–35 лет) [25]. Следует отметить выводы, полученные в исследовании CONTENT, в котором принимали участие 3152 пациентки. Участницы, принимавшие ЭЭ-содержащий КОК, были переведены на комбинацию Э2В/ДНГ или чисто прогестиновые оральные контрацептивы по разным причинам. Важно, что именно молодые пациентки в возрасте от 18 до 25 лет среди принимавших Э2В/ДНГ высоко оценили препарат после переключения (80,2% – удовлетворены и очень удовлетворены приемом препарата) [23].
В отношении безопасности Э2В/ДНГ в 2016 г. было опубликовано международное проспективное контролируемое наблюдательное когортное исследование INAS SCORE (n=50 203), которое проводилось в США и 7 странах Европы (Австрия, Франция, Германия, Италия, Польша, Швеция и Великобритания). Цель исследования – оценка сердечно-сосудистых рисков на фоне Э2В/ДНГ в сравнении с другими КОК, в частности с комбинацией ЭЭ/ЛНГ, наиболее изученной в отношении венозной тромбоэмболии (ВТЭ). Анализ данных показал, что применение комбинации Э2В/ДНГ на протяжении до 5,5 года (в среднем в течение 2,1 года) сопровождалось таким же или даже более низким риском ВТЭ по сравнению с другими КОК и ЭЭ/ЛНГ [26].
В связи с низкой информированностью женщин об ОМК следует активно применять адаптированный опросник FIGO, который поможет уже на уроне первичного звена выявить проблему.
Заключение
Диагностика ОМК пока довольно сложна, но сложная диагностика требуется далеко не во всех случаях. Продумав алгоритм диагностики, оценив ответы пациентки при опросе и определив план необходимых действия, следует определить набор дальнейших исследований. ОМК значительно снижает качество жизни женщины, касаясь как физической, так и эмоциональной сферы, поэтому целями терапии ОМК являются уменьшение кровопотери во время менструации, нормализация и стабилизация показателей железа (в некоторых ситуациях – ферритина) и клинически значимое улучшение качества жизни.



