Последние десятилетия во многих странах мира характеризуются ростом заболеваемости гормонозависимыми гиперпластическими состояниями, к которым относятся гиперпластические процессы эндометрия. С одной стороны, имеется необходимость морфологического подтверждения диагноза, без чего невозможно оценить частоту, распространенность гиперпластических процессов эндометрия и степень онкологического риска. С другой стороны, это не может быть показанием к проведению тотального популяционного обследования с использованием диагностических внутриматочных вмешательств [1, 2]. Именно в связи с этим за последнее десятилетие стандартная эхография превратилась в гинекологии в рутинное исследование, которое широко используется клиницистами в качестве метода диагностики гиперплазии эндометрия.
«Золотым» стандартом в диагностике внутриматочной патологии на современном этапе является диагностическое выскабливание под контролем гистероскопии с последующим гистологическим исследованием соскоба [2, 3]. По данным Л.А. Ашрафяна, чувствительность метода составляет 93,8%, специфичность – 91,3% [4]. Несмотря на преимущества, этот метод имеет свои ограничения. Для выполнения гистероскопии необходимо дорогостоящее оборудование, что ограничивает возможность применения метода как стандартного скрининга. Кроме того, метод не лишен серьезных осложнений, а также требует специального обезболивания [5, 6]. Очень важен выбор времени диагностического выскабливания. Оптимально, если оно производится за 1–2 дня до предполагаемой менструации.
Аспирационная (Пайпель) биопсия эндометрия является одной из наиболее распространенных в Европе диагностических манипуляций в практике гинеколога [7–9]. По точности диагностики патологических изменений эндометрия аспирационная биопсия не уступает диагностическому выскабливанию. Чувствительность метода составляет 62,5–91,5%, специфичность — 94%, ложноположительные результаты встречаются в 31% случаев, ложноотрицательные – 7,9% [7, 8]. Необходимо отметить, что этот метод имеет следующие существенные преимущества: может производиться амбулаторно; является малоболезненной процедурой; длительность проведения манипуляции менее одной минуты; вызывает минимальную травматизацию, поскольку не требует расширения цервикального канала; позволяет получить ткань из любых отделов полости матки; снижает риск воспалительных осложнений.
Обобщая вышесказанное, можно заключить, что Пайпель-биопсия проще и дешевле обычной биопсии и имеет особые преимущества перед обычной процедурой в ситуациях, когда у пациентки есть риск распространения эндометриоза, бесплодие, а также при некоторых общих заболеваниях (например, сахарном диабете). Пайпель-биопсия позволяет проводить исследование практически безболезненно и без осложнений, в любое время, избегать лишних материальных затрат. Это имеет огромное значение, если тактика ведения пациентки требует регулярного повторного забора эндометрия для исследования.
Цель исследования: оценить недостатки двухмерного трансвагинального ультразвукового исследования и преимущества Пайпель-биопсии эндометрия в диагностике гиперпластических процессов эндометрия путем расчета корреляционных взаимосвязей между вышеуказанными методами и гистологическим заключением.
Материалы и методы исследования
Проведен ретроспективный анализ историй болезни женщин репродуктивного возраста с гиперпластическими процессами эндометрия гинекологических отделений г. Витебска за последние 10 лет.
Нами также проанализированы 128 историй болезни женщин репродуктивного возраста, поступивших в гинекологическое отделение для раздельного диагностического выскабливания под контролем гистероскопии и трансвагинальных ультразвуковых заключений в 2D-режиме с целью изучения их совпадений с окончательными гистологическими заключениями после раздельного диагностического выскабливания. Все ультразвуковые исследования были проведены амбулаторно, а пациентки направлены в стационар с подозрением на патологию эндометрия в плановом порядке. У всех пациенток отсутствовали жалобы и клинические симптомы гиперплазии эндометрия.
Возраст пациенток варьировал в пределах 36–44 лет. Толщина эндометрия составила от 7,1 до 13,00 мм. Внутриматочные вмешательства в анамнезе перенесли 46,9% пациенток. Менструальная функция не была нарушена в 95,3% случаев. Средний возраст менархе составил 13,33±1,53 года. Средняя продолжительность менструации – 5,23±1,59 дня, менструального цикла – от 28 до 30 дней. Умеренная менструальная кровопотеря отмечена в 61,7% случаев, отсутствие болезненных ощущений в период менструации – в 89,8% случаев.
Перед проведением раздельного диагностического выскабливания в асептических условиях после фиксации шейки матки пулевыми щипцами за переднюю губу без расширения цервикального канала аспирационным зондом «Юнона» («Симург», Санкт-Петербург, Россия) проводилась аспирационная биопсия эндометрия. Нами оптимизирована методика забора материала для цитологического и гистологического исследования, полученного путем Пайпель-биопсии эндометрия. Суть методики заключается в следующем. После извлечения аспирационного зонда из матки полученный материал помещали во флакон и заливали 10% раствором нейтрального формалина. Флакон маркировался и направлялся для стандартного гистологического исследования. Затем в шприц набирали 4–5 мл стерильного 0,9% раствора натрия хлорида и через аспирационный зонд смывали оставшийся в инструменте материал; смывную жидкость помещали в центрифужную пробирку и центрифугировали 8 мин при скорости вращения центрифуги не более 1000 об/мин (при большей скорости возможно разрушение клеток эндометрия). Надосадочную жидкость сливали, а из осадка приготавливали цитологические препараты, которые маркировали и направляли в цитологическую лабораторию. После проведения аспирационной биопсии проводили раздельное диагностическое выскабливание по стандартной методике с последующим направлением материала в гистологическую лабораторию.
Статистическая обработка данных осуществлялась с применением прикладного программного пакета Statistica 6.0 (StatSoft Ink., 1994–2001), адаптированного для медико-биологических исследований. Вычисляли относительные частоты признака (%). Нормальность распределения количественных признаков проверяли с использованием критерия Колмогорова–Смирнова. При использовании описательной статистики определялись параметры: выборочное среднее (Mean (М)); среднее квадратичное отклонение (SD); медиана (Ме), 25-й квартиль (25), 75-й квартиль (75) [10, 11]. Использован Roc-анализ.
Результаты и обсуждение
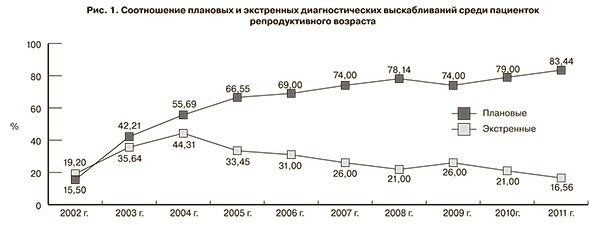
Нами проанализированы показания к проведению раздельного диагностического выскабливания в гинекологических отделениях и хирургическом кабинете дневного стационара за период времени с 2002 по 2011 гг. Из исследования были исключены женщины, поступившие в плановом порядке для проведения раздельного диагностического выскабливания в рамках предоперационного обследования с миомой матки, опухолями яичников. Мы проанализировали случаи госпитализации женщин репродуктивного возраста в плановом (подозрение на гиперпластический процесс эндометрия по данным ультразвукового исследования) и экстренном (обильные кровянистые выделения из половых путей) порядке (рис. 1).
 Следует отметить, что на протяжении последнего десятилетия процентный вес раздельных диагностических выскабливаний среди пациенток репродуктивного возраста, выполненных по экстренным показаниям, колебался незначительно (c 19,2 до 20–30%), достигая максимума в 2004 г. С другой стороны, количество плановых раздельных диагностических выскабливаний среди пациенток репродуктивного возраста значительно выросло к 2011 г. (2002 г. – 15,5%; 2011 г. – 83,4%).
Следует отметить, что на протяжении последнего десятилетия процентный вес раздельных диагностических выскабливаний среди пациенток репродуктивного возраста, выполненных по экстренным показаниям, колебался незначительно (c 19,2 до 20–30%), достигая максимума в 2004 г. С другой стороны, количество плановых раздельных диагностических выскабливаний среди пациенток репродуктивного возраста значительно выросло к 2011 г. (2002 г. – 15,5%; 2011 г. – 83,4%).
На наш взгляд, рост плановых раздельных диагностических выскабливаний связан с широким внедрением ультразвукового исследования в практику работы акушеров-гинекологов, так как в 100% случаев показаниями для плановых госпитализаций в проанализированных нами историях болезни были данные ультразвукового исследования.
Как показывает опыт многих специалистов ультразвуковой диагностики, оптимальным временем для проведения эхографии органов малого таза у женщин репродуктивного возраста является 5–7-й день менструального цикла. В эти дни менструального цикла при трансабдоминальном сканировании эндометрий либо не выявляется, либо определяется в виде тонкой эхогенной полоски, толщина которой не превышает 0,3 см. При трансвагинальном сканировании толщина эндометрия в эти дни менструального цикла составляет 0,3–0,6 см, эндометрий при этом должен быть полностью однородным, пониженной эхогенности [12].
Согласно данным литературы, ультразвуковыми критериями постановки диагноза гиперплазии эндометрия являются [12–15]: утолщение эндометрия (10 мм и более в первую фазу цикла; 15 мм и более – во вторую) и нередко овоидная форма М-эха; структура эндометрия при гиперплазии может быть неоднородной (иногда с наличием множества точечных анэхогенных включений), а эхогенность – повышенной; наружные контуры М-эха при гиперплазии обычно четкие и ровные; патологически измененный участок эндометрия может иметь как очень небольшие размеры, составляя 0,3–0,5 см, так и занимать всю или почти всю полость матки; может наблюдаться акустический эффект усиления позади значительно утолщенного эндометрия.
При анализе медицинской документации обращает на себя внимание, что врачи ультразвуковой диагностики зачастую диагностировали гиперпластический процесс эндометрия только на основании структуры эндометрия, а не его толщины и соответствия дню менструального цикла, причем исследование проводилось чаще всего в лютеиновую фазу цикла у пациенток с отсутствием клинического проявления патологии. Кроме того, до 2005 г. чаще использовалось трансабдоминальное ультразвуковое исследование, тогда как в последующие годы с целью диагностики патологии эндометрия чаще применялся трансвагинальный доступ, имеющий большую информативность, поскольку значительно повышается разрешающая способность ультразвукового оборудования; не требуется наполнение мочевого пузыря; ожирение, спаечный процесс в малом тазу и петли кишечника не оказывают существенного влияния на качество изображения; при трансвагинальном ультразвуковом исследовании сохраняется возможность двуручной манипуляции, что значительно повышает диагностический уровень обследования органов малого таза [16].
Несмотря на то что современные ультразвуковые сканеры обладают дополнительными возможностями использования допплеровских технологий (цветовое допплеровское картирование, энергетическое допплеровское картирование, импульсная допплерография), а в литературе приводятся допплерометрические показатели нормального маточного кровотока в течение менструального цикла [17], врачи ультразвуковой диагностики в единичных случаях используют эти методики.
В 39,8% случаев (51 женщина) ультразвуковые заключения не совпадали с гистологическими (при патогистологическом исследовании выявлен пролиферативный эндометрий), а следовательно, в репродуктивном возрасте каждая третья пациентка подвергалась необоснованному внутриматочному вмешательству, что особенно неблагоприятно в этом возрастном периоде, так как решается вопрос о сохранении здоровья и восстановлении репродуктивной функции.
Чувствительность и специфичность ультразвукового выявления патологии эндометрия колеблется в широких пределах по данным различных авторов. Например, по данным В.Н. Демидова, чувствительность ультразвукового выявления патологии эндометрия составляет 92,2%, а специфичность – 97,3% [12, 18, 19]. По данным А.Н. Стрижакова и А.И. Давыдова, точность ультразвуковой диагностики гиперпластических процессов эндометрия составляет 68,5%, полипов эндометрия – 67,7%, рака – 58,3% [12, 20]. Причем в репродуктивном возрасте чувствительность метода составляет 25%, в постменопаузальном – более 90% [21]. Как известно, к основным преимуществам метода относится его безопасность, неинвазивность и широкая доступность; но за последнее десятилетие именно этот метод исследования побуждает врачей акушеров-гинекологов к проведению травмирующей инвазивной диагностической процедуры – раздельному диагностическому выскабливанию. Несмотря на то что точность трансвагинальной эхографии значительно выше трансабдоминального ультразвукового исследования, остается много нерешенных вопросов, касающихся диагностики и дифференциальной диагностики гиперпластических процессов эндометрия. Необходимо отметить, что эхографическая дифференциальная диагностика гиперплазии эндометрия без атипии и атипической гиперплазии эндометрия практически невозможна [12]. А риск малигнизации именно атипической гиперплазии эндометрия составляет 50–100%, тогда как сложная гиперплазия эндометрия без атипии малигнизируется в 0,3–45,1%, простая гиперплазия эндометрия без атипии – в 1%. Поэтому скрининг, как правило, неэффективен среди женщин без клинической симптоматики болезни, что подтверждается рядом исследований. Так, трансвагинальная сонография с последующей биопсией эндометрия у 1926 получающих заместительную гормональную терапию выявила лишь 1 случай рака эндометрия [22].
 Оценку информационной значимости трансвагинальной эхографии в В-режиме при прогнозировании гиперпластического процесса эндометрия определяли при помощи Roc-анализа (Receiver Operating Characteristic analysis) c построением характеристической кривой зависимости чувствительности от вероятности ложноположительных результатов и измерением площади под ней. Выбирали оптимальную «точку разделения» – значение толщины эндометрия, которое наилучшим образом отражает компромисс между чувствительностью и специфичностью и позволяет оценить прогностическую ценность положительного и отрицательного результатов.
Оценку информационной значимости трансвагинальной эхографии в В-режиме при прогнозировании гиперпластического процесса эндометрия определяли при помощи Roc-анализа (Receiver Operating Characteristic analysis) c построением характеристической кривой зависимости чувствительности от вероятности ложноположительных результатов и измерением площади под ней. Выбирали оптимальную «точку разделения» – значение толщины эндометрия, которое наилучшим образом отражает компромисс между чувствительностью и специфичностью и позволяет оценить прогностическую ценность положительного и отрицательного результатов.
В качестве положительного результата (правильно предсказанного) теста в проведенном исследовании рассматривалось наличие гиперпластического процесса эндометрия в окончательном гистологическом заключении. Для проведения Roc-анализа была сформирована когорта из 104 пациенток.
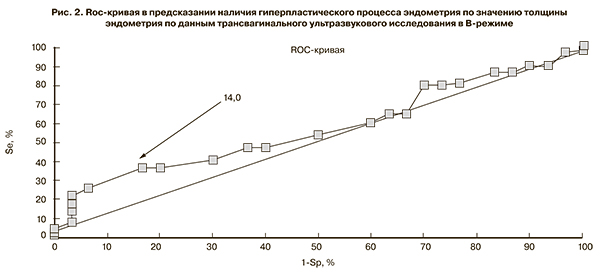
На рис. 2 приведена Roc-кривая в предсказании наличия гиперпластического процесса эндометрия исходя из значения толщины эндометрия.
Как видно на приведенном рисунке, оптимальным порогом классификации, обеспечивающим максимум чувствительности и специфичности теста (минимум ошибок I и II рода), является значение толщины эндометрия 14 мм. В этой точке чувствительность равна 36,5%, это означает, что у 36,5% женщин диагностический тест будет положительным. Специфичность в данной точке составила 83,3%, следовательно, 83,3% пациенток, у которых не будет гиперпластического процесса эндометрия, будут иметь отрицательный результат теста.
Площадь, ограниченная Roc-кривой и осью доли ложных положительных классификаций, составила 0,57, следовательно, предсказательную способность предлагаемой модели нельзя охарактеризовать как хорошую. Соответственно, трансвагинальная эхография в В-режиме не может являться методом скрининга патологии эндометрия.
Современной альтернативой инвазивным внутриматочным вмешательствам является аспирационная биопсия эндометрия, что побуждает исследователей максимально совершенствовать методику проведения этой малоинвазивной процедуры [21]. Мы забирали материал для цитологического и гистологического исследования путем Пайпель-биопсии эндометрия по методике, описанной в разделе «Материалы и методы».
Нами обследованы 50 пациенток репродуктивного возраста. Аспирационной биопсии эндометрия были подвергнуты пациентки, госпитализированные в гинекологическое отделение для раздельного диагностического выскабливания и гистероскопии в плановом порядке. Показанием для госпитализации стали данные рутинного трансвагинального ультразвукового исследования (ультразвуковое заключение: гиперплазия эндометрия).
Материал, полученный при Пайпель-биопсии, считали информативным для гистологического исследования, если заключение патоморфолога совпадало с результатами, полученными при раздельном диагностическом выскабливании. Материал считали информативным для цитологического исследования, если в препарате имелся эндометриальный эпителий. В дальнейшем мы анализировали данные цитологического исследования, полученные при Пайпель-биопсии, и сравнивали данные гистологического исследования материала, полученного путем раздельного диагностического выскабливания и аспирационной биопсии.
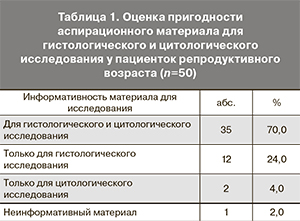
Из 50 пациенток репродуктивного возраста (табл. 1) у 35 (70,0%) материал аспирата был информативным как при цитологическом, так и при гистологическом исследовании. У 12 женщин (24,0%) репродуктивного возраста материал оказался информативным при гистологическом исследовании, но не информативным при цитологическом исследовании. А у 2 (4,0%) пациенток репродуктивного возраста материал был информативен при цитологическом исследовании, но не информативен при гистологическом исследовании. И только у 1 (2,0%) женщины материал был не информативен ни при цитологическом, ни при гистологическом исследовании.
Аспирационное исследование позволило получить информативные результаты у 49 из 50 женщин (98%). У 3 пациенток (6,0%) в цитологических препаратах не было обнаружено клеток эндометриального эпителия, что можно считать дефектами приготовления цитологических препаратов и недостатками техники получения аспирата.
Из табл. 2 видно, что информативность гистологического исследования полученного материала была достоверно (р<0,05) выше в сравнении с цитологическим методом исследования, несмотря на то что материал также обладал информативностью для цитологического исследования в высоком проценте случаев.
Учитывая, что при постановке диагноза гиперпластического процесса эндометрия и назначении последующей терапии врача интересует получение именно гистологического заключения, мы рассчитали диагностическую чувствительность и диагностическую специфичность метода Пайпель-биопсии эндометрия с учетом получения материала, пригодного для гистологического исследования с целью постановки диагноза. При расчетах за «золотой стандарт» приняты результаты гистологического исследования, полученные после проведения раздельного диагностического выскабливания.
Диагностическая чувствительность метода Пайпель-биопсии эндометрия составила 94%, диагностическая специфичность – 100%. Мы также рассчитали диагностическую эффективность метода, которая составила 97%.
С целью оценки взаимосвязи данных ультразвукового исследования и Пайпель-биопсии эндометрия с окончательным гистологическим заключением нами произведен расчет коэффициента ранговой корреляции Спирмана между полученными ультразвуковыми заключениями с окончательным гистологическим диагнозом (наличие или отсутствие гиперплазии эндометрия), а также между заключениями, полученными при Пайпель-биопсии и раздельном диагностическом выскабливании (наличие или отсутствие гиперплазии). Так, нами выявлены слабоположительные корреляции между полученными ультразвуковыми заключениями (толщина эндометрия) и гистологическим заключением (R=0,2; р>0,05). С другой стороны, нами выявлены статистически значимые выраженные положительные корреляционные взаимосвязи между гистологическими заключениями, полученными при Пайпель-биопсии и раздельном диагностическом выскабливании (R=0,8; р<0,001).
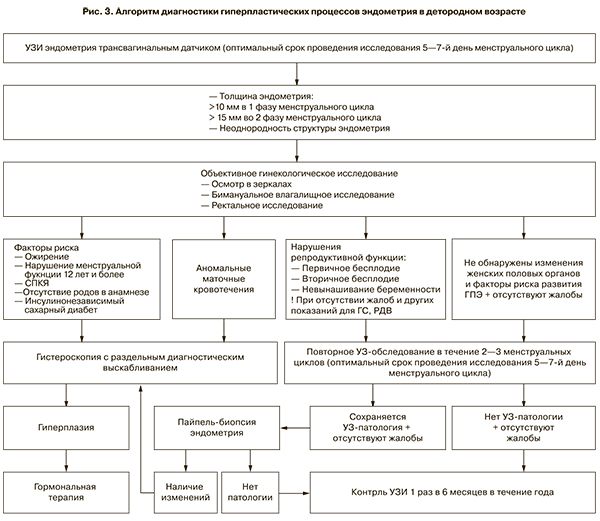
Исходя из приведенных выше данных видно, что аспирационная биопсия эндометрия обладает высокой информативностью, что позволило нам разработать алгоритм диагностики и лечения гиперпластических процессов эндометрия в репродуктивном возрасте (рис. 3). Это особенно важно для пациенток, не реализовавших репродуктивную функцию, особенно при наличии бесплодия, учитывая минимальную инвазивность вмешательства.
Заключение
За последнее десятилетие возросло количество плановых раздельных диагностических выскабливаний по поводу предполагаемых по данным ультразвукового исследования фоновых и предраковых заболеваний эндометрия среди пациенток репродуктивного возраста, тогда как количество выскабливаний, выполненных в экстренном порядке, колеблется незначительно.
Альтернативой диагностическому выскабливанию является аспирационная биопсия эндометрия, производимая в амбулаторных условиях с помощью миниатюрных инструментов, наиболее известным из которых является «Пайпель».
Несомненно, метод аспирационной биопсии является экономически выгодным, поскольку может выполняться в амбулаторных условиях и не требует анестезии. Одновременное использование гистологического и цитологического методов исследования материала, полученного при Пайпель-биопсии, улучшает качество диагностики внутриматочной патологии, что позволяет включить этот метод в алгоритм диагностики гиперпластических процессов эндометрия в репродуктивном возрасте.
Учитывая большой процент ложноположительных результатов, полученных при ультразвуковом исследовании, особенно у пациенток без клинических проявлений патологии, эхографические данные следует трактовать только в совокупности с факторами риска в динамике нескольких менструальных циклов.



