В последние годы отмечается стойкое увеличение продолжительности жизни населения. К 2030 г. каждый пятый человек в мире будет старше 65 лет [1–3]. В связи с этим актуальность изучения заболеваний женщин в постменопаузе возрастает.
Заболеваемость гиперпластическими процессами эндометрия в постменопаузе составляет 5%, и у 80% больных раком эндометрия в анамнезе имеются указания на гиперплазию эндометрия [4, 5].
Подтверждена связь между раком эндометрия и наличием в анамнезе рака молочных желез (РМЖ). Повышение риска рака эндометрия отмечается при приеме тамоксифена – синтетического антиэстрогенного препарата, используемого для лечения РМЖ. Риск развития рака эндометрия составляет 2–3 случая на 100 леченных тамоксифеном женщин, а вероятность возникновения аденоматозного полипа повышается с 10 до 36% [6–8].
Радикальным методом лечения внутриматочной патологии у пациенток, получающих адъювантную терапию РМЖ тамоксифеном, является гистерэктомия. Однако последняя часто бывает невозможной или нежелательной ввиду абсолютных или относительных противопоказаний [9–14].
В связи с вышесказанным актуален поиск новых альтернативных способов лечения патологии матки. Современный этап развития медицины с возможностью использования малоинвазивного доступа позволяет пересмотреть традиционные способы лечения внутриматочной патологии у пожилых и соматически отягощенных больных.
Гистерорезектоскопическая аблация эндометрия представляет эффективный метод лечения гиперпластических процессов эндометрия без сопутствующего приема тамоксифена и является альтернативой гормонотерапии и радикальному хирургическому вмешательству. Развитие самих моно- и биполярных гистерорезектоскопических технологий и применение их в практической деятельности показало высокую эффективность коагуляционной аблации эндометрия и безопасность, по сравнению с резекционной технологией у пациенток на фоне атрофии эндометрия и инволютивных изменений в стенке матки в постменопаузе [15–21].
Таким образом, лечение внутриматочной патологии в поздней постменопаузе, характеризующейся инволютивными процессами в репродуктивной системе, продолжает оставаться актуальной проблемой современной гинекологии.
Цель исследования: сравнительная оценка методов оперативного лечения патологии эндометрия при приеме тамоксифена у пациенток в поздней постменопаузе.
Материал и методы исследования
С ноября 2010 по сентябрь 2013 г. (34 месяца) были обследованы 136 женщин после лечения РМЖ, с толщиной эндометрия более 5 мм при трансвагинальном ультразвуковом исследовании (УЗИ), и/или с наличием симптома кровотечения. Все исследуемые женщины принимали тамоксифен, дневная доза которого составляла 20 мг, а длительность приема – от 6 месяцев до 5 лет. От всех пациенток было получено информированное согласие для включения в исследование. В исследование не включались пациентки с раком шейки матки, туберкулезом, имеющие противопоказания к оперативному вмешательству.
Предоперационное обследование включало: общие клинические методы исследования, расширенную кольпоскопию, УЗИ органов малого таза, диагностическую гистероскопию в сочетании с раздельным диагностическим выскабливанием (РДВ) слизистой цервикального канала и тела матки, полипэктомией, коагуляцией основания при необходимости, а также морфологическое исследование удаленных тканей. Показанием для гистероскопии стали: подозрение на патологию эндометрия по УЗИ и/или маточное кровотечение. Морфологическое исследование удаленных тканей было референсным тестом диагностики внутриматочной патологии.
На первом этапе исследования проводили клинико-статистическую характеристику обследованных женщин в общей выборке. Далее 136 пациенток были разделены на 3 группы. I группа составили пациентки, подвергшиеся монополярной коагуляционной гистерорезектоскопической аблации эндометрия после предварительной гистероскопии, РДВ и полипэктомии (n=54). Показанием к монополярной коагуляционной аблации послужило наличие и профилактика рецидивов патологии эндометрия.
Во II группу были включены пациентки, подвергшиеся биполярной коагуляционной гистерорезектоскопической аблации эндометрия после предварительной гистероскопии, РДВ и полипэктомии (n=32). Биполярную аблацию эндометрия проводили в случаях, когда имелись противопоказания к применению монополярной технологии в связи с экстрагенитальной патологией: эндопротезирование тазобедренных суставов в анамнезе, наличие искусственного водителя ритма сердца.
Моно- или биполярную аблацию эндометрия выполняли через 1 месяц после гистероскопии, РДВ, полипэктомии. Данный срок оптимален, так как за это время происходит поверхностная эпителизация эндометрия, что служит профилактикой повышения уровня интравазации во время электрохирургической аблации эндометрия. Монополярную или биполярную деструкцию эндометрия во всех случаях проводили с помощью гистерорезектоскопических инструментов фирмы Olympus (Япония).
Монополярную электродеструкцию эндометрия высокочастотным током проводили в режиме «коагуляции» при выходной мощности генератора 80–90 ВТ. В качестве электрода использовали «шар». Резекцию эндометрия, предполагающую его непосредственное удаление до миометрия, применили при полипах эндометрия, резецируя фиброзную «ножку» полипа до уровня неизмененного миометрия. В качестве оптической среды использовали диэлектрик – 5% раствор глюкозы. Биполярную электродеструкцию эндометрия проводили высокочастотным током в режиме «коагуляции» при выходной мощности тока генератора 120–150 Вт. В качестве электрода использовали «шар». Резекцию эндометрия применяли у пациенток при полипах эндометрия, резецируя фиброзную «ножку» полипа до уровня неизмененного миометрия при выходной мощности тока генератора 280 Вт. В качестве среды для расширения применяли 0,9% раствор хлорида натрия. В этих случаях для резекции использовали петлю-электрод с углом наклона 45°, что позволяло резецировать даже ножку полипа, исходящую из области трубного угла.
III группу составили пациентки (n=50), которые находились под наблюдением в течение 1 года после гистероскопии, РДВ и полипэктомии.
В послеоперационном периоде отдаленные результаты оперативного лечения патологии эндометрия в постменопаузе оценивали при помощи УЗИ и диагностической гистероскопии с использованием гибкого или жесткого офисного гистероскопа.
Внутреннюю поверхность матки в условиях офисной гистероскопии визуализировали с использованием однопроточного фиброгистероскопа диаметром 3,1 мм с операционным каналом 1,2 мм. Наличие операционного канала позволяло проводить прицельную «щипковую» биопсию эндометрия.
Манипуляцию проводили с учетом показаний и противопоказаний для проведения панорамной гистероскопии, в асептических условиях, амбулаторно, без расширения цервикального канала, фиксации шейки матки, обезболивания.
Результаты проведенного лечения оценивали в течение 12 месяцев. Через 3, 6 и 12 месяцев проводили УЗИ для динамического наблюдения за состоянием внутренних женских половых органов, изменением их размеров и структуры в связи с проведенным оперативным вмешательством.
Через 12 месяцев всем больным I, II и III групп проводили амбулаторную гистероскопию с прицельной и аспирационной биопсией эндометрия.
Результаты исследования
Средний возраст обследованных женщин составил 62±8,12 года (50–81 год). Средний возраст наступления менопаузы у пациенток соответствовал 50,1±4,1 года и варьировал от 34 до 63 лет (в том числе у 1 пациентки преждевременная менопауза в 34 года). Продолжительность постменопаузы у пациенток составила в среднем 10,25±6,4 года и колебалась от 5 до 30 лет.
Среди сопутствующих экстрагенитальных заболеваний наиболее часто встречались болезни сердечно-сосудистой – 92 (67,6%), пищеварительной – 73 (54%), эндокринной – 41 (30,1%) и мочеполовой системы – 51 (37,5%). При этом у 40 (29,4%) женщин выявляли ожирение.
Анализ гинекологической заболеваемости пациенток показал, что ее структура была представлена преимущественно миомой матки – 37 (27%), аденомиозом – 31 (22,7%) и воспалительными заболеваниями матки, придатков и влагалища – 30 (22%).
Изучение наследственного анамнеза показало, что в общей выборке 55 (40,4%) родственниц первой линии болели онкологическими заболеваниями.
 У 15 (11%) обследованных женщин была выявлена I стадия РМЖ, у 106 (78%) – II стадия, у 12 (8,8%) – III стадия, у 3 (2,2%) – IV стадия. Основным видом лечения было хирургическое удаление опухоли – в 135 (99,3%) случаях, в качестве адъювантной терапии применяли тамоксифен. В подавляющем большинстве случаев объем операции ограничивался односторонней мастэктомией – 113 (83,1%), двусторонняя мастэктомия применялась у 2 (1,5%) женщин, резекция молочной железы – у 20 (14,7%), а у 1 (0,7%) пациентки хирургическое лечение не проводилось. Лучевая и химиотерапия пациенткам с РМЖ проводилась в 12 (8,8%) и в 25 (18,4%) случаях соответственно. Суточная доза тамоксифена у всех женщин, вошедших в исследование, составила 20 мг. Продолжительность терапии тамоксифеном на момент выявления внутриматочной патологии варьировала от 3 до 24 мес.
У 15 (11%) обследованных женщин была выявлена I стадия РМЖ, у 106 (78%) – II стадия, у 12 (8,8%) – III стадия, у 3 (2,2%) – IV стадия. Основным видом лечения было хирургическое удаление опухоли – в 135 (99,3%) случаях, в качестве адъювантной терапии применяли тамоксифен. В подавляющем большинстве случаев объем операции ограничивался односторонней мастэктомией – 113 (83,1%), двусторонняя мастэктомия применялась у 2 (1,5%) женщин, резекция молочной железы – у 20 (14,7%), а у 1 (0,7%) пациентки хирургическое лечение не проводилось. Лучевая и химиотерапия пациенткам с РМЖ проводилась в 12 (8,8%) и в 25 (18,4%) случаях соответственно. Суточная доза тамоксифена у всех женщин, вошедших в исследование, составила 20 мг. Продолжительность терапии тамоксифеном на момент выявления внутриматочной патологии варьировала от 3 до 24 мес.
У 26 (19,1%) больных отмечены жалобы на кровяные выделения, а остальные 110 (80,9%) пациенток жалоб не предъявляли.
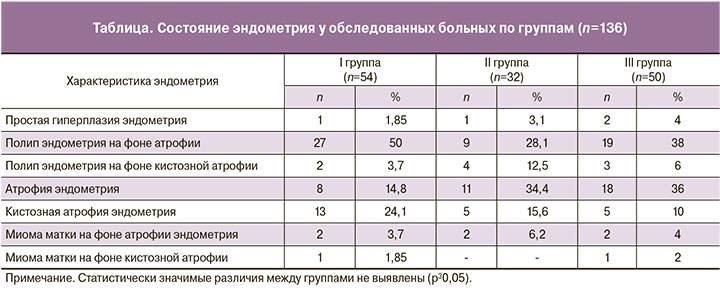
При морфологической верификации диагнозов после гистероскопии, РДВ и полипэктомии была выявлена следующая патология: полип эндометрия – у 64 (47,1%), при этом у 55 (85,9%) из них на фоне атрофичного эндометрия, 11 (14,1%) – на фоне кистозной атрофии, атрофия эндометрия – у 37 (27,2%), кистозная атрофия эндометрия – у 23 (16,9%), гиперплазия эндометрия – у 4 (2,9%) и миома матки – у 7 (5,9%) больных. Гистологически кистозная атрофия характеризовалась перигландулярной конденсацией стромальных клеток, эпителиальной метаплазией и пролиферативной активностью. При морфологическом исследовании все полипы оказались доброкачественными, ни одного случая малигнизации не было выявлено. Состояние эндометрия у больных после морфологической верификации диагнозов представлено в таблице.
Продолжительность гистерорезектоскопической коагуляционной аблации в моно- или биполярном режиме во всех исследуемых случаях колебалась от 10 до 25 мин. Средняя длительность операции составила 16,29±3,6 мин. Длина полости матки варьировала от 5 до 9 см, в среднем составила 7,0±0,9 см. Скорость прокатывания электрода по внутренней поверхности матки жестко не фиксировалась (в среднем 2–3 мм/сек), являясь субъективным параметром. Повторные прокатывания по уже обработанной поверхности не применялись. Выбранная нами скорость движения активного электрода обусловлена изменением цвета и внешнего вида эндометрия. Ткани, подвергшиеся деструкции, приобретали характерный желто-коричневый цвет, утрачивали рыхлую структуру.
Также был проконтролирован уровень интравазации, который не превышал 500 мл в I и II группах. Все больные, подвергшиеся би- или монополярной гистерорезектоскопической аблации эндометрия, после операции находились под наблюдением анестезиолога, получали профилактическую антибактериальную терапию. При отсутствии осложнений больные выписывались на 3-и сутки после операции.
На 2-е сутки после аблации эндометрия у 1 больной I группы была субфебрильная температура, обусловленная гематометрой. После зондирования полости матки и антибиотикотерапии больные выписывались на 5-е сутки с выздоровлением. Повторного образования гематометры не было ни у одной пациентки.
Критериями эффективности аблации эндометрия в проводимом исследовании были: отсутствие кровяных выделений, щелевидное М-эхо при УЗИ, наличие внутриматочных синехий при «офисной» гистероскопии, отсутствие ткани эндометрия при морфологическом исследовании.
Через 3 месяца ни у одной пациентки в I, II и III группах патологической эхографической картины не выявлено; соответственно не было показаний для проведения гистероскопии и РДВ. М-эхо щелевидное, менее 2–3 мм, с эхо-позитивными включениями (фиброз).
Через 6 месяцев после хирургической коррекции патологии эндометрия у всех женщин из I и II группы по УЗИ выявлена атрофия эндометрия. М-эхо щелевидное, менее 2–3 мм, с эхо-позитивными включениями (фиброз). В то же время у 5 (10%) женщин из III группы М-эхо было более 5 мм, что потребовало проведения повторной гистероскопии и РДВ.
Через 12 месяцев после хирургического лечения внутриматочной патологии в I группе только у одной пациентки (1,9%) М-эхо было более 5 мм, что и стало показанием для повторной гистроскопии с РДВ. Во II группе по УЗИ выявлена атрофия эндометрия. В III группе у 30 (60%) женщин наблюдалось утолщение эндометрия, что и стало показанием для повторной гистероскопии с РДВ.
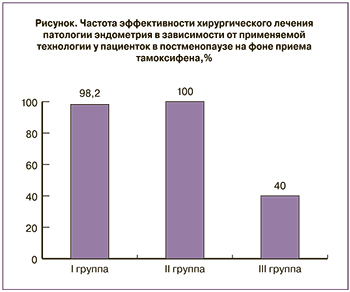
Таким образом, частота повторных гистероскопий в I группе составила 1,9%, во II группе ни у одной пациентки не было показаний к повторной гистероскопии, в III группе необходимость в проведении повторной гистероскопии имела место в 60%.
Таким образом, было показано, что у больных с внутриматочной патологией на фоне адъювантной терапии РМЖ по прошествии 12 месяцев динамического наблюдения эффективность метода коагуляционной высокочастотной электрохирургической аблации эндометрия значительно выше, чем гистероскопии, РДВ и резекции полипа, независимо от применения моно- или биполярной технологии. Анализ эффективности хирургической коррекции внутриматочной патологии на фоне адъювантной терапии РМЖ представлен на рисунке.
Обсуждение
В настоящее время ранняя диагностика и лечение патологии эндометрия в постменопаузе продолжает оставаться актуальной проблемой, составляющей 60–70% в структуре гинекологических заболеваний. Средний возраст пациенток с раком эндометрия составляет 60 лет, при этом ранняя диагностика и лечение внутриматочной патологии эндометрия являются вторичной профилактикой рака эндометрия [4, 22, 23].
В литературе имеется мало данных об эффективности гистерорезектоскопической коагуляционной деструкции эндометрия (моно- или биполярной) на фоне продолжающегося воздействия тамоксифена на эндометрий с целью предотвращения рецидивов. Первое рандомизированное исследование выполнили M. Goldenberg и соавт. в 1998 году, показавшие, что применение гистероскопической полипэктомии с монополярной аблацией эндометрия является эффективным методом лечения тамоксифен-ассоциированных полипов эндометрия, при объеме выборки 20 женщин в группе гистероскопии и РДВ и 10 – в группе аблации эндометрия [24].
Позже опубликовали результаты исследования W. Gao и соавт., где также придерживались данной тактики. Однако в указанной работе не были сформулированы группы сравнения и эффективность аблации оценивалась только при полипах эндометрия [25].
В настоящем исследовании на втором этапе после гистероскопии, РДВ, полипэктомии и коагуляции основания полипа проводили гистерорезектоскопическую аблацию эндометрия у 86 больных из I и II групп. Аблацию эндометрия проводили в случаях рецидивирования тамоксифен-ассоциированной патологии эндометрия. Монополярную гистерорезектоскопическую коагуляционную аблацию применяли в 54 случаях (I группа), а биполярную – в 32 случаях (II группа) при наличии противопоказаний к монополярной технологии.
Повторная гистероскопия (стационарная) с РДВ была применена в I группе у одной пациентки с жалобами на однократные кровяные выделения из половых органов, утолщением М-эха более 6 мм при УЗИ. При этом во время контрольной гистероскопии визуализировались синехии в области трубных углов на фоне атрофичного эндометрия и гиперемия в области перешейка. При морфологическом исследовании выявлена атрофия эндометрия. У остальных 53 больных рецидивы не были выявлены. По данным УЗИ через 12 месяцев у всех исследуемых М-эхо или отсутствовало, или было менее 3 мм, неоднородное, с фиброзом. При контрольной офисной гистероскопии у данных пациенток визуализировались внутриматочные синехии. У других исследователей частота рецидивов после аблации по данным гистологии составила 2–10% при сроках наблюдения 1,5–3 года. Во II группе повторная стационарная гистероскопия не понадобилась ни в одном случае. А в III группе повторную стационарную гистероскопию применяли у 30 (60%) больных ввиду рецидивирования тамоксифен-ассоциированной патологии эндометрия по данным УЗИ и офисной гистероскопии [24, 25].
Тамоксифен, вызывая стромальные изменения в эндометрии уже через 3 месяца после начала приема, приводит к ложноположительному утолщению М-эха при трансвагинальном УЗИ; у большинства женщин в постменопаузе, не имевших клинических проявлений, может иметь место доброкачественная патология эндометрия при приеме тамоксифена, в связи с чем необходимо проводить УЗИ малого таза до начала лечения тамоксифеном, далее каждые 6 месяцев; при выявлении ультразвуковым методом утолщения эндометрия более 5 мм рекомендуется проводить гистероскопию с биопсией; после морфологического исключения злокачественности изменений оптимально проведение гистерорезектоскопической коагуляционной аблации (в моно- или биполярном режиме) эндометрия в любые сроки антиэстрогенной терапии для предотвращения рецидивов.
Заключение
Проведение аблации эндометрия у пациенток, получающих адъювантную терапию РМЖ тамоксифеном, позволяет существенно снизить частоту рецидивов тамоксифен-ассоциированной патологии эндометрия. В результате анализа полученных данных в ходе исследования были сделаны выводы, что эффективность моно- и биполярной аблации значительно выше, чем гистероскопии, РДВ и полипэктомии (98,2, 100 и 40% соответственно).



