Рак молочной железы (РМЖ) занимает первое место среди злокачественных образований у женщин, как в мире, так и в России.
За последние десятилетия в связи с улучшением диагностических методов отмечен рост числа начальных стадий РМЖ, а также выявления cancer in situ, и, как следствие, растет число органосохраняющих операций на молочной железе, что является методом хирургической реабилитации пациенток.
Средний возраст выявления РМЖ у женщин составляет 50 лет, в последние годы наметилась устойчивая тенденция к увеличению числа молодых пациенток до 40 лет и количество пациенток данной возрастной группы по отношению к общему числу пациенткок с РМЖ возросло с 6 до 16% [1].
РМЖ на фоне беременности выявляют реже по сравнению с раком шейки матки и по частоте выявления РМЖ занимает второе место. На 1500–4000 беременностей выявляют один случай РМЖ, при этом средний срок гестации, на котором диагностируют заболевание, – 21 неделя [2].
Международный термин PABC: Pregnancy associated breast cancer («Рак молочной железы, ассоциированный (связанный) с беременностью» – РМЖСБ). РМЖСБ включает три ситуации: 1) рак диагностируют на фоне беременности, 2) рак диагностируют на фоне лактации и 3) рак диагностируют в течение одного года после завершения беременности.
Универсальной онкологической точки зрения по поводу тактики ведения пациенток с РМЖ на фоне беременности на сегодняшний день не существует, так как каждый случай индивидуален, в зависимости от стадии заболевания, срока гестации, локализации процесса, гистологических характеристик опухоли, решении пациентки о продолжении беременности. Так как время наступления беременностей и родов увеличивается у женщин в возрастной группе 35 лет и старше, то и рост выявления РМЖ на фоне беременности очевиден [6].
При сохранении беременности в III триместре возможны ранние преждевременные роды, а именно с 34-й недели.
Влияние беременности на течение и прогноз РМЖ не доказано. Несомненно, диагностика РМЖ у беременных имеет особенности, по этой причине высока вероятность ошибок, и, как следствие, выявляют местно-распространенные формы РМЖ. Также существует зависимость лечения от триместра беременности, в котором выявлена опухоль молочной железы.
Хирургическое лечение РМЖ при беременности не противопоказано и не зависит от триместра беременности; объем хирургического вмешательства зависит от стадии, локализации опухолевого узла и соотношения размера опухоли к размеру молочной железы. В I триместре беременности лекарственную терапию не проводят, так как практически все препараты проникают через плаценту и оказывают токсическое влияние на плод. По данным литературы, во II–III триместрах беременности цитостатические препараты не увеличивают частоту развития пороков у плода. Доказано, что препараты таксанового ряда во II–III триместрах беременности не влияют на риск патологии развития плода.
В случае НЕR2 положительного молекулярного типа опухолевого узла назначение трастузумаба приводит к маловодию и, как следствие, вызывает осложнения у плода, поэтому при беременности не назначают таргетные препараты. После родов целесообразно прекращение лактации особенно при продолжении курсов полихимиотерапии или гормонотерапии [2].
Лучевая терапия и гормонотерапия на фоне беременности не возможны из-за риска развития осложнений у плода.
Клиническое наблюдение
В МНИОИ им. П.А. Герцена обратилась пациентка З., 24 лет, диагноз: фиброаденома левой молочной железы (цитологическое исследование узлового образования левой молочной железы №2414/15 – фиброаденома). Данное исследование было выполнено по месту жительства, из обследований проведено УЗИ молочных желез, где описано ровное образование размером 15 мм, края образования четкие, локализация узла – верхне-внутренний квадрант, заключение УЗИ: фиброаденома левой молочной железы.
К ошибке можно отнести проведение только цитологического исследования образования молочной железы, в данном случае необходимо было выполнить гистологическое исследование опухолевого узла, но положительный момент в том, что пациентка была направлена на ультразвуковое исследование молочных желез, несмотря на молодой возраст, и что в итоге была выполнена секторальная резекция, которая позволила диагностировать онкологическое заболевание.
Пациентке в МНИОИ им. П.А. Герцена 15.05.2015 г. выполнена секторальная резекция левой молочной железы под местной анестезией, осложнений не было. Пациентка беременна (26 недель).
При плановом гистологическом исследовании Э 93533-36 узел 1,5×1 см. Микро-инвазивный рак без признаков специфичности солидного строения, 2-й степени злокачественности, опухолевый рост по краю резекции.
ИГХ –РЭ 0, РП 0, НЕR2 2+, Кi-67 15%, FISН-амплификация обнаружена – нелюминальный НЕR2 позитивный тип.
С учетом молодого возраста, неблагоприятного молекулярно-биологического типа опухоли на онкологическом консилиуме принято решение о проведении курсов полихимиотерапии (ПХТ) во время беременности.
С 15 июня 2015 г. проведено 2 курса ПХТ по схеме АС, лечение пациентка перенесла удовлетворительно, токсических и гематологических реакций не выявлено. Рекомендовано плановое кесарево сечение, которое выполнено 22.07.2015 г. на 36-й неделе, ребенок в анамнезе у пациентки второй, родилась доношенная девочка. Лактация медикаментозно остановлена.
Далее пациентке продолжены 2 курса химиотерапии по схеме АС и 4 курса ТН до 23.11.2015 г. с последующим продолжением таргетной терапии до года.
У пациентки, по данным генетического исследования крови, выявлена мутация в гене BRCA1, в связи с этим хирургическое лечение решено выполнить двустороннее, с профилактической подкожной мастэктомией справа с одномоментной реконструкцией молочной железы – на рисунке 1 пациентка до операции.
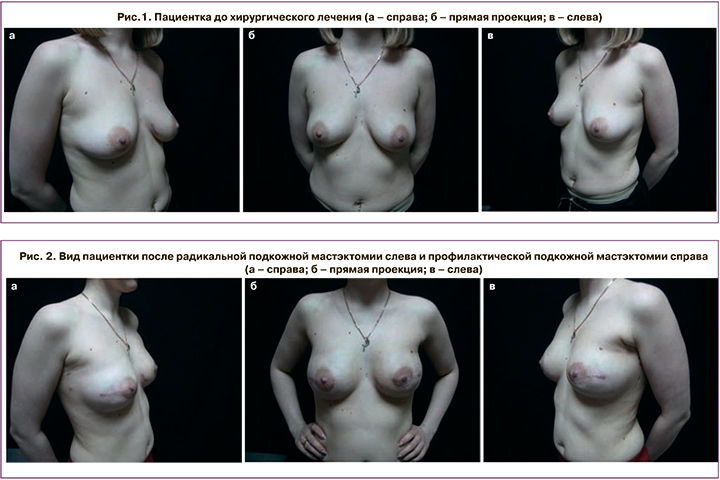
26.01.2016 г. выполнено хирургическое лечение в объеме радикальной подкожной мастэктомии слева с реконструкцией эндопротезом (425 см3) и сетчатым имплантатом (parietex), профилактическая подкожная мастэктомия справа с реконструкцией эндопротезом (425 см3) и сетчатым имплантатом (parietex).
На рисунке 2 пациентка через 2 недели после хирургического лечения, косметический результат хороший, молочные железы симметричные.
Гистологическое исследование послеоперационного материала АА 83830-58: 1) правая молочная железа 13×10×3 см, 2) левая молочная железа 15×12×3 см с клетчаткой и 14 лимфоузлами.
Микро – 1,2 в ткани левой и правой молочных желез фиброзно-кистозные изменения, опухолевого роста нет. В 14 лимфоузлах без метастазов.
После операции с учетом данных послеоперационного гистологического исследования рекомендована таргетная терапия до года.
В позднем послеоперационном периоде, через 4 месяца, выявлена протрузия импланта левой молочной железы, далее удаление импланта, повторная реконструкция левой молочной железы экспандером, замена экспандера на имплант, ротация импланта и реоперация реконструированной левой молочной железы из-за ротации импланта. Все этапы хирургических вмешательств выполнены с 2016 по 2021 гг. На рисунке 3 вид пациентки после хирургических вмешательств на левой молочной железе, симметрия сохранена, эстетический результат хороший.
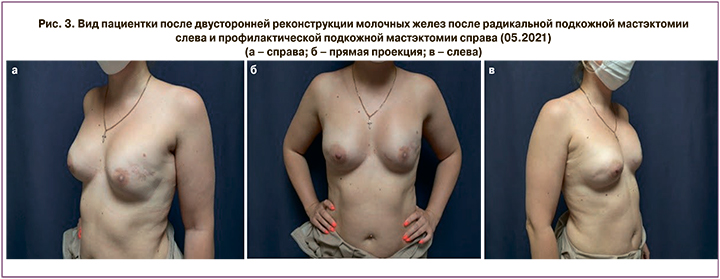
В настоящее время дочери 6 лет, отклонений в развитии не выявлено, девочка посещает детский сад, здорова.
При контрольном обследовании в июле 2021 г. пациентка находится в ремиссии, данных за прогрессирование РМЖ не выявлено.
Обсуждение
РМЖ у беременных имеет одинаковый прогноз при сравнении с небеременными молодыми женщинами, а сам прогноз зависит от стадии, молекулярно-биологического типа опухолевого узла, морфологических данных. Часто у беременных пациенток с диагнозом РМЖ преобладают нелюминальные типы опухоли (ЭР-/ПР-), на которые гормональные изменения в организме беременной женщины не влияют.
Выявление РМЖ в I триместре представляет дилемму для онколога. Если пациентка настаивает на сохранении молочной железы, лечение может представлять опасность как для эмбриона, так и для матери, поскольку включает обязательно лучевую терапию.
Если необходимый компонент лечения предполагает проведение химиотерапии, то это возможно во II–III триместрах. Наиболее часто применяют циклофосфамид и доксорубицин с 5-фторурацилом [3].
В работе Волочаевой М.В. (2014) показано, что новорожденные дети, которые родились у матерей, получавших курсы ПХТ во время беременности при РМЖ, практически не отличаются от группы сравнения, и наличие патологии новорожденных связана с досрочным родоразрешением, морфофункциональной незрелостью и недоношенностью, а не с проведением противоопухолевой терапии у беременных в анамнезе [4].
Надо признать, что в последние годы парадигма от прерывания беременности при РМЖ сменилась на возможности лечения во время беременности в случае желания пациентки сохранить беременность и возможность рождения здорового ребенка [5, 6], который прошел совместный путь противоопухолевого лечения матери, при этом необходимо дальнейшее наблюдение за данной группой детей.
Так же актуальным является вопрос о планировании беременности после лечения РМЖ, а именно, через какой период времени это возможно, какая беременность предпочтительна – самостоятельная или с применением вспомогательных репродуктивных технологий (ЭКО, криоконсервация яичниковой ткани, яйцеклеток), необходимость суррогатного материнства. Данные вопросы необходимо решать онкологам и гинекологам совместно.
В статье представлено клиническое наблюдение пациентки 24 лет, у которой во время беременности, по данным ультразвукового исследования, было диагностировано образование в молочной железе и выполнена пункция узлового образования. Следует отметить, что при наличии узловых образований в молочной железе на фоне беременности необходимо выполнять биопсию с гистологическим исследованием. Пациентка направлена в МНИОИ им. П.А. Герцена для хирургического лечения, по результатам которого при плановом гистологическом исследовании диагностирован рак молочной железы нелюминальный НЕR2 позитивный, с последующими курсами ПХТ, выполненными во время беременности, с последующим родами, продолжением хирургического лечения, таргетной терапией до 1 года. Обязательным является исследование крови на наличие мутаций у пациенток молодого возраста с РМЖ, несмотря на отсутствие отягощенного онкологического анамнеза, а также при всех биологических типах опухолевого узла, что и было выполнено у данной пациентки. Выявлена мутация гена ВRCА1, которая изменила хирургическую тактику лечения, была проведена подкожная радикальная мастэктомия слева с одномоментной реконструкцией, а также профилактическая подкожная мастэктомия справа с одномоментной реконструкцией, что безусловно, является хирургическим методом профилактики РМЖ.
Пациентка реабилитирована проведенными реконструкциями молочных желез эндопротезами. Период наблюдения за пациенткой и ребенком более 6 лет, и мама, и дочь здоровы, проводится дальнейшее наблюдение.
Заключение
Данным клиническим наблюдением мы хотим обратить внимание на наличие онкологической настороженности среди гинекологов, врачей женских консультаций, терапевтов и проведение у молодых пациенток на фоне беременности обязательного ультразвукового исследования молочных желез, а также рекомендовать УЗИ и после родов при наличии лактации для ранней диагностики узловых образований молочных желез и морфологической верификации методом трепан-биопсии.



