Перинатальная инфекционная патология – одна из актуальных и сложных проблем современного акушерства и одна из ведущих причин заболеваемости новорожденных. В России подтвержденная частота перинатальной смертности в результате инфекционно-воспалительных процессов составляет 10–18%, уступая внутриутробной гипоксии, асфиксии, респираторным расстройствам и врожденным аномалиям [2].
Частота ранней неонатальной смертности при внутриутробном инфицировании колеблется от 5,3 до 27,4%, а мертворождаемость достигает 16,8%.
В настоящее время не существует прямых (неинвазивных) методов диагностики, доказывающих наличие активного инфекционного процесса у плода. Для клинической практики важен не только факт инфицирования плода/новорожденного, но и определение степени активности течения инфекционного процесса. Постановка диагноза внутриутробно возможна только при проведении исследования крови плода, полученной методом кордоцентеза. Однако на современном этапе развития науки не существует данных о нормативах показателей иммунной системы плода, а этиологическая верификация возбудителя позволяет лишь установить факт внутриутробного инфицирования, в то время как спрогнозировать реализацию инфекции у конкретного пациента не представляется возможным [9]. Кроме того, в практике использование инвазивных методов обследования весьма ограничено в связи с наличием противопоказаний и небезопасностью их проведения.
Таким образом, встает вопрос о поиске косвенных достоверных методов прогнозирования развития инфекционного процесса у новорожденного на основании результатов обследования матери. Наиболее важным вопросом является прогнозирование внутриутробного инфицирования во время беременности и разработка алгоритмов ведения и лечения данной категории пациенток с целью снижения младенческой заболеваемости и смертности.
Целью настоящего исследования явилось выявление диагностических и прогностических критериев развития внутриутробной инфекции (ВУИ) для повышения эффективности лечения и снижения частоты осложнений беременности и неонатальной заболеваемости.
Материал и методы исследования
Проведен ретроспективный анализ историй родов 302 пациенток и новорожденных (2009–2010) с целью выявления клинико-анамнестических критериев риска ВУИ. Наряду с этим в проспективном исследовании под наблюдением находились 49 пар мать-новорожденный группы риска ВУИ с целью разработки прогностической модели и 53 пары мать-новорожденный группы риска ВУИ для оценки эффективности разработанного алгоритма. Обследование матерей осуществлялось во II–III триместрах беременности, подтверждение/исключение диагноза ВУИ проводилось по результатам дополнительного обследования новорожденного в первые сутки после родов. Основным материалом для исследования служили: венозная кровь, моча и ликвор (по показаниям). Определение ДНК потенциальных возбудителей проводили методом полимеразной цепной реакции (ПЦР) на наборах «ДНК-сорб-АМ» и «ДНК-сорб-В» и комплектах для амплификации «АмплиСенс» (производства ФГУН «Центральный научно-исследовательский институт эпидемиологии», Москва, Россия). Детекцию результатов осуществляли на многоканальном автоматическом люминесцентном анализаторе «АЛА-1/4» по конечной точке («Biosan», Латвия) или методом электрофореза при помощи УФ-трансиллюминатора в электрофоретической камере «SE-2».
Для установления взаимосвязей плаценты женщин были подвергнуты гистологическому исследованию.
Статистическая обработка осуществлялась с помо щью пакета прикладных программ Statistika-6 и стандартных математических таблиц Microsoft Excel. Для характеристики показателей, посвященных ретроспективному анализу историй родов беременных, использовались: непараметрический дисперсионный анализ Краскела-Уоллиса, однофакторный дисперсионный анализ для независимых выборок и статистика Кульбака. Для статистической обработки иммунологических исследований дополнительно был использован тест Манна-Уитни.
Для разработки оценочной прогностической таблицы вероятности развития ВУИ использовался последовательный анализ А. Вальда. При составлении диагностической таблицы для отбора наиболее информативных признаков использовался точный критерий Фишера. Информативность (I) каждого из диагностических коэффициентов рассчитывалась по формуле Кульбака, которая в отличие от критерия Хи-квадрат (χ2) оценивает не достоверность различия распределений, а степень этих различий. Малоинформативные (I<0,5) признаки были исключены из рассмотрения.
Проверка информативности прогностической таблицы производилась на исследованной группе женщин. Сравнивались предсказанные случаи ВУИ с фактическими и составлялась четырехпольная таблица с последующим определением чувствительности, специфичности, безошибочности, вероятности ложноположительного и ложноотрицательного ответов.
Результаты исследования и обсуждение
На I этапе при анализе 302 историй родов производилось формирование наиболее значимых
факторов риска, определение диагностических критериев ВУИ. Диагноз ВУИ ставился на основании положительных результатов ПЦР, иммуноферментного анализа, бактериологического исследования, проводимого у новорожденных детей. Удельный вес внутриутробной инфекции составил 21,19% (основная группа n=64). В том случае, если при дополнительном обследовании ВУИ не диагностировалось, пациенток включали в группу сравнения (n=238).
Результаты исследования показали, что наиболее значимыми критериями риска развития внутриутробной инфекции явились: осложненный акушерско-гинекологический анамнез (р=0,00),
перенесенные воспалительные заболевания органов малого таза (р=0,00), хронический пиелонефрит (р=0,01), наличие экстрагенитальных заболеваний (р=0,05); угроза прерывания настоящей беременности (р=0,00), вагинит (р=0,00), бактериальный вагиноз (р=0,00), респираторно-вирусные заболевания (р=0,03), перенесенные во время настоящей беременности. Из числа ультразвуковых маркеров наиболее значимыми оказались следующие критерии: задержка развития плода (р=0,04), нарушение плодово-плацентарного кровотока (р=0,02), многоводие (р=0,03), пиелоэктазии у плода (р=0,03), кальцинаты плаценты (р=0,03), утолщение плаценты (р=0,03), взвесь в околоплодных водах (р=0,000).
При проведении гистологического исследования плацент в случае подтверждения ВУИ преобладали восходящее и гематогенное инфицирование (32,79%), гематогенное инфицирование (24,59%), восходящее инфицирование и кальциномоторные процессы (14,75%) и восходящее инфицирование с инфарктами (4,92%). Доля соответствующих сроку гестации плацент составила 21,31 %. При отсутствии инфекции отмечались в основном незрелость последа (более половины всех случаев – 58,16%) и признаки патологической незрелости с приспособительными изменениями (30,54%), не считая плаценты, соответствующей сроку гестации – 9,21%. Различия групп по результатам морфологического исследования плацент были не только в высшей мере статистически значимы
(р=0,000), но и очень сильны (φ=0,89).
На II этапе исследования создана прогностическая модель ВУИ. Для ее формирования значимость выделенных факторов риска была еще раз проверена в проспективном исследовании у 49 беременных (табл. 1).
Таблица 1. Прогностическая таблица ВУИ.
Проверка прогностической таблицы показала, что она позволяет с 92%-ной точностью предсказывать наличие ВУИ и с 92%-ной точностью – ее отсутствие.
Результаты клинико-лабораторного обследования новорожденного подтвердили внутриутробное инфицирование у 17 детей, а в 32 случаях были выявлены гипоксические поражения центральной нервной системы (ЦНС) разной степени выраженности, сформировавшиеся в результате длительно существующей плацентарной недостаточности (ПН). В связи с этим основная группа была разделена на две подгруппы: 1-я –с наличием ВУИ (n=17), 2-я – с гипоксическим поражением ЦНС (группа сравнения n=32).
В 1-й подгруппе преждевременно родились 76,47% детей, средний срок продолжительности
гестации составил 31±3,4 нед. При этом в 76% случаев причиной преждевременных родов явилось дородовое излитие околоплодных вод, в 11% развилась спонтанная родовая деятельность, не поддающаяся медикаментозной коррекции, а в оставшихся случаях досрочно было проведено оперативное родоразрешение. Среди показаний к оперативному родоразрешению преобладала острая гипоксия плода (23%). У каждого второго ребенка диагностировали тяжелую или средней
степени тяжести асфиксию, при этом ее частота у недоношенных была в 3 раза выше по сравнению с доношенными (р=0,000). В данной подгруппе у 23,53% новорожденных отмечалась клиника поражения ЦНС в виде менингоэнцефалита и органического поражения головного мозга. При этиологической расшифровке из крови и/или ликвора была детектирована ДНК следующих патогенов: вируса простого герпеса 1, 2 типов – 11,8%, цитомегаловируса – 17,6%, вируса Эпштейна-Барр – 47,1%, вируса герпеса типа 6 – 5,9%. Частота микст-инфекции при различных ассоциациях возбудителей составила 17,6%. При герпесвирусной инфекции отмечалось более раннее начало заболевания – на 5–7-й день жизни, острое течение с повышением температуры тела, гипертензионным синдромом, нарушением микроциркуляции, гепатолиенальным синдромом, без специфических высыпаний на коже и слизистых оболочках, в ряде случаев с поражением кишечника в виде некротизирующего энтероколита. При исследовании ликвора цитоз был не более 1000 клеток сегментоядерного характера со сменой цитоза на лимфоцитарный на фоне специфической терапии. При стандартном бактериологическом исследовании ликвора во всех случаях получен отрицательный результат. В случаях восходящего инфицирования (41,18%) отмечалась клиника пневмонии (17,6%), энтероколита (11,8%), поражения кожи и слизистых оболочек, такие как омфалит, конъюнктивит, везикулез различной степени выраженности встречались в 70,6% случаев. У 29,4% новорожденных имелось сочетание нескольких инфекционных очагов. Генерализованная инфекция наблюдалась
в двух случаях у недоношенных. Анализ видового состава микроорганизмов, полученных при культуральном исследовании мазков из зева у новорожденных с диагностированной внутриутробной пневмонией, показал преобладание гемолитического эпидермального стафилококка и гемолитического энтерококка, причем в двух случаях выявлен массивный рост, а у одного новорожден-ного установлена хламидийная моноинфекция. У одного ребенка с энтероколитом определена микоплазменная инфекция. В другом случае определен массивный рост пиогенного стрептококка. Состав выявляемой микрофлоры у новорожденного совпадал с микробным пейзажем
вагинального отделяемого матери. Необходимо отметить, что в случае бактериальной этиологии
ВУИ у всех матерей в той или иной степени выявлялись нарушения видового состава вагинальной
микрофлоры на момент данной беременности, а в анамнезе женщин имелись неоднократные курсы
лечения воспалительных заболеваний нижнего отдела репродуктивной системы.
Во 2-й подгруппе показатель недоношенных детей составил 12,5%. У 69% новорожденных данной подгруппы имела место клиника гипоксически-ишемического поражения ЦНС в виде синдрома угнетения или возбуждения, в 34% имело место сочетание гипоксического и токсико-метаболического поражений ЦНС (никотин), что проявлялось в виде синдрома угнетения.
Одним из главных условий профилактики и лечения ВУИ, вызванных бактериальной флорой и возникших вследствие восходящего инфицирования, является своевременная диагностика нарушения микробиоценоза гениталий и их адекватная терапия [7]. Однако часть инфекционных процессов реализуется через факторы ПН [6,11]. При гематогенном инфицировании, перед проникновением в организм плода возбудитель, нарушая плацентарный барьер, приводит, в первую очередь, к развитию хорионита (плацентита) с последующим формированием ПН, клинически проявляющейся хронической гипоксией плода и задержкой его внутриутробного роста [2]. Для гематогенного пути инфицирования характерно преобладание васкулитов плацентарного ложа матки, с последующим развитием интервиллузита, васкулитов хориальной пластинки. Если блокировать инфекционный процесс на этом этапе, то можно не только предупредить развитие ВУИ, но и таких его осложнений как ПН. С этой целью, помимо этиотропной, необходимо проводить метаболическую терапию, которая способствует
поддержанию компенсаторно-приспособительных механизмов и стабилизации имеющегося патологического процесса. Учитывая тот факт, что реализация инфекционного процесса определяется патогенностью инфекционного агента и эффективностью защитных механизмов организма, помимо метаболической терапии целесообразно использовать иммуно-корригирующие
препараты [3, 5, 8, 10]. В настоящее время антибактериальные, противовирусные препараты,
применяются очень широко и в большинстве случаев без показаний. Окончательный диагноз ВУИ внутриутробно может быть поставлен только при обнаружении специфического иммунного ответа у плода или выявления у него возбудителя с помощью инвазивных методов диагностики, однако использование данных методов обследования весьма ограничено в связи с наличием противопоказаний к их проведению и небезопасностью использования. В связи с этим была предложена схема ведения беременных группы риска ВУИ в соответствии с разработанной прогностической таблицей (см. рисунок).
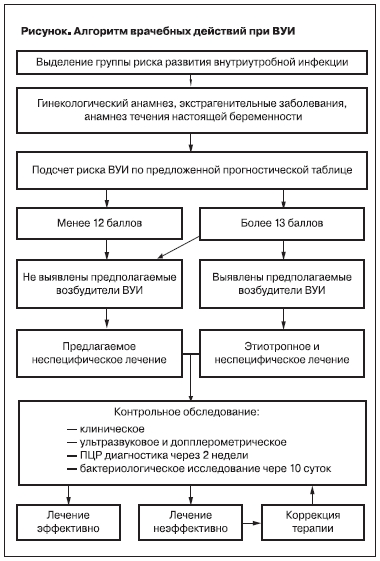
При выявлении риска тяжелой степени (более 13 баллов) необходимо провести расширенный спектр лабораторных исследований для верификации наличия возможных патогенов. Лабораторные исследования должны включать:
1) вирусологический метод: материалом служит кровь, выделения из цервикального канала, слюна, моча, при необходимости амниотическая жидкость;
2) бактериоскопическое исследование нативных и окрашенных мазков из уретры, цервикального канала и влагалища;
3) бактериологическое исследование с посевом содержимого цервикального канала, уретры и влагалища;
4) сероиммунологический метод;
5) ПЦР для идентификации ДНК возбудителей (кровь, моча, отделяемое из цервикального канала, амниотическая жидкость).
С учетом возможной гипердиагностики, вирусная инфекция должна быть верифицирована
не менее чем двумя методами.
При идентификации возбудителя необходимо проведение этиотропной терапии (противовирусной и/или антибактериальной) параллельно с иммунокоррекцией, санацией влагалища и лечением/профилактикой ПН. При высоком риске ВУИ (более 13 баллов) и отсутствии возбудителей проводится только лечение/профилактика ПН.
Для оценки эффективности разработанного алгоритма были обследованы 53 беременные с признаками ВУИ по результатам ультразвукового исследования (не менее 3 маркеров). Все пациентки были разделены на 2 группы путем последовательного рандомизированного отбора (при помощи таблицы случайных чисел):
1-я группа (n=27) пациенток, получала в соответствии со стандартами антибактериальную и неспецифическую терапию, направленную на улучшение функции маточно-плацентарного
комплекса. 2-я группа пациенток (n=26) получала лечение, согласно разработанному алгоритму врачебных действий. Контрольную группу составили 49 пациенток без признаков ВУИ, сопоставимые
по возрасту и другим дополнительным данным.
Выделенные группы были проверены на однородность. При оценке степени риска ВУИ пациентки 1-й и 2-й групп были однородны, в то время как с контрольной группой они имели значимые различия. Для группы контроля данный показатель находился в пределах низкого риска ВУИ: -19,0 баллов (-25,0– -10,0), а в группах сравнения он в среднем соответствовал высокому риску ВУИ и составлял для 1-й и 2-й групп соответственно: 12,0 (1,0–31,0, р=0,00) и 14,0 (5,0–22,0, р=0,00) баллов. По анамнестическим показателям 1-я, 2-я и контрольная группы были однородны (р>0,017). Результаты проверки сравниваемых групп на однородность по наличию проявлений инфекционных процессов во время беременности показали значимые различия между контрольной группой и пациентками с наличием риска ВУИ, в то время как 1-я и 2-я группы достоверных различий не имели. Проверка сравниваемых групп на однородность по наличию маркеров ВУИ по УЗИ также отмечала наличие достоверных различий между группой контроля и двумя основными, при этом между собой 1-я и 2-я группы значимых различий не имели. По результатам обнаружения инфекционных агентов 1-я и 2-я группы были однородны (р>0,017).
В 1-й группе этиотропную терапию получали все пациентки. Во 2-й группе этиотропное лечение
было назначено только 57,7±9,69% пациенткам, имеющим высокий риск ВУИ (более +13 баллов)
при наличии идентифицированного возбудителя. Остальные пациентки получали только неспецифическую терапию, направленную на улучшение функции маточно-плацентарного комплекса.
Различия в частоте применения этиотропного лечения между сравниваемыми группами были статистически значимы (р=0,001).
При подтверждении герпетической инфекции проводилось противовирусное лечение человеческим иммуноглобулином по 25 мл внутривенно через день 3 раза. При выявлении урогенитального хламидиоза, микоплазмы, уреаплазмы лечение проводилось с использованием макролидов джозамицина (500 мг 3 раза в сут в течении 7–10 дней) или спирамицина (по 3 000 000 МЕ 3 раза в сут
в течении 7–10 дней) [1, 5].
При наличии изменений влагалищной флоры использовалась местная форма клиндамицина в виде 2%-ного вагинального крема (ежедневное однократное введение 7 г крема в течение 3 дней)
с обязательным применением на втором этапе препаратов эубиотиков: живых лиофилизированных лактобацилл (Ацилакт) по 1 свече 2 раза в сут в течение 10 дней [1].
При изолированном нарушении плодово-плацентарного кровотока назначали актовегин (200 мг 3 раза в сут в течение 3 нед) или 5 мл внутривенно капельно в 200 мл 0,9%-ного раствора натрия хлорида (10 раз) [4]. При наличии гемодинамических нарушений в системе мать-плацентаплод во II триместре назначали аспирин (250 мг через сут в течение 3 нед), во II и III триместрах – дипиридамол (курантил по 75 мг внутрь 3 раза в сут).
Эффективность разработанного алгоритма врачебных действий оценивалась по результатам течения беременности и родов, в том числе – оценке состояния новорожденного по шкале Апгар, а также на основании выявления или отсутствия инфекционных возбудителей у новорожденного и в тканях плаценты.
После проведенного лечения по результатам течения беременности и родов 1-я и 2-я группы различий не имели (р>0,017). Значимые различия выявлялись между контрольной группой и пациентками двух основных групп по частоте диагностики ПН: в 1-й и 2-й группах соответственно 66,7±9,07, и 76,9±8,27%, в группе контроля – 20,4±5,76% (р=0,000) (табл. 2).
При исследовании новорожденного на наличие ВУИ после проведенного лечения во время беременности 1-я и 2-я группы значимых различий не имели (р>0,017). Значимые различия между
контрольной группой и пациентками 1-й и 2-й групп были по частоте выявления морфологических признаков воспаления плаценты: в 1-й группе морфологические признаки воспаления встречались в 37,0±9,29%, во 2-й – 34,6±9,33%, в контрольной – 0,0±0,00% (р=0,000) .
Таблица 2. Оценка состояния новорожденного и наличия осложнений течения беременности
у пациенток, получавших лечение (U-критерий Манна-Уитни, χ2 с поправкой Йетса, точный критерий Фишера)
Таким образом, эффективность проведенного лечения классическим способом и по предложенному алгоритму была одинаковой. Следовательно, предложенный алгоритм ведения женщин с риском ВУИ обладает бóльшей приемлемостью и комплаентностью, так как этиотропная терапия назначается только в случае высокого риска инфицирования плода (более 13 баллов) и при идентификации возбудителя, что уменьшает медикаментозную нагрузку у женщин со средним и низким риском ВУИ.
Кроме того, фармакоэкономическая эффективность разработанного алгоритма проявляется в более низкой стоимости лечения (выборочное назначение этиотропной терапии) при одинаковой эффективности.



