Преждевременные роды входят в группу больших акушерских синдромов, что обусловлено не только общностью патогенетических механизмов, но и удельным весом в структуре перинатальной заболеваемости и смертности [1, 2]. Среди первоочередных мероприятий, направленных на снижение частоты преждевременных родов, большую роль играет токолитическая терапия. В настоящее время показано, что пролонгирование беременности с помощью токолиза наиболее эффективно на 48 часов. Это время позволяет провести профилактику синдрома дыхательных расстройств глюкокортикоидами и перевести беременную в перинатальный центр для оказания специализированной помощи недоношенному новорожденному [3].
В течение последних лет наблюдается постепенная смена приоритетов в применении токолитических препаратов и в большинстве стран гексопреналин и сернокислая магнезия заменены на блокатор окситоциновых рецепторов атозибан и блокатор кальциевых каналов нифедипин [4, 5].
Данная смена обусловлена высокой частотой побочных эффектов при использовании гексопреналина и неэффективностью сернокислой магнезии [6, 7].
В то же время остается невыясненным, какой из применяемых в настоящее время токолитиков имеет преимущества при ведении беременных с угрожающими преждевременными родами.
Последнее мультицентровое исследование APOSTEL III не обнаружило существенных различий в материнских и перинатальных исходах между группами женщин, получавших лечение нифедипином или атозибаном [8, 9].
Тем не менее, результаты исследования противоречивы. Так, имелась тенденция к более высокому уровню перинатальной смертности в группе нифедипина, которая не соответствовала подтвержденным данным частоты сепсиса. Напротив, частота бронхопульмональной дисплазии имела тенденцию к повышению в группе атозибана. При отсутствии различий в продолжительности пролонгирования беременности в целом после исключения беременных с преждевременным излитием вод период пролонгирования беременности на фоне применения нифедипина оказался в среднем на 10 дней больше, но это не сочеталось с улучшением перинатальных исходов.
Полученные авторами результаты не выявили различий в частоте побочных реакций. Однако в другом крупном когортном исследовании была показана более высокая частота гипотензии и тахикардии при использовании для токолиза нифедипина [10].
В связи вышеизложенным по-прежнему представляет научный и практический интерес сравнение эффективности и безопасности наиболее часто применяемых токолитиков – нифедипина и атозибана, что и стало целью данного исследования.
Материал и методы исследования
В исследование включены 111 беременных с угрожающими преждевременными родами в сроке беременности от 28 до 34 недель.
Критериями включения в исследование служили: удовлетворительное состояние беременной и плода, целый плодный пузырь, срок беременности 24–33 недели 6 дней, зарегистрированная сократительная деятельность матки (четыре и более схваток за 30 минут продолжительностью не менее 30–40 сек), раскрытие шейки матки от 1 до 3 см и укорочение на 75% от исходной величины, информированное согласие пациентки
Критериями исключения из исследования были: тяжелые состояния беременной, требующие родоразрешения в экстренном порядке (преждевременная отслойка нормально расположенной плаценты, тяжелая преэклампсия, эклампсия и др.); дистресс плода; врожденные пороки развития плода или плаценты; антенатальная гибель плода; хориоамнионит или другой острый инфекционный процесс; повышенная чувствительность к нифедипину или атозибану.
Токолитическую терапию начинали сразу после установления диагноза, уточнения срока беременности, оценки состояния матери и плода, критериев включения/исключения, оценки противопоказаний к применению препарата. В 54 наблюдениях проведен токолиз нифедипином, в 57 – атозибаном.
Схема токолиза нифедипином:
- 20 мг per os; далее – если сокращения матки сохраняются – через 30 мин 20 мг повторно, затем по 20 мг каждые 3–8 ч в течение 48 часов по показаниям;
- или 10 мг сублингвально, затем, при необходимости, каждые 20 мин по 10 мг (максимальная доза в течение первого часа 40 мг), затем каждые 4 часа по 20 мг до 48 часов. Максимальная доза 160 мг/сут.
Продолжительность токолиза – 48 часов.
Схема токолиза атозибаном:
1-й этап – внутривенно медленно (в течение 1 минуты) вводили 0,9 мл (1 флакон) атозибана без разведения (начальная доза 6,75 мг);
2-й этап – в течение 3 часов проводили инфузию атозибана в дозе 300 мкг/мин (доза атозибана 18 мг/час);
3-й этап – продолжительная до 45 часов инфузия атозибана в дозе 100 мкг/мин (доза атозибана 6 мг/час).
Общая продолжительность лечения не превышала 48 часов. Максимальная доза атозибана на весь курс составляла 330 мг.
Степень эффективности токолиза определяли по длительности пролонгирования беременности (48 часов, 7 суток, более 14 суток).

При оценке эффективности токолитической терапии также учитывали субъективную оценку самочувствия пациенткой в течение первых 3 часов, через 24 и 48 часов лечения. Для этого использовали шкалу самооценки («самочувствие ухудшилось», «не изменилось», «незначительно улучшилось», «значительно улучшилось», «ничего не беспокоит»).
Для объективной оценки эффективности токолитической терапии использовали клиническую оценку тонуса матки при пальпации, определение частоты и длительности схваток, характер и частоту сердечных сокращений плода по данным кардиотокографии, динамический контроль состояния шейки матки – через 2 часа и 48 часов от начала лечения с помощью эхографической цервикометрии.
Проводили клиническую оценку новорожденных по общепринятым критериям.
Статистический анализ полученных результатов проведен с помощью статистической программы SPSS Statistics v19.
Исследование проведено в рамках научно-исследовательской работы «Разработка клинических рекомендаций по ведению и диагностике невынашивания беременности и преждевременных родов», одобренной Этическим комитетом ФГБУ НМИЦ АГП.
Результаты исследования
Сравниваемые группы беременных не отличались по возрасту (табл. 1). Однако частота заболеваний сердечно-сосудистой системы была выше у женщин группы атозибана за счет пациенток с тахиаритмией (n=5), тогда как в группе нифедипина не было наблюдений пациенток с данной патологией. Также в группе атозибана достоверно чаще встречался пиелонефрит, 6 против 16 наблюдений. В то же время анемия беременных и тромбофилические мутации генов низкого риска несколько чаще встречались у женщин группы нифедипина (4 и 8 наблюдений соответственно), чем атозибана (2 и 3 наблюдения соответственно).
Среди гинекологических заболеваний наиболее часто встречались эндометриоз (7,41 и 7,02%) и миома матки (7,41 и 8,8%). Вследствие более высокой частоты бесплодия в анамнезе общая частота гинекологических заболеваний оказалась выше в группе атозибана (табл. 1).
В обеих группах преобладали первородящие (51,85 и 64,91%). Количество женщин с абортами в анамнезе составляло в группе нифедипина 13 (24,07%), атозибана – 3 (3,51%) (p<0,05). Самопроизвольное прерывание беременности на ранних сроках встречалось в обеих группах в 22,6% наблюдений. По два выкидыша отмечено в 12,96 и 10,53% наблюдений соответственно. Преждевременные роды в анамнезе были в 29,6 и 15,8% (p>0,05).
В 11,11 и 21,05% соответственно данная беременность наступила в результате применения вспомогательных репродуктивных технологий (p>0,05). В группе женщин, получавших лечение нифедипином, было 2 дихориальные диамниотические двойни. В группе атозибана дихориальных диамниотических двоен было 7, дихориальных моноамниотических – 3, монохориальных – 2. Таким образом, частота многоплодия была выше в группе атозибана.
С одинаковой частотой в группах встречались женщины с рубцом на матке после предшествующей операции кесарева сечения (11,1 и 10,5%).
Течение беременности на ранних сроках у женщин обеих групп характеризовалось высокой частотой угрожающего прерывания беременности, по поводу чего они получали лечение в стационаре (табл. 2). С высокой частотой встречалась истмико-цервикальная недостаточность, в связи с которой в сроках 18–21 неделя беременности было проведено наложение швов на шейку матки. Из других осложнений беременности наиболее часто отмечены анемия беременных, а также задержка роста плода (по 18,5 и 14,0%; 3,7 и 14,0% наблюдений). Значимых различий в частоте осложнений беременности между группами не было.
Срок беременности на момент госпитализации колебался от 28 до 34 недель и в группе нифедипина был в среднем на 7 дней больше, чем у беременных группы атозибана – 32,81±1,16 нед. (30–34 недели) против 31,02±1,44 нед. (28–33 недели) (p<0,001). При поступлении в стационар длина шейки матки по данным эхографической цервикометрии у женщин в группе нифедипина колебалась от 2,0 до 2,8 см, составляя в среднем 2,51±0,26 см, в группе атозибана – от 0,7 до 2,8 см, в среднем – 2,36±0,49 см (p<0,05).
Зрелость шейки матки по модифицированной шкале Бишоп находилась в пределах от 4 до 9 баллов. У беременных, получавших нифедипин, оценка степени ее зрелости по шкале Бишоп составляла 5,04±0,21 против 5,35±0,87 в группе атозибана (p<0,05). В группе токолиза нифедипином чаще встречались беременные, которые уже получали лечение утрожестаном, тогда как в группе токолиза атозибаном чаще встречались женщины, которые получали лечение нифедипином. Указанное лечение было отменено с началом токолиза.
 Других различий между группами не было выявлено.
Других различий между группами не было выявлено.
Всем беременным после установления диагноза угрожающих преждевременных родов была начата профилактика респираторного дистресс синдрома плода дексаметазоном в курсовой дозе 24 мг и проведена токолитическая терапия в соответствии с вышеприведенной схемой.
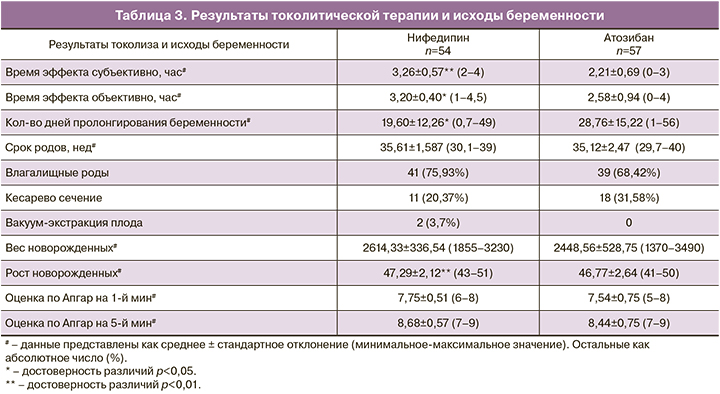
Основные результаты проведенной терапии и исходы беременности представлены в табл. 3.
Как следует из представленных результатов, время, требуемое для достижения клинического эффекта, значимо различалось между группами. В группе женщин, получавших лечение атозибаном, отчетливый эффект, субъективно определяемый пациенткой и объективно – по данным мониторного контроля, наступал раньше, чем в группе нифедипина (табл. 3).
При этом неэффективным лечение признано в 8 (14,81%) наблюдениях группы нифедипина и в 2 (3,51) атозибана (p<0,05). У этих женщин, несмотря на токолитическую терапию, прогрессировали схватки и раскрытие шейки матки, что определило необходимость отмены токолитической терапии с последующим родоразрешением в течение первых 24 часов от госпитализации.
У 46 женщин, получавших лечение нифедипином (85,19%), и 55 атозибаном (96,49%) беременность удалось пролонгировать на срок более 48 часов (p<0,05). При этом еще у 5 женщин из группы нифедипина и 11 атозибана удалось пролонгировать беременность на срок более 7 дней, и у 41 и 44 женщин, соответственно, на срок более 14 дней (p>0,05).
В доношенном сроке беременности роды произошли у 15 женщин (27,8%) после токолиза нифедипином и у 19 (33,3%) атозибаном (p>0,05%). В среднем токолиз атозибаном позволил пролонгировать беременность на 9,2 дня больше, чем нифедипином (p<0,05).
Сведения о продолжительности пролонгирования беременности в группах представлены на рисунке.
В обеих группах преобладал мужской пол плода, 64,8% и 77,2% (p>0,05). Не было получено существенных различий в массе тела новорожденных сравниваемых групп, тогда как рост плода оказался достоверно больше в группе токолиза нифедипином (p<0,01). Оценка новорожденных по шкале Апгар на 1-й минуте колебалась от 5 до 8 баллов и существенно не различалась в группах (табл. 3).
Следует отметить, что в группе атозибана в двух наблюдениях был проведен полный повторный курс терапии в течение 24 часов.
В 50,0% наблюдений после окончания токолиза нифедипином и в 42,1% после токолиза атозибаном была назначена поддерживающая терапия микронизированным прогестероном (утрожестан) по 200 мг/сутки (на ночь). Еще 19 (35,1%) и 4 (7,0%) женщин, соответственно, получали поддерживающую терапию сернокислой магнезией (p>0,05).
При лечении нифедипином у пациенток отмечалась тахикардия – у 9 (16,67%), гипотензия – у 9 (16,67%), головокружение – у 8 (14,81%).
В 8 (14,8%) наблюдениях в связи с сочетанием тахикардии, гипотензии и жалоб на слабость, тошноту и рвоту протокол токолиза нифедипином не был выполнен полностью в связи с необходимостью снижения дозы или увеличения интервала приема препарата. Следует отметить, что именно в этой подгруппе женщин имела место наиболее высокая частота неэффективности токолиза – 5 из 8 женщин этой подгруппы родили в течение первых 24 часов от момента поступления.
В группе женщин, получавших лечение атозибаном, частота побочных эффектов была значительно ниже (1,75% против 48,15%) (p<0,05). Не было наблюдений непереносимости лечебного препарата, и протокол токолиза был соблюден у всех пациенток.
После исключения из анализа 8 женщин, у которых не был выполнен протокол токолиза нифедипином в связи с непереносимостью препарата, частота пролонгирования беременности на срок более 48 часов составила 93,48%, 7 суток – 84,78% и 14 дней – 28,26%, что значимо не отличалось от результатов токолиза в группе атозибана.
Учитывая достоверно более высокую частоту многоплодия у женщин в группе токолиза атозибаном, мы провели оценку эффективности терапии среди пациенток с одноплодной беременностью. После исключения беременных с многоплодной беременностью в группе нифедипина осталось 52 женщины, атозибана – 45 женщин.
Как показал проведенный анализ, пролонгировать одноплодную беременность при угрозе преждевременных родов на срок 48 часов удалось у 88,46% женщин в группе нифедипина и 95,56% – атозибана (p>0,05); более 7 дней – у 78,84 и 86,87% соответственно. Также не получено достоверных отличий в частоте родов в доношенном сроке беременности – 28,85 и 35,55%. Однако по-прежнему количество дней пролонгирования беременности было достоверно больше в группе атозибана – 29,37±14,95 суток против 20,30±11,95 суток в группе нифедипина (p<0,01).
Обсуждение
Общая частота родов в доношенном сроке беременности существенно не различалась между группами, что вновь подтверждает отсутствие значимого эффекта токолиза на снижение частоты преждевременных родов в целом [8, 9, 11]. Тем не менее, несмотря на то, что по ряду важных показателей (количество женщин с экстрагенитальной патологией, длина шейки матки при цервикометрии и зрелость по шкале Бишоп, частота многоплодной беременности) группа нифедипина имела преимущество перед группой атозибана, блокатор кальциевых каналов уступил в эффективности пролонгирования беременности на 48 часов блокатору рецепторов окситоцина.
Индивидуальный анализ данных показал, что более высокая частота неудачи терапии нифедипином была обусловлена его плохой переносимостью, из-за чего 14,81% пациенток были вынуждены снизить дозу и/или увеличить интервал приема препарата. Именно в этой подгруппе пациенток имела место наиболее высокая частота неуспеха токолиза. При исключении женщин с невыполненным протоколом из анализа, различий между группами в частоте пролонгирования беременности на 48 часов не зафиксировано. Однако количество дней пролонгирования беременности в среднем было на 9 дней больше в группе атозибана (p<0,01).
Атозибан показал хороший профиль безопасности. В этой группе не было наблюдений невыполненного протокола токолиза. При этом эффект наступал достоверно раньше и сохранялся на более продолжительный период, что, вероятно, обусловлено более надежным выключением патогенетического механизма, запускающего и поддерживающего родовую деятельность.
В нашем исследовании группы исходно различались по количеству многоплодных беременностей. В связи с этим представляет интерес результат анализа, проведенного в группах после их исключения. Сравнительный анализ токолиза у 52 женщин с одноплодной беременностью в группе нифедипина и 45 атозибана не обнаружил различий в частоте пролонгирования беременности на 48 часов, хотя имелась тенденция более высокой эффективности атозибана (88,46% против 95,56%). При этом по-прежнему количество дней пролонгирования беременности было выше в группе атозибана. К сожалению, малое число наблюдений не позволило провести сравнительный анализ эффективности токолиза при многоплодной беременности.
Заключение
Таким образом, нифедипин и атозибан могут конкурировать по эффективности торможения преждевременных родов на 48 часов. Однако худшая переносимость нифедипина ограничивает возможность его применения. Атозибан имеет также преимущества в продолжительности пролонгирования беременности. Следует продолжить исследования для уточнения эффективности и безопасности этих препаратов при угрозе прерывания многоплодной беременности.



