Задержка роста плода (ЗРП) относится к группе больших акушерских синдромов, выявляется в 10% случаев беременностей в общей популяции и занимает одно из ведущих мест в структуре перинатальной заболеваемости и смертности [1, 2]. Основной задачей является выявление групп беременных с ЗРП для того, чтобы разработать метод, позволяющий прогнозировать и своевременно диагностировать данное осложнение [1, 3].
Особое значение в развитии беременности и полноценном росте плода отводится плацентарному барьеру, основной задачей которого является регулирование проникновения различных веществ из крови матери в кровь плода и обратно. Плацентарный барьер состоит из клеток трофобласта и синцития, покрывающего ворсинки хориона плаценты, ткани стромы ворсинок и эндотелия их капилляров, которые обеспечивают нормальное функционирование системы «мать-плацента-плод» [4].
Растворимая форма Е-кадгерина (sE-cad) и фактор роста кератиноцитов (KGF) являются митогенами, которые регулируют миграцию и дифференцировку эпителиальных клеток [5, 6]. Основной мишенью данных факторов в плаценте являются рецепторы клеток трофобласта. Кроме того, sE-cad способен взаимодействовать с E-кадгеринами, образующими межклеточные контакты, нарушая адгезивные соединения. Таким образом, от sE-cad и KGF зависят целостность и площадь поверхности плацентарного барьера. Ранее было установлено, что в плаценте уровень sE-cad снижен при ЗРП, что является возможной причиной низкой пролиферации и апоптоза клеток трофобласта, приводящих к ЗРП [7]. sE-cad и KGF активно экспрессируются в плаценте, которая может быть основным источником данных факторов в плазме крови. Вышеизложенное свидетельствует о том, что определение указанных факторов может иметь диагностическую ценность при синдроме ЗРП.
Цель – определить содержание sE-cad и KGF в плазме крови и оценить их диагностическую значимость при ЗРП.
Материалы и методы
В исследование включены 44 беременные, которые были родоразрешены в ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России. Пациентки были разделены на две группы – основная и контрольная. Основную группу составили 25 беременных с диагнозом ЗРП, подтвержденным после рождения ребенка; контрольную группу – 19 женщин с физиологически протекающей беременностью. Данное исследование было одобрено локальным этическим комитетом. Все женщины были ознакомлены с целью, задачами исследования и подписали информированное согласие на участие в нем. Критериями включения в исследование являлись: одноплодная беременность, родоразрешение в сроке 36–40 недель, ЗРП на сроке гестации с 34–40 недель (для основной группы). Критерии исключения: преэклампсия, тяжелая экстрагенитальная патология, многоплодная беременность, пороки развития плода, острые инфекционные заболевания матери.
Исследование проводили с использованием коммерческих наборов human E-Cadherin ELISA Kit, Cusabio (США) и human КGF-7 (KGF) ELISA Kit, Thermo scientific (США). Забор крови проводили перед родоразрешением в вакутейнеры, содержащие этилендиаминтетраацетат (ЭДТА). Плазма была выделена центрифугированием в течение часа после забора в два этапа при 4°С: первый – 10 минут при 200 g, второй – 10 минут при 4500 g. Образцы плазмы хранили при температуре –80°С. Непосредственно перед работой образцы плазмы крови размораживали при комнатной температуре. Иммуноферментный анализ проводили в соответствии с рекомендациями фирмы-производителя.
Статистический анализ
Полученные результаты не имели нормального распределения, и для их описания была использована непараметрическая статистика. Результаты представлены в виде медианы, верхней и нижней квартили Me (Q1;Q3). Статистическая значимость различий определялась с помощью непараметрического критерия Манна–Уитни. Сравнение групп по качественным признакам проводилось с помощью точного критерия Фишера. Различия считали статистически значимыми при p<0,05. Для определения диагностической эффективности исследуемой модели использовался ROC-анализ. Данные ROC-анализа представлены в виде площади под кривой с 95% доверительным интервалом. Для статистической обработки результатов и построения графиков использовались программы Attestat (Россия) и OriginPro 8.5 (USA).
Результаты
Основные клинические данные, особенности и исходы беременностей исследуемых женщин представлены в таблице.
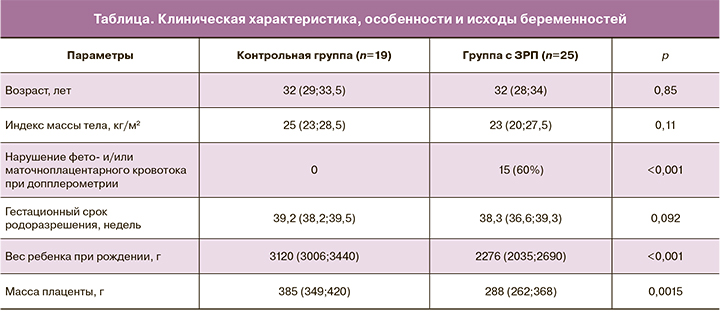
Как видно из данных, представленных в таблице, группы пациентов не различались по возрасту, индексу массы тела и сроку родоразрешения. Обращает на себя внимание, что в группе с ЗРП только в 60% случаев антенатально диагностировались нарушения фето- и/или маточноплацентарного кровотока по данным допплерометрии, а также имела место достоверно низкая масса плацент (р<0,001).
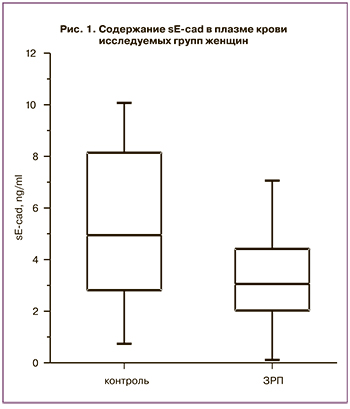 Исследование содержания sE-cad в плазме крови женщин показало, что в основной группе данный показатель был снижен (p=0,006) (рис. 1).
Исследование содержания sE-cad в плазме крови женщин показало, что в основной группе данный показатель был снижен (p=0,006) (рис. 1).
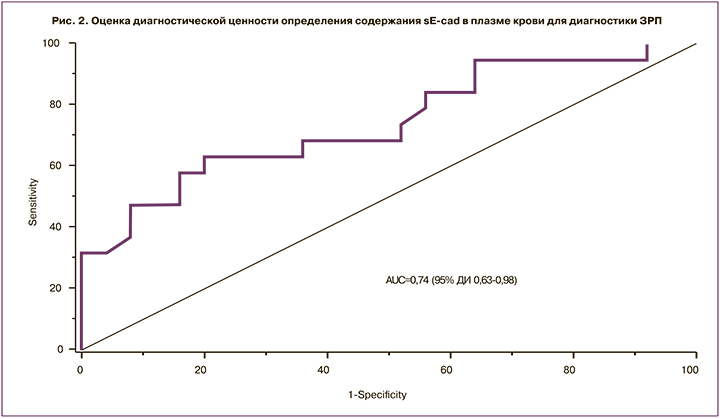
Результаты для контрольной группы составили 4,9 (2,8; 6,3) нг/мл, для основной группы – 3,1 (2,0; 3,9) нг/мл. ROC-анализ показал хорошую диагностическую ценность: AUC=0,74 (95% ДИ 0,63–0,98), чувствительность – 63%, специфичность – 80%, прогностическая ценность положительного и отрицательного результатов – 74,1% и 70,6% соответственно, оптимальный порог составил 4,6 нг/мл (рис. 2).
Исследование содержания KGF в плазме крови женщин показало, что в основной группе данный показатель был повышен (p=0,037) (рис. 3).
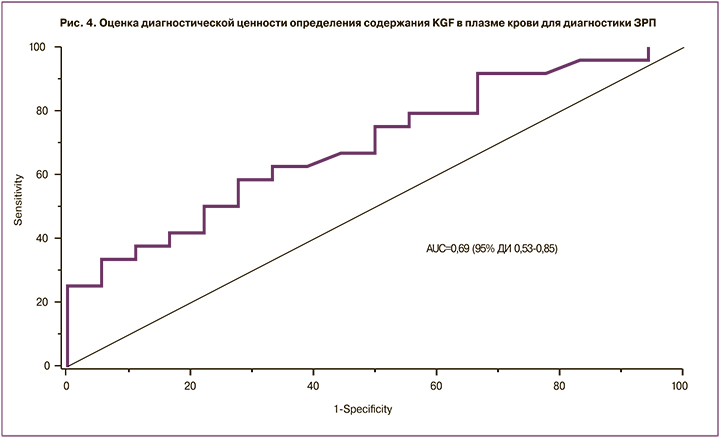
Результаты для контрольной группы составили 0,13 (0,11;0,15) нг/мл; для основной – 0,15 (0,12;5,78) нг/мл. ROC-анализ показал среднюю диагностическую ценность: AUC=0,69 (95% ДИ 0,53–0,85), чувствительность – 58%, специфичность – 72%, прогностическая ценность положительного и отрицательного результатов – 70% и 54,2% соответственно, оптимальный порог составил 0,15 нг/мл (рис. 4).

Обсуждение
По литературным данным, ЗРП, как правило, характеризуется сниженным фето- и/или маточноплацентарным кровотоками [1, 3, 4]. Однако эти данные разноречивы. Исходя из вышеизложенного, необходим поиск наиболее значимых диагностических маркеров ЗРП.
Одной из причин плацентарной недостаточности является медленное развитие хориона плаценты, что отражается в меньших размерах плаценты, показанных в нашем исследовании. Предполагается, что данные процессы происходят под влиянием фактора роста эндотелия сосудов, вазоконстрикторов и вазодилататоров [8]. В данной работе мы исследовали факторы, которые определяют рост клеток трофобласта плаценты, формирующих плацентарный барьер. Без нормального развития клеток плацентарного барьера невозможно формирование сосудов плаценты. Исследованные факторы (sE-cad и KGF) определяют пролиферацию, дифференцировку и миграцию клеток трофобласта в плаценте. Обнаруженное снижение содержания sE-cad в плазме крови при ЗРП соотносится с более низким уровнем sE-cad в плацентах женщин с данным синдромом [7]. Известно, что недостаточный уровень sE-cad в эпителиальных клетках приводит к снижению пролиферации и подвижности, дифференцировки и апоптозу эпителиальных клеток [9]. Полученные результаты позволяют предположить, что недостаток sE-cad может быть причиной медленного развития хориона плаценты, в результате чего формируется ЗРП. ROC-анализ показал хорошую диагностическую ценность содержания sE-cad в плазме крови, что отражает происходящие процессы в плаценте и может быть использовано для диагностики ЗРП. В данном исследовании было обнаружено увеличение содержания KGF в крови беременных с ЗРП. Повышенный уровень KGF как фактора пролиферации может свидетельствовать об активации компенсаторных механизмов, направленных на усиление пролиферации клеток трофобласта плаценты. ROC-анализ показал хорошую диагностическую ценность содержания в плазме крови sE-cad и удовлетворительную для KGF. Следовательно, для диагностики ЗРП наиболее подходящим из исследуемых факторов является sE-cad или сочетанное определение sE-cad и KGF.
Заключение
Таким образом, изучение уровней растворимой формы Е-кадгерина и KGF в плазме крови беременных может отражать патологические процессы, происходящие в плаценте, что может быть использовано для своевременной диагностики ЗРП.
Работа выполнена с поддержкой государственного задания «Изучение диагностической и прогностической роли молекулярно-генетических и иммунологических факторов в синдроме задержки роста плода».



