Нарушение иннервации мышц тазового дна может быть обусловлено, прежде всего, нейропатией полового нерва, который является «королем промежности» [1]. В литературных источниках при описании проблем иннервации тазовых органов используется огромное количество терминов: «пудендальная нейропатия», «пудендальная невралгия», «синдром канала полового нерва», «синдром канала Алькока», «синдром компрессии полового нерва», «тоннельная пудендопатия», «интерлигаментарная пудендоневропатия», «подгрушевидно-остистая пудендонейропатия». Нейропатия полового нерва может проявляться как болевым синдромом в дерматомах, иннервируемых половым нервом, так и выпадением чувствительности, нарушением функций держания и эвакуации кишечного содержимого и мочи, половыми дисфункциями.
В то же время, учитывая полиморфность этиопатогенетических факторов, вызывающих хронический тазовый болевой синдром, на наш взгляд, для более точного определения нейрогенного генеза боли правильнее использовать термин «хронический нейрогенный тазовый болевой синдром» [2, 3]. Впервые нейрогенный характер хронической тазовой боли описали J. Boisson et al. [4] и M.E. Neil и H.M. Swash [5]. R.A. Shmidt [6] выделяет две основные причины хронической нейрогенной тазовой боли – миофасциальный болевой синдром и компрессия полового нерва. Диагноз «нейрогенный тазовый болевой синдром» является диагнозом исключения, при котором все другие воспалительные и органические причины тазовой боли будут исключены.
В колопроктологической литературе последних лет хроническую тазовую боль стали рассматривать как производное функциональных нарушений и топографо-анатомических взаимоотношений мышечно-связочного аппарата тазового дна и органов малого таза. «Синдром опущения промежности», «слабость тазового дна», «синдром спастического тазового дна» – эти синдромы включают в себя не только сочетанные нарушения функций дефекации, мочеиспускания, пролапса тазовых органов, но и в большинстве своем хроническую боль в области промежности во время натуживания или после продолжительного стояния [7].
Рассмотрим в отдельности каждую из возможных причин в патогенезе хронической нейрогенной тазовой боли. С точки зрения Р.Е. Baldry [8], при миофасциальном болевом синдроме в патологический процесс включаются различные мышцы тазового дна с образованием в них триггерных точек [9–15]. Триггерные точки представляют собой нейрофибромиотонические участки – «узелки» в мышечной ткани. Они образуются вокруг окончания нервного волокна и пальпируются, как напряженные узелки. Пациенты обычно очень четко определяют их локализацию. Характерной особенностью является то, что боль локализуется не только в самой триггерной точке, но и иррадиирует в различные области – в промежность, половые органы, перианальную область, копчик [11].
Второй причиной хронического нейрогенного тазового болевого синдрома является компрессия/натяжение полового нерва [3, 7, 15–19]. Несмотря на многочисленные публикации по изучению нейрогенных причин тазовой боли, алгоритм диагностики для выявления нейрогенных причин тазовой боли до конца не определен. Ряд авторов подчеркивают значимость изучения только латентности М-ответа при стимуляционной электронейромиографии (ЭНМГ) [20], другие – исследования глубокого пудендального (ГПР) и бульбокавернозного рефлексов (БКР) [21, 22], третьи считают проведение ЭНМГ-исследований необязательным [23].
В связи с вышеизложенным целью нашей работы было оценить роль комплексного нейрофизиологического исследования для выявления нейропатии полового нерва у пациентов с болевым синдромом на фоне пролапса тазовых органов.
Материалы и методы
В лаборатории клинической патофизиологии ФГБУ «ГНЦК им. А.Н. Рыжих» Минздрава России в 2019 г. были обследованы 44 женщины, в том числе по направлению из ГБУЗ МО МОНИИАГ, с пролапсом тазовых органов и с болевым синдромом. Пролапс тазовых органов был в виде ректоцеле – у 29/44 (65,9%) (распределение ректоцеле: 1-я степень – 18/29 (62,1%), 2-я степень – 9/29 (31,0%), 3-я степень – 2/29 (6,9%) пациенток) и сочетания ректоцеле и внутренней ректальной инвагинации – у 15/44 (34,1%). Средний возраст больных составил 48,8 (12,2) года. Жалобы на боли в прямой кишке, анусе (с иррадиацией в копчик, в область гениталий и кожу промежности), не связанные с дефекацией, предъявляли все 44 пациентки. При этом болезненность, онемение, парестезии в области гениталий, внутренней поверхности бедра и промежности отмечались у 14/44 (31,8%) женщин; ослабление чувствительности при половом акте и отсутствие оргазмов – у 15/44 (34,1%) пациенток; диспареуния была отмечена в 8/44 (18,2%) случаях. Помимо болевого синдрома, жалобы на недержание компонентов кишечного содержимого (газов и жидкого кала) были у 35/44 (79,5%) пациенток.
Все пациентки были комплексно обследованы в объеме: физикальный осмотр, колоноскопия, дефекография, комплексная сфинктерометрия и комплексное нейрофизиологическое обследование в виде стимуляционной ЭНМГ для изучения латентного периода проведения возбуждения по двигательным нервам (латентность М-ответа), а также ГПР и БКР. Все пациентки были консультированы урологом и гинекологом, а также предоставляли данные магнитно-резонансной томографии пояснично-крестцового отдела позвоночника с целью исключения гинекологической, урологической и нейрохирургической патологий.
Интенсивность болевого синдрома у всех пациенток оценивали по визуальной аналоговой шкале (ВАШ) [23, 24]. Наличие и характер жалоб на недержание кишечного содержимого оценивали в соответствии со Шкалой оценки недержания по Wexner [25].
Для исключения миофасциальных болевых синдромов проводили соответствующие мануальные тесты для определения «синдрома леваторов», «синдрома внутренней обтураторной мышцы», «синдрома грушевидной мышцы», «бульбокавернозного синдрома». Исключались синдром Хаушипа–Ромберга и синдром подвздошно-поясничной мышцы. Для уточнения нейропатии проводилось мануальное тестирование бедренно-полового, подвздошно-подчревного, подвздошно-пахового и седалищного нервов.
Аноректальная манометрия в виде комплексной сфинктерометрии выполнялась по оригинальной методике НМИЦ колопроктологии («Способ оценки функционального состояния запирательного аппарата прямой кишки». Патент №2576445 от 05.12.16). Учитывались среднее давление в анальном канале в покое и максимальное давление при волевом сокращении. Параметры нормы указанных показателей для этого метода составляют: 41–63 и 110–178 мм рт. ст. соответственно [26].
Комплексное нейрофизиологическое исследование выполняли на аппарате «Нейро-ЭМГ-Микро» («Нейрософт», Россия) в виде стимуляционной ЭНМГ для мышц тазового дна с помощью электрода Св. Марка («Способ определения нейрофизиологического состояния мышц тазового дна». Патент №2708052). Вначале проводилась стандартная стимуляционная ЭНМГ для изучения латентного периода проведения возбуждения по дистальным отделам двигательных волокон полового нерва (латентность М-ответа) с нормами для интравагинального использования электрода 1,54–2,55 мс [21]. Далее, при той же локализации электрода, выполнялась регистрация ГПР путем изучения смешанного возвратно-рефлекторного ответа в режиме одиночной стимуляции при субмаксимальном, максимальном и супрамаксимальном стимуле с оценкой латентности ГПР. Норма ГПР – 36,18 (4,29) мс (или в пределах 21–41 мс) [22]. Далее, с помощью того же электрода Св. Марка, который в данном случае использовали как регистрирующий, проводилось изучение БКР с регистрацией ответа с мышц тазового дна с нормами латентности 34,88 (4,29) мс (или в пределах 25–42 мс) [22].
Для статистического анализа данных использовался статистический пакет Stata 14.2 (StataCorp). Форматы описательной статистики представлены следующим образом: для количественных данных, имеющих нормальное распределение, используется формат М (SD), где М – среднее арифметическое, SD – стандартное отклонение; для количественных данных с распределением, отличающимся от нормального, представлены медиана (Me) и квартили первый (Q1) и третий (Q3) в формате Me (Q1; Q3).
Проверка нормальности распределения признака, включая остатки в уравнениях регрессии, осуществляется на основании критерия Шапиро–Уилка (нулевая гипотеза о нормальном распределении). Для определения статистической значимости различий между изучаемыми группами пациенток в работе использовался непараметрический U-критерий Манна–Уитни.
В статье используется корреляционный анализ (коэффициент корреляции Спирмена), при этом результат представлен в виде коэффициента корреляции (r) и верхней и нижней границ доверительного интервала (CI-верх, CI-низ) в формате r (CI-верх; CI-низ).
Также в работе были применены однофакторная и многофакторная линейные регрессии с целью выявления статистически значимых предикторов снижения тонуса по сфинктерометрии. В многофакторной модели мы не использовали процедуру отбора признаков, включая все факторы одновременно. Для оценки возможной мультиколлинеарности использовался фактор, увеличивающий дисперсию (VIF), для оценки возможных выбросов во всех моделях – показатель интерквартильной широты (IQR).
В данной работе мы останавливаемся на 5% уровне значимости для определения значимости различий (р<0,05).
Результаты
Медианный балл по шкале ВАШ составил 5 (1,0;9,8), распределение не будет нормальным (р=0,37). При оценке анальной инконтиненции по шкале оценки недержания по Wexner среднее значение составило 7,5 (5,2) балла, распределение нормальное (р<0,001). По данным комплексной сфинктерометрии, средние показатели давления в анальном канале в покое, свидетельствующие о состоянии тонуса анальных сфинктеров, были снижены до 38,6 (11,4) мм рт. ст. (что было ниже на 5,9% нижней границы физиологических норм). Параметры давления при волевом сокращении, характеризующие сократительную способность анальных сфинктеров, составили 109,7 (39,8) мм рт. ст. (практически на нижней границе возрастной физиологической нормы).
Латентность М-ответа была увеличена у 29/44 (65,9%) пациенток. При этом билатеральное увеличение латентности регистрировалось в 12/29 (41,4%) случаях, монолатеральное – у 17/29 (58,6%) пациенток, из них справа увеличенный ответ регистрировался у 6/17 (35,3%), а слева – у 11/17 (64,7%) женщин. Распределение показателей М-ответа ненормальное. Медианные показатели латентности у всех пациентов составили 2,35 (2,10;2,78) мс справа и 2,60 (2,03;2,70) мс слева.
Нарушение ГПР (увеличение латентности, «деформация» или полное отсутствие ответа) было зарегистрировано у 37/44 (84,1%) больных. Латентность БКР была увеличена в 39/44 (88,6%) случаев, составляя в среднем 53,6 (8,0) мс справа и 55,5 (6,3) мс слева.
Таким образом, больных, у которых был бы увеличен только М-ответ без изменения ГПР и БКР, не было; при этом у 5/29 (17,2%) пациенток М-ответ был увеличен вместе с нарушением ГПР, у других 5/29 (17,2%) было отмечено совместное увеличение латентности М-ответа и латентности БКР. В 15/44 (34,1%) случаев было зарегистрировано увеличение латентности только ГПР или БКР при нормальном М-ответе.
Проведенный статистический анализ с использованием теста Манна–Уитни не показал статистически значимых различий в оценке интенсивности боли по шкале ВАШ между пациентками (р=0,60) с нормальной и увеличенной латентностью М-ответа. Как мы уже отмечали выше, в выборке нет больных, которые бы не имели отклонения от нормы хотя бы по 1 показателю (латентность М-ответа, нарушение ГПР, латентность БКР). При этом только у 1/44 (2,3%) пациентки наблюдался 1 из упомянутых признаков, у 25/44 (56,8%) были отмечены 2 признака, а у 18/44 (40,9%) зарегистрированы все 3. Однако статистически значимой корреляции между показателями боли в баллах по шкале ВАШ и количеством признаков обнаружить не удалось (r=0,01 (-0,296;0,298); р=0,99).
Таким образом, статистически значимых предикторов боли у обследуемой категории пациенток в виде нейрофизиологических показателей увеличения латентностей М-ответа и БКР, а также нарушения ГПР – по отдельности или в сочетании –в нашей работе найти не удалось.
Также нами были построены регрессионные модели (оценки сделаны методом наименьших квадратов), в которых независимыми переменными, выступающими в качестве предикторов, являлись полученные нейрофизиологические показатели, а в качестве зависимых – учитывался балл по шкале ВАШ и показатели сфинктерометрии в состоянии покоя и при волевом сокращении, а также степень ректоцеле. Значимых коэффициентов перед независимыми переменными не удалось получить ни в одном из указанных уравнений как в однофакторных, так и в многофакторных моделях. Так, для ВАШ показатели р для коэффициентов составили (здесь и далее представим в виде «однофакторная модель»/«многофакторная модель»): для показателя М-ответа – p=0,70/0,71, для показателя БКР – р=0,39/0,46, для показателя ГПР – р=0,22/0,33.
Для параметров давления в покое статистическая значимость для М-ответа составила p=0,15/0,38, для показателя БКР – р=0,11/0,16, для показателя ГПР – р=0,52/0,48. Для параметров давления при волевом сокращении статистическая значимость для М-ответа – p=0,81/0,45, для латентности БКР – р=0,08/0,07, для показателя ГПР – р=0,86/0,79. В случае разных степеней ректоцеле статистическая значимость для М-ответа была p=0,77/0,81, для показателя БКР – р=0,13/0,12, для показателя ГПР –р=0,70/0,51.
Кроме того, ни в одной из моделей не наблюдалось статистически значимой положительной связи между баллами по шкале ВАШ, параметрами тонуса анальных сфинктеров и тем фактом, были ли отклонения от нормы независимых переменных билатеральными или монолатеральными. Нет никакой зависимости между показателями боли (балл по шкале ВАШ) и тонуса анальных сфинктеров (баллы по шкале Wexner, давление в покое и при волевом сокращении) и количеством одновременно наблюдаемых отклонений как в однофакторной, так и в многофакторной модели.
U-Тесты Манна-Уитни указывают на то, что показатель ВАШ не зависит от того, наблюдается ли у пациента сочетание увеличения латентности БКР и нарушения ГПР или только 1 из данных признаков (р=0,78), причем аналогичный результат получается и для пациентов с нормальным М-ответом (р=0,24).
Проводя дальнейший статистический анализ, мы попытались выявить зависимость между параметрами, характеризующими недержание кишечного содержимого, и нейрофизиологическими показателями. При этом необходимо сразу отметить очевидную закономерность: давление как в покое, так и при волевом сокращении, по данным комплексной сфинктерометрии, среди пациенток без жалоб на недержание компонентов кишечного содержимого значимо выше, чем среди пациенток с жалобами (35/44 (79,5%)). И эти различия статистически значимые: р<0,001 для давления в покое и р<0,001 для давления при сокращении.
При проведении регрессионного анализа для определения детерминант оценки недержания кишечного содержимого мы использовали линейную регрессию. В качестве зависимой переменной в уравнении регрессии выступал субъективный показатель оценки недержания по шкале Wexner.
Независимыми переменными, которые и выступали в качестве предикторов развития недержания, являлись полученные нейрофизиологические показатели:
- М-ответ, латентность: 0 – нормальная, 1 – изменена;
- ГПР: 0 – нормальный, 1 – нарушен хотя бы с одной стороны;
- БКР, латентность: 0 – не увеличена, 1 – увеличена хотя бы с одной стороны.
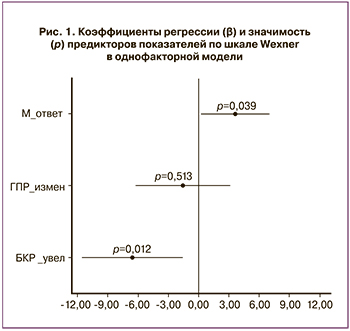 В рамках построения регрессии нами рассмотрены как однофакторные, так и многофакторные модели. Отметим, что IQR указывает на отсутствие влияющих на результат выбросов.
В рамках построения регрессии нами рассмотрены как однофакторные, так и многофакторные модели. Отметим, что IQR указывает на отсутствие влияющих на результат выбросов.
Как видно из рисунка 1 и таблицы, нарушенный М-ответ является положительным предиктором увеличения балла по шкале Wexner в однофакторной модели: β-коэффициент равен 3,64 (p=0,04). При этом показатель увеличенного БКР не имеет положительной связи с баллами по шкале Wexner (связь отрицательная), а показатель ГПР не является значимым. К тому же, как уже говорилось выше, сочетания нейрофизиологических показателей друг с другом встречаются часто, поэтому при включении их всех одновременно в многофакторную модель значимость увеличенной латентности М-ответа снижается до р=0,18, а β – до 2,37. При этом VIF в модели равен 1,11 (что указывает на наличие мультиколлинеарности), а остатки распределены ненормально (р=0,21); следовательно, в приоритете использование результатов однофакторного анализа.
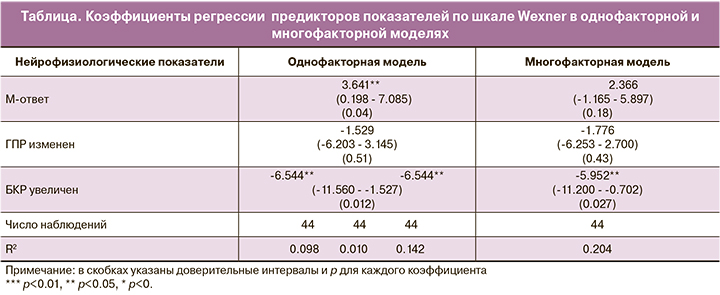
Нами была обнаружена интересная закономерность. Так, если рассмотреть показатели только для нормальных М-ответов, то значимость коэффициентов при ГПР будет р=0,36, а в случае с БКР во всех случаях наблюдается отклонение БКР от нормы при регистрируемом нормальном М-ответе.
Следует обратить внимание, что в случае с показателем баллов по шкале Wexner мы можем констатировать наличие статистически значимых различий (р=0,02) при использовании теста Манна–Уитни для балльной оценки между пациентами, у которых БКР и ГПР нарушены одновременно, и больными, у которых изменен хотя бы один из этих нейрофизиологических показателей. А при рассмотрении аналогичных различий у пациентов с нормальным М-ответом статистическая значимость наблюдается, но только на 10% уровне (р=0,1). Данный факт может указывать на необходимость дальнейшего набора клинического материала при использовании всех нейрофизиологических методик с целью выявления возможных статистических закономерностей между клиническими проявлениями недержания кишечного содержимого и изменением латентности/нарушением БКР и ГПР соответственно.
Обсуждение
Анализируя полученные результаты, мы обратили внимание на наличие 15/44 (34,1%) пациентов с клиническими проявлениями недостаточности анального сфинктера и болевым синдромом, имеющих нормальные показатели латентности М-ответа полового нерва при измененных показателях латентности ГПР и/или БКР. В связи с этим для нас принципиально важным представляется расширение методик стимуляционной ЭНМГ для выявления нарушений на всех звеньях рефлекторной дуги, включая как афферентные, так и эфферентные звенья рефлекторных ответов. Исследование латентного периода проведения возбуждения по двигательным волокнам n. рudendus при регистрации М-ответа с мышц наружного сфинктера или/и мышц тазового дна представляется, на наш взгляд, информативным для оценки состояния иннервации на дистальном участке нерва. Тогда как изучение ГПР, включающего оценку афферентной и эфферентной составляющих, которые запускаются при стимуляции смешанного полового нерва, позволяет изучать состояние иннервации и на проксимальном участке нерва.
Вместе с тем даже оценка ГПР не позволяет полностью комплексно оценивать как афферентную (от рецепторов до задних рогов спинного мозга), так и эфферентную иннервацию (от передних рогов до мышц-эффекторов), поскольку стимуляция в случае регистрации ГПР происходит не с рецепторов, а при антидромном распространении сигнала непосредственно от чувствительных волокон полового нерва в точке его раздражения у бугорка седалищной ости.
В связи с этим изучение БКР, на наш взгляд, является наиболее оптимальным для оценки деятельности мышц тазового дна, поскольку позволяет оценивать нервно-рефлекторные реакции, возникающие при стимуляции чувствительных зон промежности.
На наш взгляд, комплексная оценка при стимуляционной ЭНМГ последовательно: сначала – М-ответа, потом – смешанного возвратно-рефлекторного ответа и затем – БКР позволяет дискретно изучить как нарушение иннервации на дистальном участке эфферентного звена на проксимальном участке полового нерва, так и весь рефлекторный путь (рис. 2).
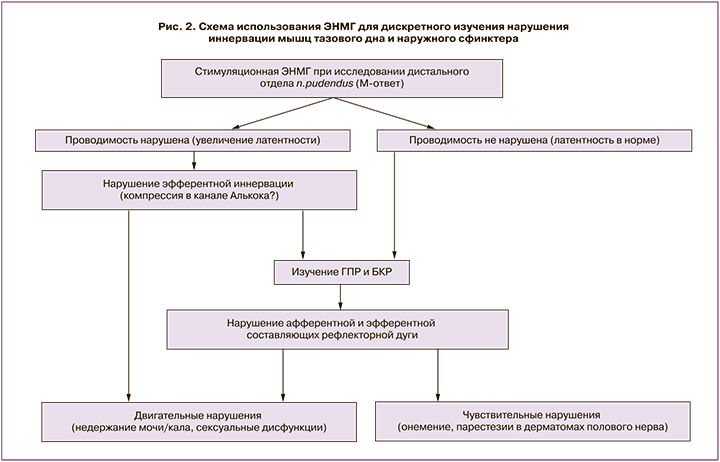
На сегодняшний день объяснить влияние нарушений ГПР и БКР на патогенез развития анальной инконтиненции у больных с пролапсом гениталий при наличии болевого синдрома представляется сложной задачей, однако данный факт требует более широкого использования стимуляционных нейрофизиологических методик и накопления материала с целью выявления определенных диагностических маркеров развития недостаточности анального сфинктера и болевого синдрома у данной категории больных.
Выводы
Нейропатия у пациенток с болевым синдромом на фоне пролапса тазовых органов монолатерально или билатерально, по данным нейрофизиологического исследования, встречается во всех наблюдениях.
У 65,9% больных нейропатия может быть диагностирована по увеличению латентности М-ответа (в совокупности с изменением показателей БКР/ГПР), в то время как в 34,1% случаев данное состояние регистрируется только по нарушению параметров ГПР и/или БКР.
Увеличенная латентность М-ответа при оценке проведения возбуждения по двигательным волокнам полового нерва может служить предиктором развития клинических проявлений недержания кишечного содержимого у пациенток с пролапсом тазовых органов и болевым синдромом.
В алгоритм нейрофизиологического исследования у пациенток с болевым синдромом на фоне пролапса тазовых органов могут быть включены, помимо изучения латентности М-ответа, оценка смешанного возвратно-рефлекторного ответа в виде ГПР, а также изучение БКР.



