Проблема дефицита андрогенов у женщин репродуктивного возраста не изучена и, несмотря на достижения в исследовании этого состояния в постменопаузе, остается открытой для дискуссии. В современной научной и клинической практике критерии диагностики андрогенного дефицита не определены, как и его вклад в обеспечение качества жизни женщины в репродуктивном возрасте [1]. Так как в настоящее время отмечается тенденция к рождению детей в позднем репродуктивном возрасте, проблема изучения андрогенного дефицита представляется крайне актуальной как с позиции репродуктивных достижений, так и поддержания качества жизни и здоровья женщин. Решение о рождении ребенка в позднем репродуктивном периоде – 35 и более лет – принимается уже на фоне изменения концентраций репродуктивных показателей, задолго до нарушения ритма менструаций, которое становится клинически выраженным к 40 годам, что сопряжено с изменением процессов фолликулогенеза [2]. Многочисленные исследования определили влияние андрогенов и их метаболитов как доминирующее на половой диморфизм, когнитивную, психоэмоциональную сферу, метаболические процессы и сексуальное функционирование. Детекция изменений вышеперечисленных функций не всегда возможна на основании только лабораторных данных, так как клиническая диагностика носит ретроспективный характер [1]. Сложности диагностики андрогенного дефицита заключаются в отсутствии референсных значений андрогенов для женщин, в том числе и по возрастным группам, и проблемах в определении концентрации тестостерона как молекулы с малой молекулярной массой, что затрудняет выявление изменений, ассоциированных со снижением уровня андрогенов. Все вышеперечисленное свидетельствует о необходимости разработки дополнительных методов диагностического исследования и создания психодиагностического конструкта.
Андрогенный дефицит определен в 2002 г. по заключению консенсуса в Принстоне («Принстонский консенсус») у женщин с физиологической менопаузой или при длительной выраженной гипоэстрогении при наличии следующего симптомокомплекса: снижения либидо, ухудшения общего самочувствия, появления дисфорических нарушений, астении, ощущения постоянной и необъяснимой усталости, субдепрессивного фона настроения, снижения костной массы и мышечной силы, истончения волос и ухудшения когнитивных и мнестических функций [3]. Такая симптоматика и проявления нарушений объясняются распределением андрогенных рецепторов (АР), экспрессия которых наблюдается в различных тканях в репродуктивных и нерепродуктивных органах, в частности в центральной нервной системе, что свидетельствует о роли андрогенов в обеспечении когнитивных функций и сексуального функционирования. Так, при гонадэктомии изменяется нейропластичность гиппокампа с последующей депрессией и снижением сексуальной мотивации и влечения. Установлено, что мозг определяет вторичные сексуальные признаки во время развития и сексуального созревания, поддерживает их функциональное состояние на протяжении всей жизни во взрослом организме и моделирует сексуальное поведение, которое является мишенью не только для эстрадиола, инициирующего сексуальное желание [4, 5], но и для тестостерона, который оказывает влияние на нейронные и поведенческие функции через геномные и негеномные эффекты [6].
Функционирование ключевых областей мозга, ответственных за мотивацию и удовольствие, зависит от концентрации тестостерона и в основном опосредовано активацией АР. Высокоаффинны АР к дигидротестостерону в медиальной преоптической области гипоталамуса, ключевой области мозга, регулирующей сексуальное поведение. В основе влияния тестостерона на сексуальное функционирование лежат нейроэндокринные механизмы; механизмы реализации эффектов, тем не менее, изучаются и находятся в зоне открытой дискуссии: через прямую стимуляцию АР или через его преобразование в эстрогены и последующее связывание с рецепторами эстрогенов [7].
С возрастом у женщин происходит прогрессивное снижение фолликулярного резерва в яичниках, что коррелирует со снижением фертильности, максимально в период от 30 до 40 лет. Наряду с наблюдаемым снижением количества антральных фолликулов (КАФ) также снижается качество ооцитов [5]. Известно, что основным фактором риска сниженного овариального резерва (СОР) является возраст [6]. Это происходит не только из-за снижения пула фолликулов в яичниках [7], но и в результате снижения чувствительности яичников к фолликулостимулирующему гормону (ФСГ) [8] и снижения уровня предшественников андрогенов (дегидроэпиандростерона (ДГЭА), ДГЭА-сульфата (ДГЭА-С), aндростендиона) и биоактивного андрогена – тестостерона [9, 10].
По результатам проведенных программ вспомогательных репродуктивных технологий (ВРТ) в ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России с 2014 по 2021 гг. отмечено увеличение числа женщин с СОР (рис. 1).

Золотым стандартом определения концентрации гормонов в крови является метод высокоэффективной жидкостной хроматографии/масс-спектрометрии. Применение психодиагностического тестирования может быть методом оценки ранних проявлений андрогенного дефицита до гормонального обследования у женщин репродуктивного возраста с целью их коррекции.
В научной и клинической практике одним из методов диагностики когнитивных нарушений и сексуального функционирования является психодиагностика в форме опросника [10]. Использование информации, полученной напрямую от пациента, при анализе клинических проявлений заболевания и оценке динамики симптомов в процессе лечения способствует реализации пациентоориентированного подхода при ведении женщин с бесплодием и СОР.
В современной медицинской практике наиболее широко используется международный опросник выявления возрастного андрогенного дефицита у мужчин – Aging Males Symptoms [11, 12]. Тогда как у женщин опросника, позволяющего выявить ранние изменения андрогенного дефицита, в доступной нам литературе не найдено. Для женщин широко используется шкала оценки дефицита эстрогенов в менопаузе – индекс Куппермана [13]. Для детальной оценки женского сексуального функционирования используется опросник FSFI – Индекс женской сексуальной функции (Female Sexual Function Index) [14, 15].
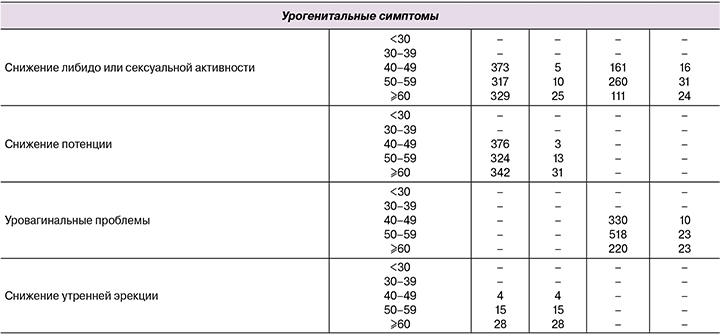
При разработке коллегами из Германии опросника для мужчин AGMS был проведен анализ 6 баз данных как мужчин, так и женщин, распределенных по возрастным периодам (Приложение 1). Проведенный анализ показал увеличение жалоб с увеличением возраста, увеличение доли пациентов с жалобами в возрастном диапазоне 30–39 лет и 40–49 лет у женщин, что свидетельствует о влиянии взросления на общее благополучие. Это особенно характерно для женщин после 35 лет и старше. Cвязь с андрогенами и андрогенным дефицитом замечена в виде снижения после 30 лет уровня андростендиона и ДГЭА-С как предшественников стероидных гормонов [16].
Женщины чаще предъявляли характерные для дефицита андрогенов жалобы после 35 лет, когда снижается функциональная активность половых желез – яичников, которая становится еще более выраженной после 40 лет. Равномерное распределение и встречаемость жалоб как у мужчин, так и у женщин еще раз подтверждало возраст-ассоциированное снижение половых стероидов. Целесообразным является необходимость рассмотрения проявлений синдромокомплекса при сочетании нескольких жалоб. В менопаузе чаще всего отмечались проявления из всех трех шкал, используемых для оценки степени тяжести: психоэмоциональных, соматовегетативных и генитоуринарных. Учитывая важную роль половых стероидов – эстрогенов и андрогенов в функциональной активности репродуктивной системы как у мужчин, так и у женщин, можно предположить, что дефицит половых стероидов влияет на оба пола, но выраженность их проявлений манифестирует клинически по-разному. Более того, репродуктивная активность женщин во времени сокращена в отличие от мужчин, что объясняется физиологическими особенностями, с одной стороны, и высокими концентрациями андрогенов в организме – с другой; тогда как у женщин основной циркулирующий гормон в организме – эстрадиол и его метаболиты, но андрогены являются предшественниками синтеза эстрогенов. При гиперэстрогении не отмечается увеличения фолликулярного пула яичников, тогда как при увеличении уровня андрогенов имеют место надпочечниковая гиперандрогения и синдром поликистозных яичников. Однако после 35 лет отмечено возрастзависимое снижение как фолликулярного резерва, так и уровней андрогенов с различной клинической манифестацией в зависимости от их исходных значений. Все вышеперечисленное свидетельствует о необходимости разработки и оптимизации (валидации) опросника андрогенного дефицита для женщин.
Нами был разработан и валидирован опросник оценки андрогенного дефицита у женщин – Female Androgen Deficiency (FAD) (Приложение 2) с целью ранней диагностики проявлений еще до обнаружения лабораторных изменений андрогенов. Данный опросник позволяет оценить выраженность психологических, соматических и сексуальных нарушений, обусловленных возрастным снижением андрогенов, не только в постменопаузе, но и в репродуктивном периоде, что актуально у женщин с бесплодием.
Целью данного исследования была разработка и валидация опросника FAD для оценки проявлений андрогенного дефицита у женщин репродуктивного возраста с бесплодием с целью его дальнейшего применения в клинической практике и в научных исследованиях.
Материалы и методы
Исследование проводили в период с 2019 по 2022 гг. на базе 1-го гинекологического отделения ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России.
Всем пациентам, включенным в исследование, на консультативном приеме одномоментно были даны опросники FAD и FSFI, с последующим проведением клинико-лабораторного обследования; выборочно было проведено интервьюирование, описанное ниже. Повторное заполнение опросника FAD проводилось спустя месяц после консультации (пациенты, получавшие терапию, заполнили его через месяц после андрогенного прайминга).
Для языковой валидации и исключения двойного толкования вопросов на первом этапе тестовую версию FAD проверяли на популяции из 20 женщин различных социально-экономических групп при помощи индивидуального интервьюирования. Затем таким же методом проводили апробацию опросника FAD на 10 пациентках с установленным андрогенным дефицитом и на 10 пациентках без андрогенного дефицита.
Ключевыми аспектами при интервьюировании пациентов были: оценка корректности формулировки и доступность для восприятия; комфорт при выборе ответа; легкость оценки той или иной проблемы.
В рамках этого этапа также проверяли валидность опросника на основании мнения пациентов и диапазон возможных проблем, включенных в исследование.
На втором этапе работы провели апробацию опросника FAD в группе женщин с бесплодием и СОР, у которых по данным лабораторного исследования выявлены показатели андростендиона <7,0 нмоль/л и ФСГ<8,6 мМЕ/л с оценкой психометрических свойств инструмента.
В исследование включали женщин репродуктивного возраста от 18 до 42 лет при наличии показаний для программ ВРТ и СОР при условии согласия на участие в исследовании и способности пациентов заполнить опросники. Письменное информированное согласие было получено от каждого пациента, вошедшего в исследование.
Критерии исключения: хирургическая менопауза (двусторонняя овариэктомия или гистерэктомия); гормонпродуцирующие опухоли; индекс массы тела (ИМТ) ≥30 кг/м2 и ≤18 кг/м2; ВИЧ-инфекция и другие иммунодефицитные состояния; ревматические заболевания; иммуномодулирующая терапия, прием глюкокортикоидов, комбинированных оральных контрацептивов, других гормональных препаратов, внутриматочная контрацепция, онкологические заболевания.
В исследование первоначально были включены 600 женщин – по 300 человек в группу. Пациентки, не соответствующие критериям включения, а также не предоставившие полной информации о данных анамнеза и лабораторные исследования, были исключены или отказались принимать дальнейшее участие в исследовании. 496 пациенток, вошедших в исследование, были обследованы согласно приказу 803Н Минздрава Российской Федерации от 31 июля 2020 г. При сборе анамнеза учитывались следующие факторы: возраст пациентки, соматические заболевания, курение, ИМТ, сексуальная активность, возраст наступления менопаузы у матери женщины.
Были сформированы 2 группы пациенток в зависимости от состояния овариального резерва в соответствии с Болонскими критериями. 1-я группа – 256 женщин с СОР (АМГ≤1,2 нг/мл и КАФ≤5 на 3-й день менструального цикла), 2-я группа – 240 женщин с нормальным овариальным резервом (НОР) (АМГ≥1,2 нг/мл и КАФ≥5 на 3-й день менструального цикла).
Валидация разработанного опросника FAD включала оценку нескольких параметров – надежности, валидности и чувствительности к изменениям во времени. Анализ валидности проводился на основании определения конструктной, дискриминантной, критериальной и конвергентной валидности. Анализ надежности проводили с помощью оценки внутреннего постоянства путем вычисления коэффициента α-Кронбаха (коэффициента внутренней согласованности). Конструктную валидность опросника проверяли с помощью изучения его структуры факторным анализом. Дискриминантную валидность оценивали методом известных групп, сравнивая суммарный балл по опроснику у женщин с бесплодием и СОР в программах ВРТ с донорами ооцитов. Для оценки конвергентной валидности проводили анализ корреляций между суммарным баллом и количеством испытываемых симптомов. Критериальную валидность оценивали с помощью корреляционного анализа между суммарным баллом FAD и шкалами опросника FSFI, который рассматривали как стандарт для оценки изменений сексуального функционирования у женщин. Опросник оценки андрогенного дефицита FAD характеризует 3 группы симптомов по 4 пункта в каждой группе и позволяет выявить снижение концентрации андрогенов и проявления андрогенного дефицита с учетом распространенности АР в организме женщины.
1-я группа – психологические факторы, включают в себя проблемы со сном, нервозность, потерю мотивации, депрессию.
2-я группа – соматические факторы, включают в себя ухудшение самочувствия и общего состояния, боль и ломоту в мышцах и суставах, потливость и снижение мышечной силы.
3-я группа – сексуальные факторы, включают в себя снижение частоты сексуальных отношений, снижение сексуального желания/либидо, отсутствие оргазма при половых контактах и отсутствие сексуальных фантазий и сновидений.
Каждый пункт опросника оценен в соответствии с пятью степенями выраженности симптомов: нет – 1 балл, редко (меньше чем в половине случаев) – 2 балла, в половине случаев – 3 балла, часто (больше чем в половине случаев) – 4 балла, постоянно – 5 баллов.
По каждой группе факторов тяжесть симптомов рассчитывалась путем суммирования баллов, полученных за соответствующие вопросы. Общий балл, характеризующий степень выраженности симптомов андрогенного дефицита у женщин, высчитывался при суммировании показателей всех параметров.
С целью подтверждения результата все женщины отвечали на опросник дважды, с интервалом в один месяц.
Для оценки чувствительности опросника к изменению во времени женщинам с андрогенным дефицитом проводилась терапия андрогенсодержащими препаратами (ДГЭА пероральная форма и тестостеронсодержащий гель) с целью прайминга. Были оценены результаты опросника до и после терапии, как суммарный балл, так и по трем компонентам в отдельности.
Также проводилась оценка андрогенного профиля методами масс-спектрометрии и иммунохемилюминесцентного анализа.
Статистический анализ
Статистическая обработка данных выполнялась с использованием пaкета статистических программ Statistica V10 (StatSoft Inc., США) и SPSS Statistics V17 (США).
Перед проведением сравнительного анализа количественных данных в исследуемых группах определяли вид распределения данных (тест Колмогорова–Смирнова). При нормальном виде распределения данных определяли среднее значение со стандартным отклонением M (SD), для оценки различий в группах применяли методы параметрической статистики (t- тест для сравнения данных в двух группах, парный t-тест для выявления динамических различий). При распределении, отличном от нормального, данные представлены в формате медианы с интерквартильным размахом Ме (Q1; Q3), для оценки различий в группах применяли методы непараметрической статистики (тест Манна–Уитни для сравнения данных в двух группах, тест Вилкоксона – для динамических различий).
Для сравнения качественных показателей, представленных в виде абсолютных и относительных значений, применяли метод Хи-квадрат (χ2).
В работе применяли также корреляционный анализ Пирсона (для нормально распределенных показателей) и непараметрический корреляционный анализ Спирмена. Для оценки надежности опросника рассчитывался коэффициент α-Кронбаха. Применялся факторный анализ с использованием метода главных компонент и способа вращения варимакс по критерию каменистой осыпи.
Различия между величинами считали статистически значимыми при уровне статистической значимости p<0,05.
Протокол данного исследования № 2 был одобрен комиссией по этике биомедицинских исследований при ФГБУ «НМИЦ АГП им. академика В.И. Кулакова» Минздрава России от 07 февраля 2019 г.
Результаты
При создании предварительной тест-версии опросника были выбраны оптимальные формулировки, которые были предложены с учетом культурных особенностей популяции. Для тестирования FAD в процедуру интервьюирования были включены женщины с бесплодием и СОР в возрасте от 18 до 43 лет. В процессе интервьюирования все пациенты отметили ясность изложения и понятность смысла вопросов тест-версии, положительное впечатление о предложенном способе оценки проблем, связанных с качеством жизни, а также соответствие вопросов опросника актуальным проблемам у женщин при бесплодии и СОР. В среднем заполнение опросника пациентом составило 3 минуты. На основании результатов тестирования FAD при участии пациентов определены три показателя внешней валидности – понятность, легкость и удобство оценки (для каждого симптома и для инструмента в целом), а также полнота оценки (для инструмента в целом). Каждый показатель выражен в баллах от 0 до 1; чем выше показатель, тем лучше внешняя валидность инструмента по данной категории. В целом для FAD получены высокие показатели внешней валидности: понятность – 1,0 балла, легкость и удобство оценки – 0,91 балла, полнота оценки – 0,87 балла. Общий (средний) показатель внешней валидности составил 0,88 балла. Выявленные в ходе тестирования комментарии пациентов по некоторым вопросам в целом являлись незначительными и были обусловлены, скорее всего, индивидуальными особенностями пациентов и внешними факторами.
Таким образом, по результатам тестирования FAD при участии пациентов, а также в ходе экспертной оценки клиницистами были подтверждены приемлемость опросника FAD, ее соответствие среде, высокие показатели содержательной и внешней валидности.
В апробации опросника FAD приняли участие женщины репродуктивного возраста с бесплодием и СОР, обратившиеся для проведения программ ВРТ в ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России, средний возраст больных – 37,3 (2,4) года.
У всех пациенток, учитывая статистически незначимое различие межменструального интервала, отмечалась регулярность менструального цикла, средняя продолжительность 27,4 (2,1) дня. Возраст наступления менопаузы у матерей пациенток в группе женщин с СОР составил 45,6 (2,6) года.
В структуре перенесенных воспалительных и инфекционных заболеваний половых органов каждая 3-я пациентка отмечала сальпингит и аднексит в анамнезе. На проведенные оперативные вмешательства – аппендэктомию или диагностическую лапароскопию в связи с трубно-перитонеальным фактором указывали 30% пациенток. Часто отмечалось наличие в анамнезе спаечной болезни, что, вероятно, ассоциировано с более высокой частотой оперативных вмешательств. Отмечено в среднем 2,7 (1,2) программы ЭКО в анамнезе, завершившихся негативным результатом на этапе гормональной верификации беременности. Длительность бесплодия составила 6,8 (5,9) года, 347/496 (70%) пациенток были с первичным бесплодием. Наличие в анамнезе беременностей, закончившихся родами, отмечено у 164/496 (33%) пациенток, медицинский аборт по различным показаниям – у 94/496 (19%), наличие в анамнезе на ранних сроках прерывания беременности до 6–7 недель гестации составило 173/496 (35%).
При оценке антропометрических данных нами была выявлена тенденция к увеличению ИМТ у пациенток с СОР, составив 24,6 (5,4) кг/м², хотя статистически значимого различия не выявлено.
Рассмотрим результаты апробации опросника FAD в фокусной группе женщин с бесплодием и СОР. В целом опросник был понятен и не вызывал трудностей в заполнении у подавляющего большинства пациентов.
Конструктная валидность
Для валидации структуры опросника был применен факторный анализ с использованием метода главных компонент и способа вращения варимакс по критерию каменистой осыпи (рис. 2).

В результате проведенного анализа нами выбраны 3 фактора со значением общности больше 1. После процедуры вращения методом варимакс нормализацией Кайзера получены результаты (табл. 1).
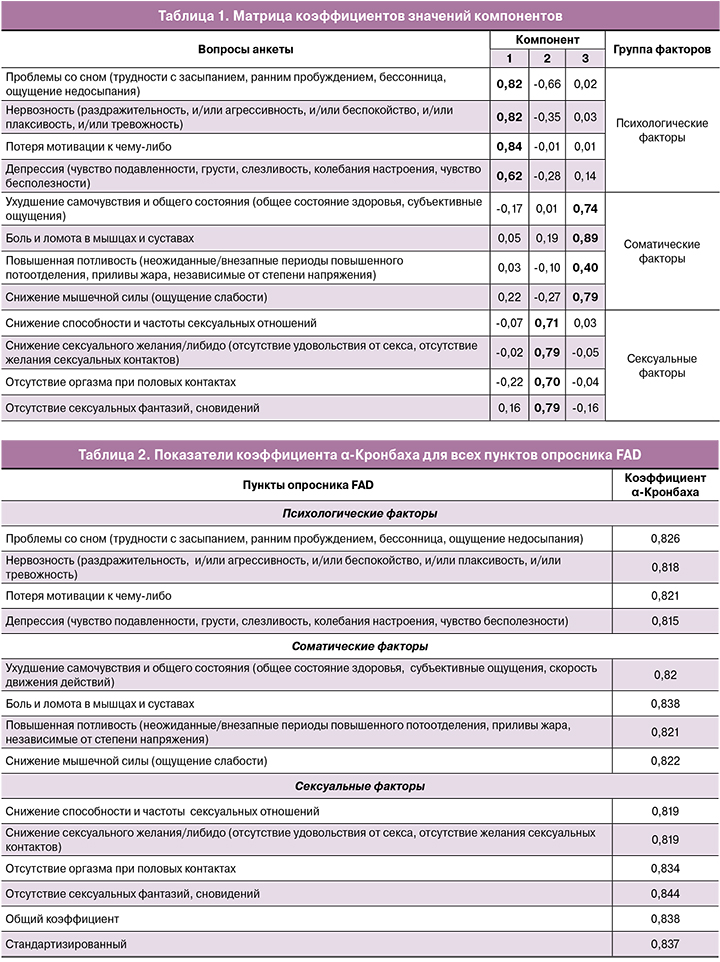
Критерий адекватности Кайзера–Мейера–Олкина (0,72) и критерий сферичности Бартлетта (p<0,001) свидетельствует о приемлемой адекватности факторного анализа к выборке. Рассчитанные коэффициенты общности превышают 1 для всех.
Таким образом, проведенный факторный анализ свидетельствует об адекватности группировки вопросов анкеты по предполагаемым факторам и устойчивой конструктной валидности.
Надежность
При анализе надежности методом оценки внутреннего постоянства для 12 вопросов, связанных с проявлениями андрогенного дефицита, получено значение коэффициента α-Кронбаха, равное 0,837. Данная величина свидетельствует о внутреннем постоянстве опросника FAD. В таблице 2 отражены значения коэффициента α-Кронбаха при поочередном удалении пунктов опросника. Можно сделать вывод, что используемый инструмент позволяет проводить достаточно точную оценку симптомов/проблем, формирующихся при андрогенном дефиците у женщин репродуктивного возраста на раннем этапе.
Ковергентная валидность
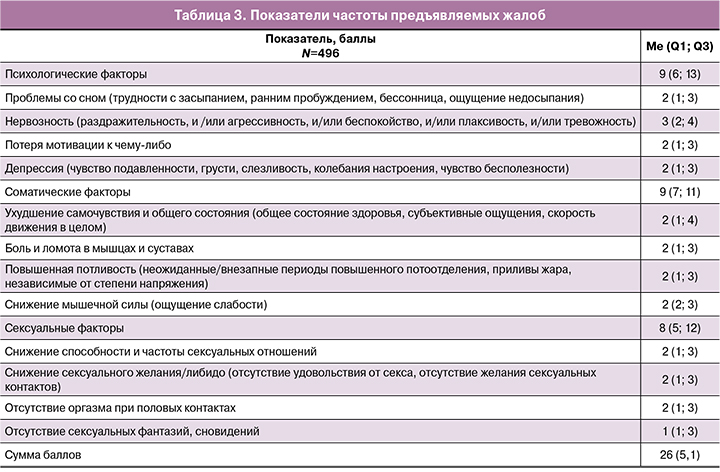
Анализ связи суммарного балла опросника с количеством предъявляемых жалоб и симптомов вследствие формирующегося симптомокомплекса – дефицита андрогенов показал, что наиболее частыми симптомами были: нервозность (3,4 (1,4) балла), снижение способности и частоты сексуальных отношений (2,9 (1,2) балла), ухудшение самочувствия и общего состояния (2,8 (1,3) балла), снижение сексуального желания/либидо (2,8 (1,1) балла). При анализе корреляций между суммарным баллом по FAD и количеством симптомов у женщин с бесплодием и СОР выявлена статистически значимая отрицательная сильная связь (r=-0,76; p<0,001). Чем больше симптомов и проблем, связанных с заболеванием, испытывает пациент, тем выраженнее проявления андрогенного дефицита. Полученный результат отражает хорошую критериальную валидность опросника FAD (табл. 3).
Дискриминантная валидность
С целью определения чувствительности опросника FAD был проведен анализ, в ходе которого выполняли сравнение суммарного балла в группах женщин с бесплодием и СОР с группой женщин с НОР и доноров ооцитов методом «известных групп»: суммарный балл по опроснику FSFI у здоровых ниже, чем у женщин с СОР (31,7 (6,2) балла против 18,4 (4,1) балла, тест Стьюдента, p<0,001). Таким образом, продемонстрирована способность инструмента определять степень выраженности проявлений андрогенного дефицита в зависимости от СОР. Эти данные характеризуют удовлетворительную дискриминантную валидность опросника.
Критериальная валидность
В процессе корреляционного анализа выявлены статистически значимые положительные корреляции между суммарным показателем по данным опросника FAD и FSFI: сильная корреляция между общим суммарным баллом и психологическими факторами – r= 0,752 (табл. 4, рис. 3).

Таким образом, показана удовлетворительная конвергентная валидность опросника FAD.
Чувствительность к изменениям
Анализ чувствительности опросника к изменениям во времени проводили на основании оценки изменений суммарного показателя по группам женщин, которые заполнили опросник через 1 месяц после андрогенного прайминга (n=203); те, кто не получал лечение андрогенами, повторно заполнили анкету через месяц после первого опроса. На фоне проводимого андрогенного прайминга выявлено статистически значимое уменьшение суммарного балла – с 31,01 (5,9) до 22,92 (4,6) (p<0,001), что свидетельствует о значимом улучшении состояния и разрешения проявлений андрогенного дефицита у женщин репродуктивного возраста на фоне терапии. Произошло статистически значимое улучшение по отдельным компонентам андрогенного дефицита: по физическому – с 10,51 (3,75) до 8,6 (2,83) балла (р<0,001), соматическому – с 10,28 (2,44) до 7,54 (2,16) балла и сексуальному – с 10,23 (2,79) до 6,78 (1,84) балла (табл. 5).
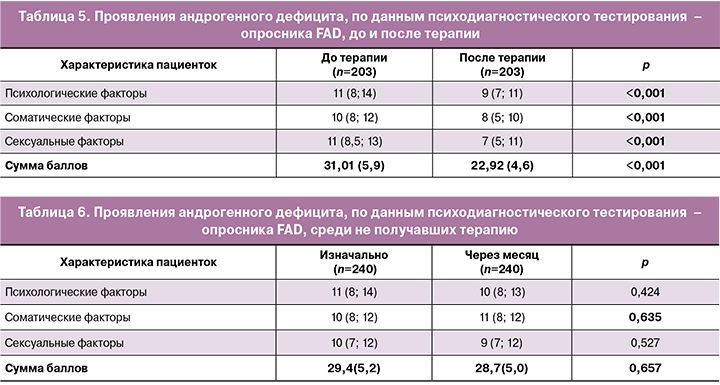
Результаты повторного опроса женщин, которые не получали терапию (n=240, включены женщины как без андрогенного дефицита, так и с андрогенным дефицитом), представлены в таблице 6. В связи с тем что данные пациенты не получали никакой терапии для коррекции андрогенного дефицита, отсутствие статистически значимых различий в динамике является логичным.
В целом на основании полученных результатов можно сделать вывод о том, что опросник FAD чувствителен к изменениям в состоянии женщин и может использоваться в практических целях как дополнительный критерий эффективности лечения.
Обсуждение
В результате исследования нами проведены разработка и валидация опросника андрогенного дефицита у женщин FAD с целью выявления проявлений андрогенного дефицита, влияющих на психоэмоциональный фон и сексуальное функционирование у женщин репродуктивного возраста с бесплодием и СОР. Показаны понятность формулировки и легкость ответов на вопрос пациентами.
Ключевыми психометрическими характеристиками, исследуемыми при тестировании опросника FAD для оценки пригодности его применения в клинической практике, являлись надежность, т.е. способность опросника выполнять точную оценку проявлений андрогенного дефицита, а также способность инструмента отражать клинические различия в состоянии больных (дискриминантная и критериальная валидность) и чувствительность к лабораторным методам оценки андрогенного профиля. Важным результатом исследования является продемонстрированная устойчивость структуры инструмента, свидетельствующая об удовлетворительной конструктной валидности и в существенной степени определяющая приемлемость ее использования для оценки проявлений андрогенного дефицита. Результаты оценки внутреннего постоянства инструмента указывают на надежность опросника FAD. Полученная величина коэффициента α-Кронбаха (0,83) характеризует высокое внутреннее постоянство его русской версии, т.е. высокую точность получаемых результатов.
Наиболее быстро реагирующими на изменение концентрации андрогенов являются ткани, в которых наблюдается экспрессия АР, в том числе нервной системы, чем и обусловлены клинические проявления андрогенного дефицита, а именно: ухудшение общего самочувствия, снижение когнитивных функций, астения, субдепрессивный и депрессивный фон настроения, ощущение усталости и снижение мотивации, истончение волос и снижение мышечной активности [17] и нарушения женского сексуального функционирования.
Возрастное снижение уровней андрогенов вносит значимый и, возможно, определяющий вклад в изменение психоэмоционального и сексуального функционирования, что объясняется снижением синтеза андрогенов и, соответственно, эстрогенов. Также необходимо учитывать вероятное снижение концентрации половых рецепторов в качестве фактора сужения окна терапевтических возможностей.
Учитывая значимость влияния проявлений андрогенного дефицита на общее благополучие женщины, необходимо включать данный синдром в дифференциальную диагностику патологических состояний даже у женщин при сохраненном ритме менструального цикла – репродуктивного возраста.
Заключение
Таким образом, полученные результаты позволяют утверждать, что валидированный опросник андрогенного дефицита у женщин в соответствии с международными и отечественными стандартами является надежным, валидным и чувствительным инструментом для оценки ранних проявлений андрогенного дефицита у женщин с бесплодием и СОР и позволяет оценить эффективность проводимой терапии андрогенсодержащими препаратами, что может использоваться в клинической практике и в научных исследованиях в репродуктивной медицине.