Аномально инвазивная плацентация (АИП) [врастание плаценты, приращение плаценты, placenta accreta spectrum (PAS)] – патологическое состояние, формирующееся в ранние сроки гестации вследствие имплантации бластоцисты, которое патоморфологически определено полным или частичным отсутствием децидуальной оболочки (decidua basalis), приводящим к приращению или прорастанию ворсинами хориона/плаценты мышечного слоя матки [1].
Актуальность обсуждаемой проблемы определена рядом причин. Во-первых, возросшей в последние годы распространенностью данной аномалии плацентации (примерно 1,7 на 10 000 беременностей) [2, 3], явившейся следствием лавинообразного роста частоты проведения кесарева сечения (КС). Частота операций КС в мире увеличилась более чем в 3 раза за последние 30 лет, и на сегодняшний день составляет около 25%; в некоторых клинических учреждениях третьего уровня Российской Федерации данный показатель превышает 40% [4]. Во-вторых, ассоциированностью PAS с акушерскими кровотечениями, как следствие, – с материнской смертностью (до 52%) [5, 6] и, в заключение, – трудностями диагностики. По данным Гуса А.И. и соавт., до родов PAS не диагностируется в 2/3 случаев, при том, что в 1/3 случаев это происходит в специализированных многопрофильных стационарах [7]; в то же время в 28% случаев пренатально сформулированный диагноз PAS не имеет гистопатологического подтверждения [8].
В настоящее время основным методом диагностики АИП является ультразвуковое исследование (УЗИ) [9–11]. Пионерами ультразвуковой диагностики АИП является группа американских специалистов, которые в 25 недель гестации на фоне маточного кровотечения диагностировали предлежание плаценты с аномально отсутствующей гипоэхогенной ретроплацентарной зоной. Диагноз АИП был подтвержден при морфологическом исследовании удаленной матки [12].
По данным D’Antonio E. et al., при УЗИ у 3907 беременных с риском АИП отмечена высокая эффективность метода с чувствительностью 90,7% (95% ДИ 87,2–93,6) и специфичностью 96,94% (95% ДИ 96,3–97,5) при диагностическом отношении шансов 98,59% (95% ДИ 48,8–199,0) [13].
Долгое время приоритетным сроком ультразвуковой диагностики АИП являлся III триместр беременности [13]. В последнее десятилетие прослеживается тенденция к уменьшению срока обнаружения АИП. Обнаружение предикторов АИП возможно, по мнению Panaitova J. et al., в сроке 12–16 недель [14]. Блинов А.Ю. и соавт. представили описание случая пренатальной диагностики истинного приращения предлежащей плаценты во время скринингового УЗИ в 13 недель и 4 дня у беременной с отягощенным акушерским анамнезом [15]. В 2020 г. Демидов В.Н. и соавт. высказали мнение, что диагноз АИП в большинстве случаев может быть установлен уже в 14–19 недель беременности [16].
Мотивация к «уменьшению сроков» диагностики обсуждаемой проблемы следующая: качественное, успешное лечение АИП в значительной мере предопределено максимально ранней ее диагностикой, позволяющей своевременно сформулировать оптимальный алгоритм действий, определяющий место, сроки, технологии лечения и состав команды специалистов, принимающих участие в родоразрешении такой пациентки. Учитывая сказанное, представляем собственный клинический опыт ранней ультразвуковой диагностики аномально глубокой инвазии хориона – предиктора врастания плаценты, верифицированного в последующем при патологоанатомическом исследовании.
Клиническое наблюдение
Пациентка М., 35 лет. Менархе с 14 лет, менструальная функция без особенностей. Настоящая беременность – пятая. В анамнезе одни физиологические роды per vias naturales в срок (2009 г.), два артифициальных аборта в I триместре (2011 г. и 2021 г.) и одно КС в 2019 г. (отслойка нормально расположенной плаценты).
В сроке 7 недель обратилась к гинекологу для постановки на диспансерный учет по беременности. На данном этапе пациентка жалоб не предъявляла, состояние расценено как удовлетворительное.
В сроке гестации 7+1 недель при эхографии в ГБУ Ростовской области «Перинатальный центр» было описано следующее: «...локализация хориона по передней стенке матки в области послеоперационного рубца, структура хориона неоднородная с расширенными лакунарными пространствами, визуализируются участки гиперваскуляризации миометрия передней стенки матки, толщина миометрия в области «рубца» 2,1 мм» (рис. 1а, б). Сформулировано заключение: беременность 7+1 недель, эхографические признаки врастания хориона в область послеоперационного рубца.
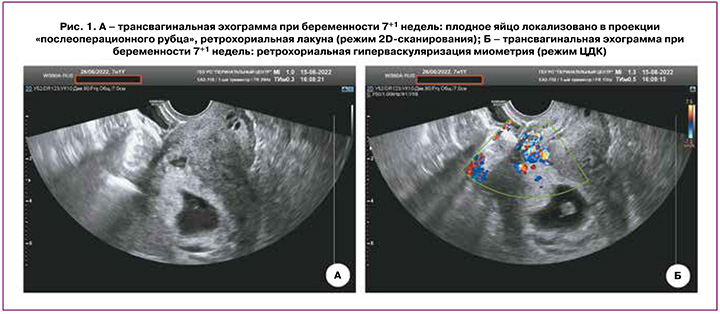
При эхографии в рамках раннего пренатального скрининга описана «низкая локализация плаценты». Визуализация с применением технологии цветового допплеровского картирования не проводилась.
При дальнейшей эхографии, выполненной в отделении ультразвуковой диагностики НИИАП РостГМУ в сроках 17, 19, 22, 25, 30 недель гестации, заключение об аномальном прикреплении хориона в ранние сроки трансформировалось в формулировку о PAS. Так, в сроке 19 недель описано следующее: плацента перекрывает область внутреннего зева, располагаясь по передней стенке матки в проекции послеоперационного рубца, слева визуализируются множественные ретроплацентарные лакуны с ламинарным кровотоком, достигающие зоны истонченного миометрия, в режиме ЦДК – гиперваскуляризация, на участке 50 мм в области «рубца» миометрий отчетливо не лоцируется, субплацентарно в режиме стереоскопической визуализации кровотока (LumiFlow) обнаружены сосуды, достигающие задней стенки мочевого пузыря, не проникающие в него (рис. 2 а, б). На основании проведенного исследования сформулировано заключение о предлежании плаценты, осложненном АИП (placenta increta, PAS 3a по версии Jauniaux E. et al. [10]).
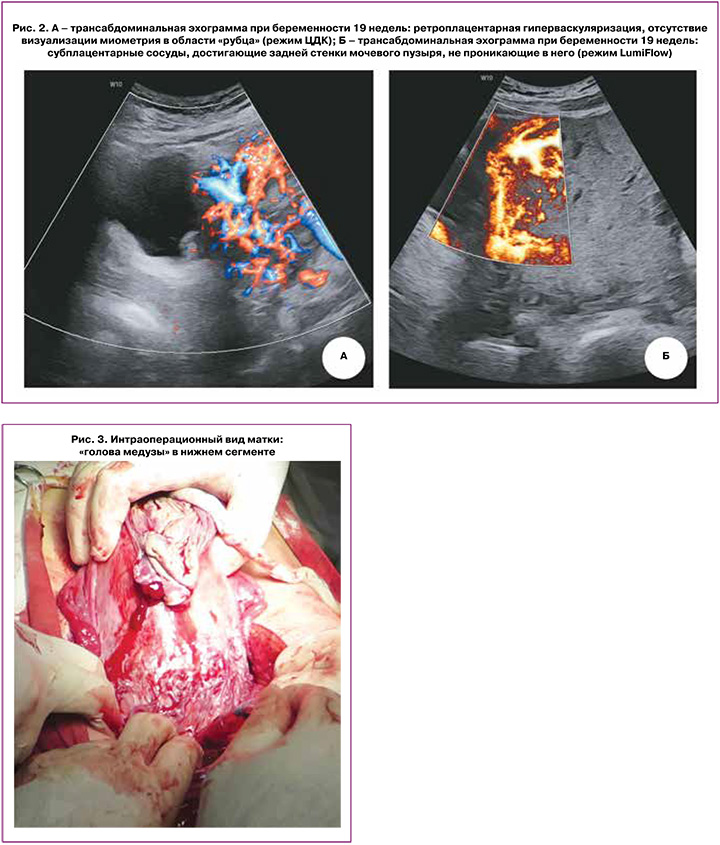
В сроке 37+2 недель в плановом порядке беременность была завершена оперативными родами абдоминальным путем. Под эпидуральной анестезией выполнено донное КС. Родилась доношенная девочка массой 2500 г, длиной 38 см с оценкой по Апгар 7/8 баллов. После рождения ребенка без попыток отделения плаценты осмотрены органы малого таза. Идентифицированы признаки АИП – сосудистая «голова медузы» нижней трети передней стенки тела матки (рис. 3). После лигирования внутренних подвздошных и яичниковых артерий с обеих сторон произведена метропластика. Иссечена часть передней стенки матки с плацентой. Тело матки восстановлено непрерывными швами по авторской методике [17]. Кровопотеря составила 1800 мл. Интраоперационно использована система для реинфузии крови (Sell Saver). Гемотрансфузия в послеоперационном периоде не проводилась. На 7-е сутки в удовлетворительном состоянии пациентка была выписана.
При патологоанатомическом исследовании иссеченной части передней стенки матки выявлены следующие изменения. Большую часть препарата занимала зона волокнистой соединительной ткани толщиной от 1,2 до 0,2 см местами плотной, местами рыхлой. К рубцовой ткани с выраженным ангиоматозом прилежала зона фибриноидного некроза с клетками трофобласта и частично некротизированными терминальными ворсинами. Децидуальная ткань на этом участке истончена, а местами отсутствовала (рис. 4а). На остальном протяжении децидуальная ткань неравномерной толщины с кровоизлияниями, обширными зонами фибриноидного некроза Рора и Нитабух, с образованием глубоких «бухт», приникающих в миометрий до ⅔ толщины, содержащих ворсины и клетки трофобласта (рис. 4б). Между гладкомышечными волокнами и в соединительной ткани были обнаружены клетки синцитио- и цитотрофобласта (рис. 4в). В промежуточных ворсинах плаценты, окруженных фибриноидом, – десквамация эпителия, облитерационная ангиопатия части артерий. Терминальные ворсины хориона с фиброзом стромы, ангиоматозом, образованием синцитиокапиллярных мембран и синцитиальных почек, в гипертрофированном миометрии – гравидарная трансформация артерий (рис. 4г).
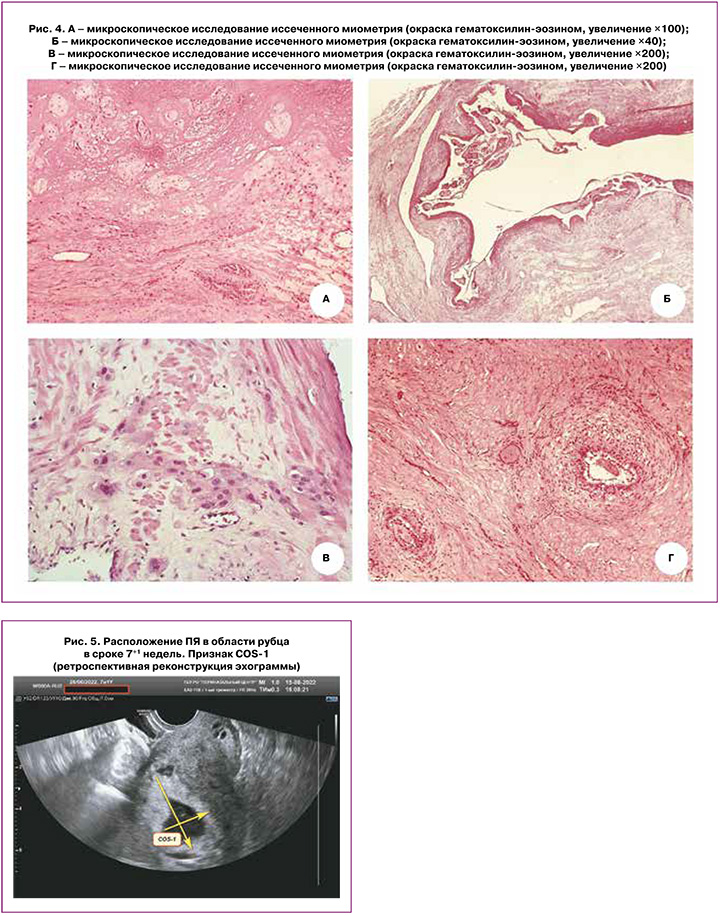
Заключение: послеоперационный рубец в стенке гравидарно трансформированной матки, приращение плаценты (placenta increta), вторичная хроническая плацентарная недостаточность.
Обсуждение
Представленное клиническое наблюдение наглядно демонстрирует реальную возможность ранней ультразвуковой диагностики АИП. Таким ультразвуковым признаком для прогнозирования PAS в ранние сроки беременности в 2017 г. Cali G. et al. [18] определили признак «перекрестка» (crossover sign, COS). В основе его – связь между расположением плодного яйца (ПЯ) при сроках 6–8 недель беременности и рубцом на матке после КС. Для оценки этого признака в сагиттальном сечении проводится прямая линия, соединяющая область внутреннего зева и дно матки и проходящая через эндометрий. Вторая линия проводится перпендикулярно эндометрию через верхний и нижний полюсы ПЯ, имплантированного в область рубца на матке после КС. В зависимости от расположения ПЯ выделяют несколько возможных вариантов, один из которых – COS-1. В этом случае ПЯ расположено на 2/3 своего диаметра выше линии эндометрия по направлению к передней стенке матки. По данным авторов, COS-1 в 100% случаев был ассоциирован с тяжелыми вариантами PAS [18].
Ретроспективно проведенная нами оценка этого признака (рис. 5) продемонстрировала, что в 7+1 недель ПЯ было эктопически расположено на ⅔ своего диаметра выше линии эндометрия по направлению к передней стенке матки в проекции рубца после КС. Таким образом, имел место признак COS-1, предполагающий высокую вероятность PAS 3, что и подтвердилось в дальнейшем.
Заключение
Обнаружение признаков АИП в максимально ранние сроки гестации предполагает отнесение пациенток в группу высокого риска формирования PAS для последующего целенаправленного поиска специфических признаков данной плацентарной патологии, способствующих в дальнейшем оптимальному планированию органосохраняющих приемов родоразрешения этих пациенток. Использование современного ультразвукового оборудования, «заряженного высоким диагностическим потенциалом», в руках подготовленного, мотивированного, ориентированного на целенаправленный поиск данной патологии специалиста – залог успешной ранней диагностики АИП, предполагающей улучшение акушерских и перинатальных исходов.



