Соединительная ткань в организме выполняет различные функции – барьерную, общую и местную адаптогенную, регенеративную, морфогенетическую. Как известно, основой соединительной ткани является коллаген, составляющий одну третью часть всех белков организма. В литературе описано 28 типов коллагена, однако более 90% всего коллагена в организме приходится на I, II, III и IV и V-образующие фибриллы, которые могут объединяться в волокна [1, 2].
Стенка влагалища имеет толщину 3–4 мм, не содержит желез и практически не содержит чувствительных нервных окончаний. Мышечная оболочка влагалища образована преимущественно продольными пучками гладкомышечных волокон, кнаружи от которой располагается адвентиция – оболочка из плотной соединительной ткани с высоким содержанием эластических волокон, коллагеновых волокон I и III типов, в которой располагаются обширное венозное сплетение, нервные клетки и пучки нервных волокон. Базальная мембрана имеет толщину около 1 мкм и состоит из двух пластинок: светлой (lamina lucida), включающей аморфное вещество, и темной (lamina densa), имеющей аморфный матрикс с рыхлой соединительной тканью (коллаген IV типа), обеспечивающей механическую прочность. Многослойный плоский эпителий (МПЭ) состоит из четырех слоев клеток и имеет толщину 150–200 мкм, достигая до 2 мм на отдельных участках. Иннервация влагалища осуществляется симпатической и парасимпатической нервной системой. Терморецепторы, как известно, бывают 2 видов: холодовые (колбочки Краузе), залегающие на глубине около 0,17 мм, и тепловые (тельца Руффини), находящиеся на глубине около 0,3 мм от поверхности эпителия, а также голые окончания афферентных нервных волокон. В эпителии вульвы, в частности, находятся терморецепторы, свободные нервные окончания и инкапсулированные чувствительные нервные окончания (тельца Фатера-Пачини и Мейснера) [3–7]. Строение стенки влагалища и структуру МПЭ, а также эпителия вульвы и глубину расположения терморецепторов необходимо учитывать при внедрении в практику современных методов терапии, основанных на селективном фототермолизе.
В настоящее время лазеры активно используются в различных областях медицины, в том числе и в гинекологии, что делает актуальным вопрос влияния различного вида лазерного излучения на биоткани, в особенности на соединительную ткань. В научной литературе на сегодняшний день имеется множество данных об исследованиях, посвященных действию лазерного излучения на ремоделирование молекул коллагена [8, 9]. Основными физическими параметрами лазера, определяющими воздействие на ту или иную биологическую мишень, являются длина генерируемой волны, плотность потока энергии и время воздействия. Биологические ткани неоднородны и являются интенсивно рассеивающими средами. Только поглощение лазерной энергии оказывает терапевтически значимое воздействие на ткани. Спектр поглощения воды, основного хромофора биологической ткани, лежит в среднем и дальнем инфракрасном диапазоне волн. Эрбиевый лазер имеет длину волны 2,90 мкм (средний инфракрасный диапазон), максимально поглощается водой, что и определяет его воздействие на биоткань без явлений коагуляции и аблации, в результате чего формируется обширная, но неглубокая зона прогрева [10, 11].
Таким образом, в настоящее время актуально проведение клинических исследований, направленных на изучение воздействия лазерной энергии на структуру коллагена, МПЭ влагалища и эпителий вульвы, как в репродуктивном возрасте, так в пери- и постменопаузе. Необходимо подтвердить эффективность и безопасность применения данного метода лечения, уточнить показания к применению и параметры процедур, а также определить длительность положительного эффекта.
Вопрос коррекции генитоуринарных расстройств у пациенток, перенесших лечение после онкологических заболеваний гениталий, особенно актуален, так как гормонотерапия им в ряде случаев противопоказана, или пациентки не намерены использовать гормоны, а хирургический метод лечения крайне нежелателен в связи с выраженным рубцовым процессом вследствие проведения соответствующего лечения.
Цель исследования — оценить эффективность применения эрбиевого лазера в лечении отдельных проявлений генитоуринарного менопаузального синдрома у онкогинекологических пациенток.
Материал и методы
В клиническом исследовании приняли участие 17 пациенток, перенесших комбинированное лечение (оперативное лечение в объеме экстирпации матки с придатками + лучевая терапия) рака тела матки I стадии в анамнезе 5 и более лет назад и имеющих стойкую ремиссию данного заболевания. Все пациентки наблюдались у онколога по месту жительства, регулярно проходили амбулаторное обследование. Диагноз на момент включения в исследование: пролапс тазовых органов I—II степени, смешанный тип недержания мочи (гиперактивный мочевой пузырь со стрессовым компонентом), стрессовое недержание мочи (СНМ), вульвовагинальная атрофия (ВВА). Средний возраст пациенток составлял 63,5±5,9 года. Исследование проводилось на базе гинекологического отделения ГКБ № 1 им. Н.И. Пирогова (Москва). Всем пациенткам до начала лечения был проведен стандартный комплекс обследований (гинекологический осмотр, исследование мазков отделяемого влагалища на микрофлору, цитологическое исследование на наличие атипичных клеток, ультразвуковое исследование органов малого таза, кашлевая проба). В доступной для пациенток и их родственников форме были разъяснены механизм действия лазерного излучения и этапы проведения процедур. Для оценки выраженности проявлений генитального пролапса и недержания мочи было проведено анкетирование пациенток с помощью опросника PFDI-20 (Pelvic Floor Disorders Distress Inventory), включающего три подраздела: симптомы пролапса тазовых органов (POPDI – Pelvic Organ Prolapse Distress Inventory–6), колоректально-анальные симптомы (СRAD – Colorectal Anal Distress Inventory–8), симптомы недержания мочи (UDI – Urinary Distress Inventory–6). Оценка симптомов ВВА проводилась с помощью VSQ (The Vulvovaginal Symptom Questionnaire), состоящего из 21 вопроса, на который можно ответить «да» или «нет». Также проводилось определение индекса вагинального здоровья (ИВЗ) в динамике. Для оценки трофики стенок влагалища проводили ультразвуковое исследование с цветовым допплеровским картированием изображения, а также соноэластографию в режиме реального времени на аппарате Toshiba Aplio 500 для определения плотности тканей. Статистическая обработка данных проводилась с помощью пакета программ Statistica 10.
Каждой пациентке было проведено 3 процедуры воздействия лазерным излучением на стенки влагалища, область преддверия и вульвы (плотность потока энергии в среднем составляла 10 Дж/см2): процедура IntimaLase (постепенное воздействие на стенки влагалища по направлению изнутри кнаружи пакетами из 4-х импульсов SMOOTH на каждый участок) и процедура IncontiLase (воздействие на стенки влагалища путем подачи лазерной энергии пакетами из 4-х импульсов SMOOTH на каждый участок, для следующего этапа – после замены адаптера двумя-тремя импульсами в каждой точке выполняется обработка преддверия влагалища и периуретральной зоны). Все пациентки возвращались к повседневной активности сразу после окончания процедур.
Напомним, что в нашем исследовании лечение YAG-лазером использовалось в качестве монотерапии и соответственно протоколу проведения процедур, предварительная подготовка препаратами эстриола и обезболивание не использовалось. При истонченном эпителии влагалища в перименопаузе, недостатке гликогена в клетках МПЭ, наличии атрофических изменений МПЭ влагалища, области преддверия влагалища и вульвы, ткани-мишени теряют количество хромофора (воды) и становятся более чувствительными. Раздражение терморецепторов воспринимается пациенткой, как болевое ощущение различной интенсивности, в связи с чем необходим подбор параметров воздействия в каждом конкретном случае (снижение плотности потока энергии до необходимого уровня Дж/см2). Так, при работе в области преддверия влагалища и вульвы в связи с жалобами пациенток на болевые ощущения (n=13, 76%), параметры потока энергии при первой процедуре были снижены до 6–8 Дж/см2, что не снижает эффективности терапии, не противоречит протоколу проведения процедур и мнению других исследователей [12—15]. В дальнейшем практически у всех пациенток (n=15, 88%) при проведении 2-й и 3-й процедур плотность потока энергии составляла 10 Дж/см2. Осложнений после проведения процедур отмечено не было.
 Результаты
Результаты
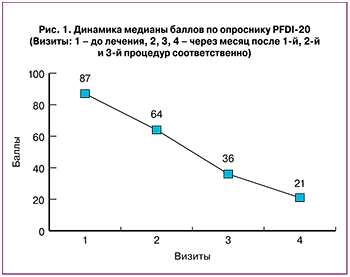
Анализ данных по опроснику PFDI-20 показал, что основные жалобы у пациенток были связаны именно с проявлением симптомов недержания мочи (подраздел UDI-6): учащенное мочеиспускание, потеря мочи по каплям, недержание мочи при кашле, смехе и т.д. Медиана баллов на первом визите до лечения составила 87 [67;105], после проведения терапии (через месяц после 3-й процедуры) было отмечено снижение медианы баллов до 21 [17;30], что свидетельствует о регрессии или исчезновении симптомов генитоуринарных расстройств после проведения 3-х сеансов воздействия лазерным излучением (рис. 1).
Данные подраздела UDI-6 (рис. 2) показали уменьшение всех симптомов дизурических расстройств, в особенности, более чем на 50% снижение частоты встречаемости в группе и выраженности таких симптомов, как недержание мочи при кашле, чихании или смехе (СНМ), учащенное мочеиспускание. Ноктурия (нарушение сна в связи с позывами к мочеиспусканию чаще одного раза за ночь) до лечения беспокоила 95% (n=16) пациенток, после проведенной терапии — 35% (n=6).
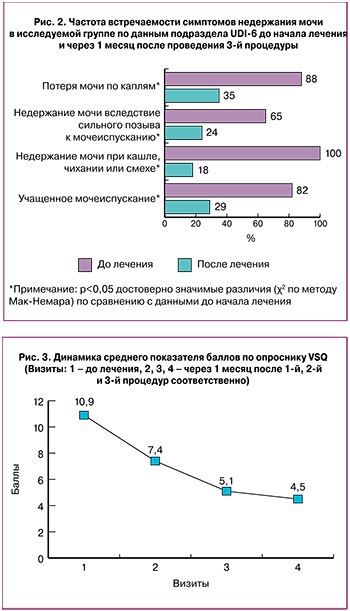 Оценка симптомов ВВА проводилась с помощью опросника VSQ (рис. 3). Максимальное количество баллов по опроснику – 20. Пациентки, отметившие «нет» на вопрос 17, на следующие 4 вопроса не отвечают. Средний показатель баллов в исследуемой группе до начала лечения составил 10,9±2,3, через месяц после проведения 3-й процедуры – 4,5±2,0 балла. Было выявлено снижение как частоты, так и интенсивности проявлений ВВА, в частности, таких как сухость, зуд и жжение во влагалище и в области преддверия более чем на 50%, по сравнению с данными до начала лечения (t-критерий Вилкоксона, p<0,05).
Оценка симптомов ВВА проводилась с помощью опросника VSQ (рис. 3). Максимальное количество баллов по опроснику – 20. Пациентки, отметившие «нет» на вопрос 17, на следующие 4 вопроса не отвечают. Средний показатель баллов в исследуемой группе до начала лечения составил 10,9±2,3, через месяц после проведения 3-й процедуры – 4,5±2,0 балла. Было выявлено снижение как частоты, так и интенсивности проявлений ВВА, в частности, таких как сухость, зуд и жжение во влагалище и в области преддверия более чем на 50%, по сравнению с данными до начала лечения (t-критерий Вилкоксона, p<0,05).
ИВЗ оценивался по 5 показателям по 5-балльной шкале: количество и качество отделяемого влагалища, pH, увлажненность, эластичность и толщина эпителия влагалища. Баллы распределялись следующим образом: 25—21 — здоровое состояние эпителия влагалища, 20—16 — незначительная атрофия, 15 и ниже — умеренные и значительные атрофические изменения влагалищного эпителия. ИВЗ от 21 до 25 баллов, характеризующий здоровое состояние влагалищного эпителия, наблюдался у 12% (n=2) больных до лечения. После проведенной терапии (через месяц после 3-й процедуры) ИВЗ составлял от 21 до 25 баллов у 76% (n=13) пациенток, у остальных 24% (n=4) — от 16 до 20 баллов, что говорит о нормализации уровня pH, уменьшении сухости, улучшении увлажненности эпителия влагалища (таблица).
Для определения упругости (или жесткости) стенки влагалища был использован современный метод – соноэластография в режиме реального времени, позволяющий определить степень уплотнения стенки влагалища с помощью внутриполостного влагалищного датчика с центральной частотой 6,0 мГц. При давлении на стенку влагалища вагинальным датчиком оценивается изменение частоты эхо-сигнала. На эластограмме по цветовой шкале плотная ткань изображается пурпурно-синим, а мягкая – красно-желтым цветом. Преобладание красно-желтого цвета свидетельствует о потере тканями эластичности. При оценке состояния стенок влагалища с помощью соноэластографии у 70% (n=12) пациенток (p<0,05) после лечения было отмечено повышение степени упругости стенок влагалища (преобладание синего цвета по цветовой шкале) по сравнению с данными до лечения, что косвенно свидетельствует о запуске процессов неоколлагеногенеза. При проведении контрольного ультразвукового исследования для оценки трофики тканей после лечения у 56% (n=10) пациенток наблюдалось увеличение количества визуализируемых сосудов в области влагалищной стенки (p<0,05), что подтверждает запуск процессов неоангиогенеза.

Обсуждение
В настоящее время в литературе имеются данные о проведении подобных научных работ, однако актуальность темы и необходимость проведения дальнейших исследований не вызывает сомнений.
В наше исследование были включены пациентки в постменопаузе, и был достигнут положительный результат лечения в отношении симптомов недержания мочи (более чем на 50% снижение частоты встречаемости и выраженности проявлений СНМ). Проспективное когортное исследование, проведенное в 2016 г. Lapii G.A. и соавт. [15], включало 85 пациенток, страдающих СНМ. Лечение проводилось лазером Er:YAG с длиной волны 2940 нм (XS Dynamis, Fotona, Slovenia). Авторы пришли к выводу, что соответствующее снижение баллов ICIQ-UI ≥ 30% может быть предсказано на основании возраста (менее 47,5 года), индекса массы тела (≤23,3), продолжительности выдержки перинеометра на начальном этапе (≥3,51 с) и показателей ICIQ-UI до вмешательства (≤10).
По нашим данным, после окончания терапии было отмечено улучшение тургора (у 70%) и трофики стенок влагалища (у 56%) по данным соноэластографии и цветового допплеровского картирования. В исследовании 2017 г. [16] авторы использовали технологию IncontiLase для лечения СНМ. Образцы биопсии влагалища до лечения показали дегенеративные и атрофические изменения в МПЭ, дезорганизацию фибриллярных структур, межклеточного матрикса и нарушения микроциркуляции. После воздействия Er:YAG-лазера авторами также были выявлены признаки неоколлагеногенеза и эластогенеза, очаги неоангиогенеза, снижение эпителиальной дегенерации и атрофии и увеличение популяции фибробластов, а также увеличение объемной плотности капилляров и толщины эпителиального слоя соответственно на 61,1 и 64,5%.
В другое исследование (Neimark A.I. и соавт., 2018) было включено 98 пациенток в возрасте 37—63 лет, которым было проведено лечение с помощью Er: YAG-лазера (Fotona, Slovenia) с использованием режима SMOOTH по поводу СНМ, генитального пролапса 0—2 степени. После проведенных процедур не было выявлено ухудшения состояния и побочных эффектов, как и в нашем исследовании. Анализ анкетирования PFIQ-7 и PISQ-12, а также урофлоуметрия показали высокие положительные результаты. По данным допплеровской флоуметрии, было получено улучшение кровотока в микрососудистом слое, что сопоставимо с нашими данными. Результаты биопсии стенки влагалища после воздействия лазера продемонстрировали явления неоангиогенеза [17].
Результаты, полученные в нашем исследовании, также можно соотнести с данными еще одного клинического исследования. Авторы включили в исследование [18] 114 пациенток в пременопаузальном периоде со СНМ и рандомизировали их в 2 равные группы. В 1-й группе проводили лечение в соответствии с протоколом IncontiLase (Er:YAG-лазер), во 2-й (плацебо) — без подачи лазерной энергии. Через 3 мес после лечения показатели в 1-й группе по опросникам ICIQ-UI SF, PISQ-12 и FSFI, а также данные перинеометрии (оценка функции мышц тазового дна) были значительно лучше, чем в контрольной группе. Пациентки, включенные в наше исследование, в анамнезе перенесшие комбинированное лечение рака тела матки I стадии, после воздействия лазерной энергии также указали на значительный положительный эффект в отношении проявлений СНМ по данным опросников.
Однако, несмотря на множество исследований, имеются и противоречивые мнения относительно эффективности воздействия лазерного излучения на состояние зрелого коллагена. Механические свойства проколлагена значительно хуже, а период полураспада зрелого коллагена настолько велик, что существенная модификация структуры молекулы в квази-физиологических условиях не может произойти в течение нескольких дней или недель после проведенной лазерной процедуры. Длительный положительный эффект не наблюдался ни в одном из известных клинических исследований. При проведении процедур синтез коллагена стимулируется не за счет физиологического неоколлагеногенеза, а в результате патологического фиброза, что является непосредственно эффектом фракционных методов омоложения [19].
На сайте FDA 30 июля 2018 г. была размещена информация для медицинских работников, выполняющих «вагинальное омоложение», косметические вагинальные процедуры или процедуры, предназначенные для лечения симптомов, связанных с менопаузой, недержанием мочи или сексуальной дисфункцией с использованием энергетических устройств, а также для пациентов, рассматривающих данный вид лечения. Устройства на основе энергии (радиочастотные или лазерные) получили разрешение FDA для общих гинекологических показаний. «Вагинальное омоложение» — это неточный термин, который используется для описания нехирургических процедур, предназначенных для лечения вагинальных симптомов и/или состояний (синдром релаксированного влагалища, вагинальная атрофия, боль во время полового акта, нарушения мочеиспускания, сексуальная дисфункция). Медицинским работникам рекомендуется помнить, что безопасность и эффективность энергетических аппаратов для выполнения так называемого «вагинального омоложения», косметических и лечебных вагинальных процедур не установлена, необходимо обсуждать преимущества и риски всех доступных вариантов лечения с пациентами [20].
В исследованиях Безменко А.А., Коваль А.А. [21] оценивалась эффективность лечения СНМ у пациенток репродуктивного возраста Er: YAG-лазером с проведением 2-х сеансов с интервалом в 28 дней. Данные магнитно-резонансной томографии, определение уровня экспрессии PDGFR-α, VEGF, а также Ki-67 как маркеров пролиферации, нашли свое функциональное отражение при оценке результатов уродинамического исследования, объясняя механизм удержания мочи после лечения эрбиевым лазером, а именно увеличение толщины стенки влагалища, образование нового коллагена и улучшение трофики ткани. Улучшение качества жизни также было выявлено при анализе данных различных опросников.
Заключение
Таким образом, применение энергии эрбиевого лазера для коррекции генитоуринарного синдрома является эффективным методом и может быть рекомендовано в качестве монотерапии при лечении стрессового и смешанного недержания мочи и ВВА у пациенток, перенесших лечение по поводу рака тела матки I стадии. Однако положительный эффект является краткосрочным, что требует, по-видимому, повторения курса процедур. Учитывая недостаток исследований в области применения селективного фототермолиза и влияния его на репаративные процессы эпителия влагалища и вульвы, необходимо регулировать параметры мощности (изменение плотности потока энергии) с учетом индивидуального статута пациенток (степень выраженности атрофических явлений, индивидуальная чувствительность, болевой порог), что не противоречит протоколу проведения процедур лазерного воздействия и не снижает терапевтической значимости метода, но избавляет от риска возможных осложнений.
Вопрос коррекции генитоуринарных расстройств у перенесших лечение по поводу онкологических заболеваний пациенток особо актуален, так как выбор методов лечения ограничен. Полученные нами результаты свидетельствуют, что использование лазерной энергии у данной категории пациенток возможно, но в состоянии ремиссии, после консультации с онкогинекологом и может быть рекомендовано в ряде случаев.



