На современном этапе проблема железодефицитных состояний и железодефицитной анемии (ЖДА) продолжает оставаться актуальной. Несмотря на возросший интерес врачей к этой патологии, большой арсенал лекарственных средств для лечения, разработку новых тестов и методов диагностики, число больных ЖДА неуклонно растет [1].
По данным ВОЗ, в мире, население которого сейчас приближается к 6 млрд человек, около 2 млрд страдают ЖДА, которая составляет 80% всех анемий [2]. Исследования ВОЗ и Мирового банка свидетельствуют о том, что ЖДА является третьей по распространенности причиной временной потери трудоспособности у женщин в возрасте 15–44 лет. По данным МЗ РФ, в России в 2000 г. было выявлено 1 278 486 случаев болезней крови и кроветворных органов, из них более 86% составили анемии [2, 3]. В отдельных группах населения частота встречаемости железодефицитных состояний достигает 50 и даже 70–80% [3–5]. Частота случаев анемии за последние 10 лет увеличилась более чем в 6 раз, причем чаще анемия встречается среди женщин детородного возраста, беременных и детей в возрасте 12–17 лет [6]. По данным официальной статистики МЗ РФ, из числа женщин, закончивших беременность в 1995 г., анемия была выявлена у 34,4%, а в 2000 г. у 43,9% [7].
Причины, приводящие к развитию ЖДА, многочисленны, в связи с чем клиницисту необходимо использовать все диагностические критерии, позволяющие установить истинную причину заболевания и выбрать обоснованную стратегию лечения [3, 8–10].
Анемия, изменяя гомеостаз материнского организма вследствие обменных, волемических, гормональных, иммунологических и других нарушений, способствует развитию акушерских осложнений [5, 11–13]. Частота их находится в прямой зависимости от степени тяжести анемии. Ранний токсикоз у пациенток с ЖДА развивается в 23–28% случаев; угроза прерывания беременности встречается в 12–15% случаев, а преждевременные роды – в 11–42%. С ЖДА связывают возрастающую частоту преждевременных родов и недоношенных детей. У беременных с дефицитом железа в 2–3 раза чаще, чем у женщин с нормальным уровнем гемоглобина (Hb), развивается приеэклампсия. Сочетание ЖДА и преэклампсии наблюдается у 14,5–50,0% женщин [14–19].
Метаболизм железа
ЖДА рассматривается как клинико-гематологический симптомокомплекс, характеризующийся нарушением образования гемоглобина вследствие дефицита железа в сыворотке крови и костном мозге и развитием трофических нарушений в органах и тканях.
Различают два вида железа: экзогенное (алиментарное), поступающее в организм только с пищей; эндогенное, которое содержится в организме в Hb, миоглобине, тканевых ферментах, плазме, в органах (печени, селезенке, костном мозге).
Обмен железа во время беременности
У женщин суточная потребность в железе составляет 1,5–1,7 мг, при обильных менструальных кровотечениях она возрастает до 2,5–3,0 мг. При потерях крови с выведением из организма более 2 мг железа в сутки развивается его дефицит. Однако при обильной менструации женщина за несколько дней может потерять 50–150 мг железа, а при наличии миомы матки, эндометриоза, гиперпластических процессов потеря может доходить до 500 мг. Для естественного восстановления запаса железа в организме после обильной менструации необходимо около 6 месяцев. Суточная потребность в железе в период беременности и нормально протекающих родов увеличивается в 2 раза, лактации – в 10 раз. К концу беременности неизбежно наступает обеднение железом организма матери в связи с депонированием его в фетоплацентарном комплексе (около 450 мг), увеличением объема циркулирующей крови (около 500 мг) и в послеродовом периоде в связи с физиологической кровопотерей в III периоде родов (150 мг) и лактацией (400 мг). Суммарная потеря железа, связанная с нормально протекающей беременностью, родами и лактацией, составляет около 1400 мг, и для ее восполнения требуется 2–3 года. Во время беременности значительная часть усвоенного железа поступает в плаценту, костный мозг, печень. В первом триместре беременности и частично во втором происходит увеличение запасов железа, о чем свидетельствуют показатели Hb: 120–135 г/л. Со второй половины беременности, особенно в третьем триместре и послеродовом периоде, содержание резервного железа снижается. Соответственно, ниже становятся и показатели Hb – от 118 до 122 г/л. Даже при физиологическом течении беременности и отсутствии признаков ЖДА концентрация сывороточного железа (СЖ) достоверно снижается. Во время гестации железо усиленно расходуется вследствие интенсификации обмена веществ: в первом триместре потребность в нем не превышает потребность до беременности, во втором – увеличивается до 2–4 мг, в третьем – возрастает до 10–12 мг/сут. За весь гестационный период на кроветворение расходуется 500 мг железа, из них на потребности плода – 280–290, плаценты – 25–100 мг. Процесс всасывания железа на протяжении беременности усиливается и составляет в первом триместре 0,6–0,8 мг/сут, во втором – 2,8–3, в третьем – до 3,5–4 мг/сут. Однако это не компенсирует повышенный расход железа, особенно в период костномозгового кроветворения плода (на 16–20-й неделе беременности) и увеличении массы крови в материнском организме. Уровень депонированного железа у всех беременных к концу гестационного периода снижается.
 У плода запасы железа создаются матерью: во время беременности она передает будущему ребенку через плаценту около 300 мг железа. Установлено, что принятое матерью железа уже через 40 минут появляется в плазме плода, а через два часа – в его эритроцитах. Плод расходует железо не только для своих эритроцитов, но и для собственного развития, а в последние два месяца беременности еще и для образования резервов в печени, селезенке и костном мозге. После рождения ребенок получает железо с грудным молоком. Если у кормящей матери в период беременности имелся некомпенсированный дефицит железа, то и в молоке будет отмечаться недостаточная его концентрация. Вместе с тем растущий ребенок потребляет большое количество железа, истощая, даже в норме, его запасы в собственном депо.
У плода запасы железа создаются матерью: во время беременности она передает будущему ребенку через плаценту около 300 мг железа. Установлено, что принятое матерью железа уже через 40 минут появляется в плазме плода, а через два часа – в его эритроцитах. Плод расходует железо не только для своих эритроцитов, но и для собственного развития, а в последние два месяца беременности еще и для образования резервов в печени, селезенке и костном мозге. После рождения ребенок получает железо с грудным молоком. Если у кормящей матери в период беременности имелся некомпенсированный дефицит железа, то и в молоке будет отмечаться недостаточная его концентрация. Вместе с тем растущий ребенок потребляет большое количество железа, истощая, даже в норме, его запасы в собственном депо.
Осложнения ЖДА у беременных и плода
На сегодняшний день получено достаточно подтверждений, что наиболее драматическим последствием анемии для здоровья человека является повышение риска материнской и детской смертности. При наличии ЖДА у беременных женщин могут возникнуть следующие осложнения: плацентарная недостаточность (18–24%); угроза невынашивания и преждевременных родов (11–42%); преэклампсия (40–50%), преимущественно отечно-протеинурическая форма; слабость родовых сил (10–15%); несвоевременное излитие околоплодных вод у каждой 3-й беременной; гипотоническое кровотечение (7–10%); послеродовые септические осложнения (12%); гипогалактия (39%).
Лабораторная диагностика ЖДА
Выделяют три последовательных этапа обеднения организма железа (по Гейнриху), для каждого этапа характерны определенные изменения лабораторных данных.
I. Прелатентный дефицит железа.
(Отсутствие анемии – гемоглобиновый фонд сохранен. Сидеропенический синдром не выявляется, уровень СЖ в норме, сохранен транспортный фонд. Снижены запасы железа в организме – снижение уровня ферритина).
II. Латентный дефицит железа.
(Сохранение гемоглобинового фонда железа – анемии нет, появление клинических признаков сидеропенического синдрома, снижение уровня СЖ, повышение общей железа-связывающей способности сыворотки (ОЖСС), эритроциты могут быть микроцитарными и гипохромными).
III. ЖДА.
Критерии постановки диагноза ЖДА
Диагноз ЖДА устанавливают на основании следующих критериев:
- Снижение уровня Hb, цветного показателя.
- Количество эритроцитов, как правило, снижено.
- Снижение уровня СЖ – гипоферремия.
- Повышение ОЖСС. Вычитая из ОЖСС уровень СЖ, определяют латентную железа-связывающую способность сыворотки (в норме – 28,8–50,4 мкмоль/л), при дефиците железа она повышена.
- Снижение насыщения трансферрина железом (НТЖ).
- Гематокрит свидетельствует о выраженности анемии, при которой, как правило, отмечается его снижение.
- Снижение уровня ферритина сыворотки является показателем уменьшения запасного фонда железа.
- Нередко выявляется тенденция к лейкопении, число тромбоцитов чаще нормально, при более выпаженной кровопотере возможен тромбоцитоз.
- Десфераловый тест (снижение выведения железа с мочой).
О роли фолиевой кислоты
Акцент на фолиевую кислоту (ФК) сделан не случайно. Результаты клинических исследований, проведенных в Венгрии, Великобритании, Франции, США и других странах, показали, что ежедневный прием женщинами в периконцепционный период по 4 мг ФК значительно снижает риск рождения у них детей с дефектами головного и спинного мозга, в частности с дефектом нервной трубки – самым распространенным и тяжелым пороком внутриутробного развития, формирующегося в первые 15 дней беременности. Данные о положительном влиянии ФК на предупреждение врожденных пороков развития получены и в России.
Некоторыми авторами отмечалось также положительное влияние ФК в снижении риска развития гестационной гипертонии (Amer. Jorn. of Epidemiology).
При недостатке ФК снижается способность клеток осуществлять синтез нуклеиновых кислот и продуцировать такие важные компоненты, как протеины, липиды и ДНК, что, в свою очередь, приводит к нарушению функции нормального деления клеток и тем самым провоцирует развитие врожденных пороков развития.
Принципы лечения и профилактики
В начале лечения ЖДА надо помнить о том, что воспалительные заболевания занимают в структуре гинекологической патологии первое место, и если у больной есть воспалительные заболевания органов малого таза, то перед началом антианемической терапии следует провести адекватную противовоспалительную терапию. В противном случае все железа, которое получит больная, будет стремиться в очаг воспаления. Биологический смысл этого процесса заключается в торможении деления железозависимых бактерий. Комплексная терапия ЖДА предполагает оптимизацию режима питания, назначение современных лекарственных средств, соблюдение трех последовательных этапов лечения [1, 6]:
- Купирование анемии.
- Терапия насыщения (восстановление запасов железа в организме).
- Поддерживающая терапия.
 Некоторые авторы предполагают, что ферротерапия должна длиться 6 и более месяцев, тогда как другие исследователи считают такой длительный прием железа неоправданным. Это связано с тем, что с развитием анемии происходит активация свободных радикалов, мешающая восстановлению интенсивности эритропоэза. При пониженном антиоксидантном потенциале длительное (больше 3 месяцев) использование препаратов железа с перегрузкой ими тканей способно усилить перекисное окисление липидов, вызвать гиперпродукцию свободных радикалов, в результате чего могут развиться оксидантный стресс, деструкция мембраны эритроцитов и как следствие – гемолиз [20–22]. В связи с этим рекомендуется проводить ферротерапию не более 3 месяцев.
Некоторые авторы предполагают, что ферротерапия должна длиться 6 и более месяцев, тогда как другие исследователи считают такой длительный прием железа неоправданным. Это связано с тем, что с развитием анемии происходит активация свободных радикалов, мешающая восстановлению интенсивности эритропоэза. При пониженном антиоксидантном потенциале длительное (больше 3 месяцев) использование препаратов железа с перегрузкой ими тканей способно усилить перекисное окисление липидов, вызвать гиперпродукцию свободных радикалов, в результате чего могут развиться оксидантный стресс, деструкция мембраны эритроцитов и как следствие – гемолиз [20–22]. В связи с этим рекомендуется проводить ферротерапию не более 3 месяцев.
На всех этапах лечения ЖДА должен осуществляться качественный мониторинг феррокинетических показателей с диспансерным наблюдением 2 раза в год. Именно такой режим диспансерного наблюдения эффективен и позволяет своевременно купировать рецидивы заболевания и предотвращать их развитие с помощью профилактических курсов ферротерапии, особенно в сложных ситуациях риска: при беременности, кормлении грудью, в климактерическом периоде, при присоединении инфекций. Такая тактика приводит к безрецидивному течению заболевания и выздоровлению.
При медикаментозном лечении и профилактике ЖДА во время беременности необходимо руководствоваться принципами ВОЗ, которые заключаются в следующем: все беременные с самого начала беременности (но не позднее 3-го месяца) и до родов должны получать 50–60 мг элементарного железа и 400 мкг ФК в сутки для профилактики ЖДА. Основное значение в профилактике имеет восполнение запасов тканевого железа. Адекватная профилактика уменьшает риск развития ЖДА при повторных беременностях. В случае выявления у беременной ЖДА суточная доза увеличивается в 2 раза. Заместительная терапия железом способствует повышению массы плода при рождении. Таким образом, адекватный подход к ведению беременных с ЖДА заключается в следующем:
- раннее выявление беременных группы риска по развитию анемии;
- тщательное обследование пациенток на наличие ЖДА и выявление ее причин;
- своевременная профилактика или лечение ЖДА с использованием специальной диеты и современных медикаментозных средств, подобранных индивидуально, с учетом феррокинетических показателей.
В настоящее время эксперты ВОЗ при лечении железодефицитных состояний рекомендуют:
- использовать пероральные лекарственные средства (удобство применения, лучшая переносимость);
- применять препараты Fe2+, а не Fe3+ как более эффективные (лучшая абсорбция). Важно помнить, что в отличие от препаратов с Fe2+, активность утилизации железа из препаратов, содержащих соли Fe3+, жестко лимитируется определенным уровнем рН желудочного сока;
- препараты с замедленным выделением Fe2+ (лучшая абсорбция и переносимость).
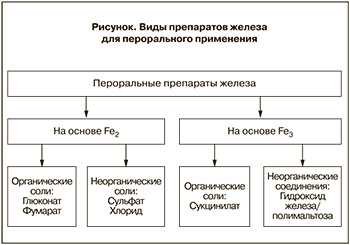
Органичность и валентность железосодержащих солей в препаратах для терапии ЖДА определяют эффективность и безопасность препарата (рисунок). В настоящее время доказано, что Fe2+ значительно превосходит по эффективности всасывания Fe3+ (уровень доказательности 1А). Биодоступность Fe2+ в несколько раз превышает Fe3+, что является одной из причин более быстрой нормализации уровня Hb и депо железа. Для всасывания Fe3+ должно восстановиться до Fe2+, после чего с помощью медь-зависимой ферроредуктазы, восстановленное Fe2+ поступает в энтероцит. Это основная причина, по которой препараты Fe3+ для достижения эффекта требуют не только более длительного применения, но и могут быть слабо эффективными в случае дефицита меди.
По данным ВОЗ и Британского общества гастроэнтерологов, терапия железодефицитных состояний у беременных, детей, пациентов с проблемами желудочно-кишечного тракта должна проводиться железосодержащими препаратами на основе фумарата, глюконата, либо других безопасных органических солей. Указание химической формы ферросоединений позволяет судить об уровне утилизации железа из различных лекарственных средств и ориентировочно судить о количестве активного (элементарного) железа в препарате (таблица).
Руководствуясь всеми перечисленными принципами, мы в своей практике для лечения и профилактики ЖДА широко используем препарат ферретаб комп.
Ферретаб содержит 163,56 мг железа фумарата (эквивалентно 152,1 мг сухого вещества, что эквивалентно 50 мг элементарного железа) и 0,54 мг фолиевой кислоты (эквивалентно 0,5 мг сухого вещества). Прием железа в виде фумарата обеспечивает быстрое восполнение его дефицита в организме, что ведет к постепенному исчезновению клинических и лабораторных признаков анемии. С точки зрения всасывания, усвояемости, переносимости данная соль железа (фумарат) наиболее физиологична из применяемых лекарственных препаратов железа. Фолиевая кислота является важнейшим фактором созревания мегалобластов, оказывает стимулирующее действие на эритропоэз. При беременности она оказывает антитератогенное действие. Существует взаимосвязь между фолатами и наличием дефектов нервных труб новорожденных, наиболее часто встречающимся из которых является spina bifida. Обеспечение фолиевой кислотой в период зачатия предупреждает приблизительно 70% дефектов нервных труб. Мы применяем ферретаб при ЖДА любой степени тяжести, обусловленной беременностью, миомой матки, аденомиозом, гиперпластическими процессами в эндометрии и другими гинекологическими заболеваниями. Для купирования легкой степени ЖДА ферретаб комп назначают внутрь, по 1 капсуле в день натощак, обильно запивая жидкостью. При выраженном недостатке железа или фолиевой кислоты необходимо увеличить дозу до двух или трех капсул в сутки. Поддерживающее лечение следует продолжать как минимум 4 недели после достижения нормального уровня Hb для нормализации ферритина сыворотки, отражающего запасы железа в организме. Терапия должна проводиться до нормализации картины крови (8–12 недель).
Терапия насыщения осуществляется, в зависимости от степени тяжести ЖДА, путем приема препарата по 1–2 капсуле в сутки. Учитывая то, что состав и структура препарата ферретаб обеспечивают его пролонгированное действие, для восполнения запасов железа поддерживающая терапия осуществляется, как правило, однократным приемом препарата в сутки. В каждой капсуле содержатся: 3 минитаблетки железа фумарата пролонгированного высвобождения и 1 минитаблетка фолиевой кислоты немедленного высвобождения. Минитаблетка фолиевой кислоты растворяется в течение нескольких минут и быстро всасывается в тощей кишке. В процессе пассажа минитаблетки железа через кишечник происходит непрерывное высвобождение и всасывание железа, что обеспечивает пролонгированное действие препарата и его однократный прием.
Длительность поддерживающей терапии зависит от наличия беременности и прогноза основного гинекологического заболевания. При продолжающихся меноррагиях ферретаб назначаем на 5–7 дней после окончания каждой менструации. При беременности препарат следует принимать в течение всего периода беременности и в течение 6 месяцев лактации. Ферретаб может быть использован и при лечении скрытого дефицита железа для восполнения запасов последнего. Препарат принимается по 1 капсуле в день под контролем показателей ОЖСС, СЖ, ферритина, уровня латентного дефицита железа. Продолжительность применения ферретаба по этому показанию, как правило, не превышает 4 недель.
Многими исследователями доказано, что добавление ФК ускоряет устранение ЖДА, мало того, пациентки с наиболее серьезными состояниями демонстрировали более заметные результаты.
Как уже говорилось выше, существенным требованием к препаратам железа для приема внутрь является удобство их применения, хорошая переносимость, что позволяет обеспечить высокий уровень приверженности больного назначенному лечению. Все эти требования абсолютно соблюдаются при лечении ферретабом. Ферретаб не оказывает неблагоприятного влияния на слизистую желудка. Железо встроено в инертный матрикс минитаблетки, что позволяет избежать высоких концентраций при высвобождении в желудке и препятствует раздражению слизистой. Всасывание железа происходит непосредственно в двенадцатиперстной кишке и верхних отделах тощей кишки. Действительно, ни в одном случае, не было зафиксировано непереносимости препарата, что обеспечивает высокий комплаенс к проводимой терапии, особенно у беременных. Беременные женщины представляют собой группу пациентов, которая нуждается в обеспечении железом и фолатами, потому что во время беременности у женщин наблюдается тенденция к появлению дефицита, как железа, так и фолатов. Следовательно, желательно соединить оба компонента в одной капсуле. Ферретаб комп. имеет уникальную лекарственную форму: капсулы пролонгированного действия, содержащие минитаблетки железа и фолиевой кислоты. Разработанная лекарственная форма позволила максимально учесть фармакокинетические особенности препаратов железа, повысить профиль безопасности и увеличить эффективность терапии.



