Прогнозирование начала преждевременных родов (ПР) представляет собой важную в практическом отношении проблему. Бессимптомное укорочение шейки матки встречается довольно часто, возникает по ряду независимых причин и не всегда приводит к ПР [1].
Длина шейки матки 25 мм или менее при оценке с помощью УЗИ ТВ имеет чувствительность 76%, специфичность – 68%, положительное прогностическое значение – 20% и отрицательный прогноз – 96% для идентификации ПР при одноплодной беременности в сроках менее 34 недели [2].
Для уточнения прогноза ПР целесообразно использовать диагностические тест-системы, основанные на определении различных биохимических маркеров в сочетании с оценкой длины шейки матки.
Положительный фетальный фибронектин (фФН) в цервикальном и/или вагинальном секрете связан с высоким риском ПР как у пациентов с наличием симптомов угрожающих родов, так и без них [3, 4], однако его определение не влияет на исходы родов. Так, недавно проведенный V. Berghella и соавт. мета-анализ, опубликованный в базе Кокрейна, включал 6 РКИ, 546 женщин с одноплодной беременностью. Авторы не выявили разницы между пациентками, которым выполнялся тест фФН с теми, у кого он не проводился. В обеих группах имела место аналогичная частота преждевременных родов при сроке беременности <37 недель (20,7% против 29,2%; относительный риск ОР=0,72; 95% ДИ: 0,52–1,01). Группы не различались по количеству женщин, которые рожали в течение 7 дней (12,8% против 14,5%; ОР=0,76; 95% ДИ: 0,47–1,21) и по сроку гестации (средняя разница, 0,20 недели, 95% ДИ: -0,26–0,67). Также не было разницы по частоте применения стероидов (29,2% против 29,2%; ОР=1,05; 95% ДИ: 0,79–1,39) и неонатальным исходам, которые включали респираторный дистресс-синдром (1,3% против 1,5%; ОР=0,91; 95% ДИ: 0,06–14,06) и поступление в отделение интенсивной терапии новорожденных (19,4% против 8,1%; ОР=2,48; 95% ДИ: 0,96–6,46). Менеджмент, основанный на тесте, требовал более высоких расходов на госпитализацию (средняя разница 153 долларов США; 95% ДИ: 4,01–281,99) [5].
Подчеркивается, что на сегодняшний день по-прежнему отсутствует консенсус, когда в диагностическом пути следует использовать тестирование фФН и как его следует сочетать с другими тестами, такими как измерение длины шейки матки. Это несоответствие создает непоследовательные оценки и вызывает путаницу [6].
Тест на определение фосфорилированного протеина-1, связывающего инсулиноподобный фактор роста (фПСИФР-1 – тест Actim Partus) предназначен для диагностики ПР или готовности к своевременным родам при неповрежденных плодных оболочках.
Однако указанный тест имеет ограниченную ценность в предсказании ПР (беременность сроком менее 32 недель, многоплодная беременность, наличие околоплодных вод в вагинальном секрете).
Было показано, что тест Actim Partus является полезным предсказателем досрочного рождения у женщин с симптомами, но его значение ограничено у бессимптомных женщин с высоким уровнем риска. Исследование для оценки использования этого теста в качестве прямого компаратора в сравнении с тестом фФН показало, что положительные и отрицательные предсказательные значения теста Actim Partus для ПР при беременности ≤37 недель составляли 0 и 70% соответственно, теста на фФН – 67 и 79% соответственно [7].
По результатам проспективного когортного исследования с участием 180 женщин с одноплодородной беременностью и с симптомами ПР, целым плодным пузырем и длиной шейки матки <25 мм на 24–34-й неделе беременности тест фПСИФР-1 имел низкую прогнозирующую эффективность для всех изученных результатов. После корректировки положительный тест фПСИФР-1 не был независимо связан с ПР в течение 7 дней (p=0,55), в отличие от длины шейки матки <15 мм (p=0,04). Авторы пришли к выводу, что тест сам по себе или в комбинации с УЗ-измерением шейки матки имеет низкую точность для прогнозирования ПР у женщин с симптомами [8].
Наиболее ценным с точки зрения прогностической ценности в настоящее время считают тест, основанный на определении плацентарного α-микроглобулина-1 (ПАМГ-1) в цервикальном секрете – тест PartoSure, отличающийся высокими значениями чувствительности и специфичности (таблица) [9].
Специфичность теста ПАМГ-1 возрастает до 100% у пациенток с длиной шейки матки менее 15 мм [10]. Установлено, что тест ПАМГ-1 статистически превосходит стандартную клиническую оценку в отношении специфичности [11].
Положительный тест ПАМГ-1 в 4 раза более надежен, чем положительный тест фФН для прогнозирования ПР в течение 7 дней (35,3% против 7,9%; р<0,05) и 14 дней (41,2% против 7,9%; p<0,05) [12].
Сравнительное исследование тестов ПАМГ-1 и фПСИФР-1 в исследовании M. Hadzi-Lega с соавт. показало, что тест ПАМГ-1 был положительным у 5,7% пациентов, тогда как фПСИФР-1 – у 29,8%. При этом чувствительность обоих тестов составила 100%, а специфичность – 83,3 и 50,0% (p≤0,05) с положительным прогнозом – 71,4 и 45,5% соответственно [13].
Разница в показателях обусловлена минимальной диагностической концентрацией белка-маркера, доступной для определения соответствующим тестом. Для фФН – это 40 нг/мл, фПСИФР-1 –10 нг/мл, а для ПАМГ-1 – всего 1 нг/мл. Поэтому частота ложноположительных результатов для ПАМГ-1 существенно ниже, а специфичность, отражающая долю отрицательных результатов, которые правильно идентифицированы как таковые, – выше. Данное положение было подтверждено в недавнем исследовании М. Ravi с соавт., показавшем, что сопоставимая прогностическая ценность тестов фФН и ПАМГ-1 (96 и 99% соответственно) была при наличии более высокой концентрации фФН – 200 нг/мл [14].
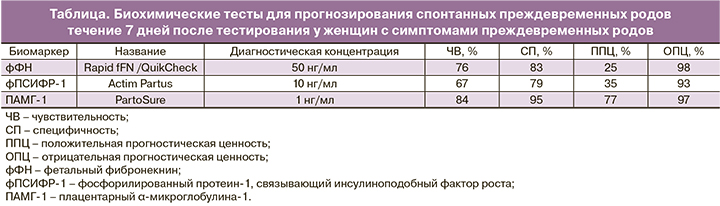
Систематический обзор и мета-анализ 2018 года, стратифицированный по риску ПР в течение 7 дней после тестирования, показал, что тест ПАМГ-1 имеет самые высокие положительные прогностические значения и коэффициент положительного правдоподобия во всех группах стратификации риска со статистической значимостью по сравнению с фФН и фПСИФР-1, а отрицательные прогностические значения и коэффициент отрицательного правдоподобия были одинаково высокими для всех трех биомаркеров [15].
L. Di Fabrizio с соавт. показали, что чувствительность и отрицательное прогностическое значение тестирования на ПАМГ-1 в отношении ПР через 7 дней у беременных женщин с длиной шейки матки 15–30 мм составляет 100%. Для прогноза ПР менее 34 недели отрицательное прогностическое значение оставалось высоким – 93% [16].
Таким образом, отрицательный тест на биомаркер ПАМГ-1 указывает на низкий риск ПР в течение следующих 1–2 недель и, следовательно, оказывает непосредственное влияние на выбор терапии. В этих случаях стандартная терапия, такая как РДС-профилактика и токолиз, не инициируется. Использование теста для определения ПАМГ-1 в дополнение к измерению длины шейки матки, по мнению C. Van Holsbeke с соавт. позволяет избежать ненужных госпитализаций и применения лекарственных средств в 71% случаев [17], а по результатам G. Lotfi с соавт. – до 91% [11].
Плацентарный α-микроглобулин-1 – это низкомолекулярный белок весом в 20000±2000 Да [18], который был найден в гистиоцитах амниотической, ворсинчатой и децидуальной тканях, в эндометрии, в гранулоцитах и в достаточно больших концентрациях в амниотической жидкости (2000–25000 нг/мл) [19–21].
ПАМГ-1 также можно обнаружить в цервикальном секрете в меньших концентрациях (0,05–2,0 нг/мл) [22]. Механизм и причины появления данного белка в цервикальном секрете до конца не изучены, но было установлено, что при наличии регулярных маточных сокращений либо при наличии воспалительных процессов в плодных оболочках, обусловленных, к примеру, инфекцией, концентрация ПАМГ-1 в цервикальном секрете повышается [19, 21].
S.M. Lee с соавт. предполагают две причины повышения концентрации данного белка в вагинальном секрете в случаях угрожающих преждевременных родов при интактном плодном пузыре: транссудация ПАМГ-1 через поры плодных оболочек при маточных сокращениях и деградация экстрацеллюлярного матрикса плодных оболочек вследствие воспалительного процесса, являющегося, в свою очередь, первопричиной угрожающих преждевременных родов [23].
Данный тест использует принцип иммунохроматографии и одобрен для применения в США (FDA, 11 апреля 2018 г.) [24].
Для проведения пробы не требуется использование влагалищного зеркала. Образец влагалищного секрета получают с помощью тампона, который помещают в пробирку с растворителем. Растворитель экстрагирует содержимое секрета в течение одной минуты, после чего тампон можно утилизировать. Затем тестовая полоска помещается в пробирку. Растворитель, содержащий антитела к ПАМГ-1 дифундирует в тестовую область полоски. В случае наличия ПАМГ-1 в пробе, он свяжется с антителами в тестовой зоне, образуя вторую полоску окрашивания. Результаты теста считываются через 5–10 минут после начала реакции.
Положительный результат теста PartoSure у беременных с симптомами угрожающих преждевременных родов с высокой вероятностью указывает на возможность наступления родов в течение 7 дней; отрицательный же результат – свидетельствует о малой вероятности наступления родов в течение 14 дней после проведения теста.
Клиническое исследование, выполненное T. Nikolova с соавт., с участием 101 пациентки с одноплодной беременностью между 20+0 и 36+6 неделями беременности с симптомами ПР, целым плодным пузырем и минимальным расширением шейки матки (≤3 см), показало, что при положительном тесте PartoSure самопроизвольные досрочные роды произойдут в течение 7 дней с высокой степенью точности (78,3%). ПР в течение 14 дней были крайне маловероятны (93,6%), если тест показал отрицательный результат [25].
Проспективное когортное исследование 100 женщин в период от 16 до 34 недель беременности с симптомами ПР и целым плодным пузырем было направлено на определение ПАМГ-1, который был обнаружен у 22,1% субъектов. Эти женщины чаще имели ПР до 7 дней, чем те, у кого не было обнаружено ПАМГ-1 – 31,6% против 7,5% соответственно (ОШ=5,6 95% ДИ: 1,5–21,6). Отрицательный прогноз составил 92,5%. Таким образом, авторы пришли к выводу, что наличие положительного результата теста на ПАМГ-1 связано с повышенной вероятностью ПР в течение 7 дней [26].
И.Ф. Фаткулиным с соавт. было установлено, что корреляция между длиной шейки матки (ДШМ) и наступлением родов тем сильнее, чем короче шейка матки и достигает своего диагностически значимого максимума при значении ≤15 мм. Использование теста на определение ПАМГ-1 в шеечно-влагалищном секрете улучшает прогнозирование исхода. При положительном результате теста у женщин с ДШМ ≤25 мм риск досрочных родов в течение 0–14 суток в 12,9 раза выше, чем у женщин с отрицательным результатом теста. Положительный результат теста более информативен и статистически достоверен, нежели факт укорочения шейки матки менее 25 и/или 15 мм. Показатели специфичности, по мнению авторов, выгодно отличаются в сторону теста на определение ПАМГ-1, практическая ценность которых еще раз подчеркивается значениями отношения правдоподобия и отношения шансов. Данная высокая специфичность приводит к уменьшению количества ложноположительных результатов. Однако, как считают исследователи, тест на определение ПАМГ-1 теряет свою информативность при условии, что ДШМ по данным УЗ-цервикометрии более 25 мм. Комбинированное применение метода УЗ-цервикометрии и теста на определение ПАМГ-1 приводит к повышению их диагностической эффективности [1].
Л.Д. Белоцерковцевой с соавт. дана оценка эффективности ранней диагностики цервикальной недостаточности (ЦН) и ее коррекции у беременных для профилактики сверхранних ПР. Обследовано 277 беременных женщин без клинических симптомов ПР с длиной цервикального канала <25 мм, которые были разделены на группы в зависимости от гестационного срока на момент выявления: в 14+0–17+6 (21,6%), в 18+0–21+6 (53,1%) и в 22+0–24+6 (25,3%) недель. Установлено, что женщины с длиной цервикального канала <25 мм в 14+0–17+6 недель беременности имеют более высокий риск самопроизвольного аборта, чем те, у кого это выявилось в 18+0–21+6. Однако выявление группы беременных, у которых роды произойдут в сроки 22+0–27+6 недель, только с помощью изучения анамнеза или данных УЗИ не всегда возможно. Поэтому в 41,5% случаях проводили тест для выявления ПАМГ-1. По мнению исследователей определение ПАМГ-1 в сроке гестации 14+0–21+6 недель дает важную информацию о перспективах получения жизнеспособного плода. Из 115 исследований теста в 25 случаях у беременных с ЦН получен положительный результат, и в 80% они родили до 28+0 недель гестации. У 90 беременных с ЦН получен отрицательный результат, и 70% из них родили в срок. Выявление положительного результата теста на ПАМГ-1 у беременных с ЦН в сроке 14+0–21+6 недель сопровождалось прерыванием беременности до 22 недель гестации в 73,7% против 6,4% у беременных с отрицательным результатом (р<0,0001). Родоразрешение в сроке 22+0–27+6 недель также происходило чаще (15,8 против 6,4%) среди беременных с положительным результатом теста ПАМГ-1. Интервал «тест – роды» у данных категорий беременных имеет достоверные различия по сравнению с беременными имеющими отрицательный результат теста: 7 дней против 133 (р<0,001). Выявление ЦН уже при первом скрининговом исследовании ставит перед врачом вопрос о дальнейшей тактике ведения. Опыт авторов продемонстрировал, что коррекция ЦН в сроке 14+0–17+6 недель может приводить к вынашиванию беременности до доношенного срока более чем у двух третей беременных (78,6%). Рождение детей в сроки 22+0–27+6 недель происходило всего лишь у каждой двадцатой пациентки. Использование акушерского пессария и хирургическая коррекция имеют сходную эффективность. При использовании коррекции ЦН достоверно реже происходит прерывание беременности до 22 недель гестации – 3,3% против 28,6% (ОШ=0,09; 95% ДИ 0,02–0,44). В то же время количество родов в срок при проведении коррекции ЦН встречается достоверно чаще – 72,5% против 28,6% (ОШ=6,60; 95% ДИ 1,90–22,98) [27].
А.Р. Ахметгалиев с соавт. поставили перед собой цель разработать алгоритм идентификации угрозы ПР, основываясь на статистическом и клиническом сравнении современных доступных диагностических тестов: УЗ-цервикометрии и экспресс-тест системы для определения содержания ПАМГ-1 в цервикальном секрете. Найдено, что женщинам с короткой шейкой матки по данным УЗ-цервикометрии целесообразно провести определение содержания ПАМГ-1 в цервикальном отделяемом. Положительным результат данного теста будет у пациенток, у которых вероятность родить в течение 14 сут. достигает 72,7%, а высокая прогностическая ценность отрицательного результата теста позволяет наблюдать пациенток в условиях женской консультации [28].
Информативность комбинированного применения теста ПАМГ-1 и УЗ-цервикометрии для определения риска ПР подтверждена в работе В.М. Болотских с соавт. При угрозе ПР тест был положительный в 100% случаев при длине цервикального канала ≤1,5 см, при этом в 75% произошли ПР, а интервал между датой теста и временем родов составил 18–44 ч. При длине цервикального канала от 1,5 до 3 (85%) только в 1 случае выявлен положительный результат теста, и интервал составил 140 ч [29].
На основании проведенных исследований были определены показания для применения: тест PartoSure предназначен для быстрой диагностики ПР в течение менее 7 дней у женщин с одноплодной беременностью с признаками и симптомами ПР, интактными плодными оболочками и минимальным раскрытием шейки матки (<3 см) между 24+0 и 34+6 неделями. Важным является также необходимость использования теста PartoSure в сочетании с другими клиническими данными – факторами риска и оценкой клинических данных и УЗ-цервикометрии [30].
Данные, полученные с помощью теста ПАМГ-1, могут значительно снизить экономическое бремя, вызванное ненужным поступлением и лечением пациентов, у которых подозреваются ПР. Сокращение использования кортикостероидов и токолитиков ведет к снижению краткосрочных и долгосрочных последствий для здоровья, связанных с использованием терапевтических препаратов, таких как кортикостероиды, антибиотики и токолитики [13].
Заключение
Таким образом, в настоящее время исследователи сходятся во мнении, что определение ПАМГ-1 является более надежным методом, чем определение фФН, фПСИФР-1 или измерение длины шейки матки и связано с сокращением расходов и ненужных медицинских вмешательств.



