В настоящее время известно, что эндометриоз поражает 5–10% женщин репродуктивного возраста и не менее ⅓ женщин с бесплодием [1]. По данным литературы, 25–50% инфертильных женщин страдают эндометриозом, а 30–50% женщин с эндометриозом имеют бесплодие [2]. Так, по данным Khine Y.M. и соавт. [3], частота эндометриоза у женщин с бесплодием увеличилась в настоящее время до 50%.
В исследовании Pantou A. и соавт. [4] было показано, что эндометриоз выявляется у 58% женщин, подвергшихся лапароскопии в качестве конечного этапа обследования по поводу бесплодия. Доля эндометриоз-ассоциированного бесплодия, по-видимому, имеет расовые и географические особенности, так, в Корее эндометриозом страдают всего около 20–30% женщин с бесплодием [5]. По данным Американского общества репродуктивной медицины [6], в 10% случаев эндометриоз является показанием для применения вспомогательных репродуктивных технологий (ВРТ).
В исследовании Huaying Yu. и соавт. [7] показана значительная частота спонтанной беременности (50,8%) у женщин с минимальным или легким эндометриозом, которая была значительно выше, чем в контрольной группе (35,6%, р=0,043).
В настоящее время абсолютно доказана взаимосвязь эндометриоза с бесплодием, но точная причина инфертильности при эндометриозе однозначно не определена. У некоторых женщин с эндометриозом беременность наступает без проблем, а у других требуется значительно больше времени для зачатия [1].
В настоящее время общепризнанным золотым стандартом в диагностике эндометриоза является лапароскопия [5, 8]. При проведении лапароскопии существует возможность и диагностировать заболевание, и одновременно провести лечение эндометриоидных гетеротопий [8]. Дополнительными преимуществами лапароскопической хирургии являются возможность завершить лечение во время процедуры, более низкая стоимость и временные затраты, меньшее количество побочных эффектов и осложнений, наступление преимущественно одноплодной беременности [9].
Многие исследования в настоящее время показали, что медикаментозное лечение при эндометриозе не улучшает фертильность [10–12]. Кокрановский обзор Hughes E. [10], включающий 23 испытания и более 3000 женщин, продемонстрировал отсутствие различий в показателях беременности с предшествующим подавлением овуляции оральными контрацептивами, прогестинами или даназолом у субфертильных женщин с эндометриозом, поэтому терапия этими препаратами может быть назначена только при лечении симптомов эндометриоза до и после беременности. Предварительная терапия этими препаратами не может улучшить фертильность, и, следовательно, их применение ведет только к отсроченному наступлению беременности. Согласно рекомендациям CNGOF-HAS Endometriosis Guidelines (Франция), NICE (Великобритания), ESHRE, гормональное лечение для подавления функции яичников не следует назначать для улучшения фертильности (степень А) [8, 13, 14]. Тем не менее комбинированный подход в лечении эндометриоз-ассоциированного бесплодия может иметь преимущества в ситуации наличия выраженных тазовых болей [8, 14].
Цель исследования – оценить клинические и социально-гигиенические особенности пациенток с эндометриоз-ассоциированным бесплодием и провести сравнительную оценку эффективности и комплаентности комбинированного подхода к его лечению с применением гестагена (диеногеста) и агониста гонадотропного рилизинг-гормона (аГнРГ).
Материалы и методы
Исследование одобрено Этическим комитетом Кемеровского государственного медицинского университета и проводилось на базе гинекологического отделения Кемеровского областного клинического перинатального центра им. Л.А. Решетовой в период с 2016 по 2018 гг. Дизайн исследования: рандомизированное открытое моноцентровое.
В исследование включены 150 пациенток с гистологически подтвержденным диагнозом эндометриоз-ассоциированного бесплодия. Критерии включения: бесплодие, гистологически подтвержденный диагноз эндометриоза, желание пациентки участвовать в исследовании и соблюдать протокол лечения. Критерии исключения: возраст моложе 18 и старше 45 лет, мужской фактор бесплодия, хроническая ановуляция, непроходимость маточных труб, тяжелые экстрагенитальные заболевания, наличие противопоказаний к медикаментозной терапии. Рандомизация проводилась в 2 группы методом «конвертов».
В 1-ю группу вошли 75 женщин, которым после проведения хирургического лечения эндометриоза (аблация и/или эксцизия) назначали аГнРГ бусерелин или диферелин в дозе 3,75 мг 1 раз в 28 дней в течение 3 месяцев внутримышечно (подкожно). Во 2-ю группу были включены 75 женщин, которым после хирургического лечения назначали гестаген (диеногест) в дозе 2 мг в сутки в течение 6 месяцев непрерывно.
После проведения лечения проводили оценку первичных и вторичных исходов. Первичные исходы: частота наступления беременности, частота регистрации сердцебиений плода в 12 недель, частота неразвивающейся беременности и живорождений оценивались через год после завершения лечения. Вторичные исходы: частота клинических проявлений эндометриоза (абдоминальный болевой синдром, дисменорея, диспареуния, кровотечения), а также частота побочных эффектов оценивались ежемесячно в течение 6 месяцев после оперативного лечения. Оценку степени тяжести болевого синдрома проводили согласно визуальной аналоговой шкале (ВАШ) боли (Huskisson E.С., 1974), оценку степени выраженности побочных эффектов – согласно числовой ранговой шкале (ЧРШ), состоящей из последовательного ряда чисел от 0 до 10. Пациентам предлагалось оценить свои ощущения цифрами от 0 (нет ощущений) до 10 (максимально возможные ощущения).
Методы обследования пациенток включали общеклиническое и специальное гинекологическое обследования, ультрасонографию (УСГ) органов малого таза аппаратом AlokaSSD 3500 (Япония), лапароскопию и гистероскопию с помощью эндоскопической техники фирмы KARL STORZ (Германия). Всем пациенткам перед включением в исследование проведены лапароскопия, коагуляция и/или иссечение очагов эндометриоза с гистологическим подтверждением диагноза.
Статистическую обработку полученных результатов производили с помощью пакета прикладных программ IMB SPSS Statistics 20. Характер распределения данных оценивали с помощью критерия Колмогорова–Смирнова. Количественные данные представлены в виде медианы (Me) и интерквартильного размаха (Q1–Q3), так как распределение величин в группах отличается от нормального. Сравнение двух независимых групп по одному или нескольким количественным признакам, имеющим хотя бы в одной из групп распределение, отличное от нормального, или если вид распределений не анализировался проводили путем проверки статистической гипотезы о равенстве средних рангов с помощью критерия Манна–Уитни. Для проверки различий между двумя сравниваемыми парными выборками нами применялся W-критерий Вилкоксона.
Для представления качественных признаков использовали относительные показатели (доли, %). Для оценки различий относительных величин использовали анализ таблиц сопряженности (χ2). При частотах меньше 5 применяли двусторонний точный критерий Фишера. Для сравнения относительных показателей, характеризующих связанные совокупности (до и после лечения), нами использовался тест Мак-Немара.
Для оценки эффекта воздействия каждого конкретного фактора на риск развития бесплодия применяли величину отношения шансов (ОШ). С целью проецирования полученных значений ОШ на генеральную совокупность нами рассчитывались границы 95% доверительного интервала [95% ДИ]. Критический уровень значимости – р2≤0,05.
Для определения численности групп использовалась формула Лера для относительных величин (определяет размер каждой сравниваемой группы):
При этом доверительная вероятность исследования выбрана 95%, ДИ 5%. Генеральная совокупность респонденток – пациенток с эндометриоз-ассоциированным бесплодием, получавших хирургическое лечение в гинекологическом отделении за год, была равной 246. Таким образом, требуемый размер выборки составил 150 пациенток.
Результаты
Основные характеристики женщин с эндометриоз-ассоциированным бесплодием, включенных в исследование, представлены в табл. 1.
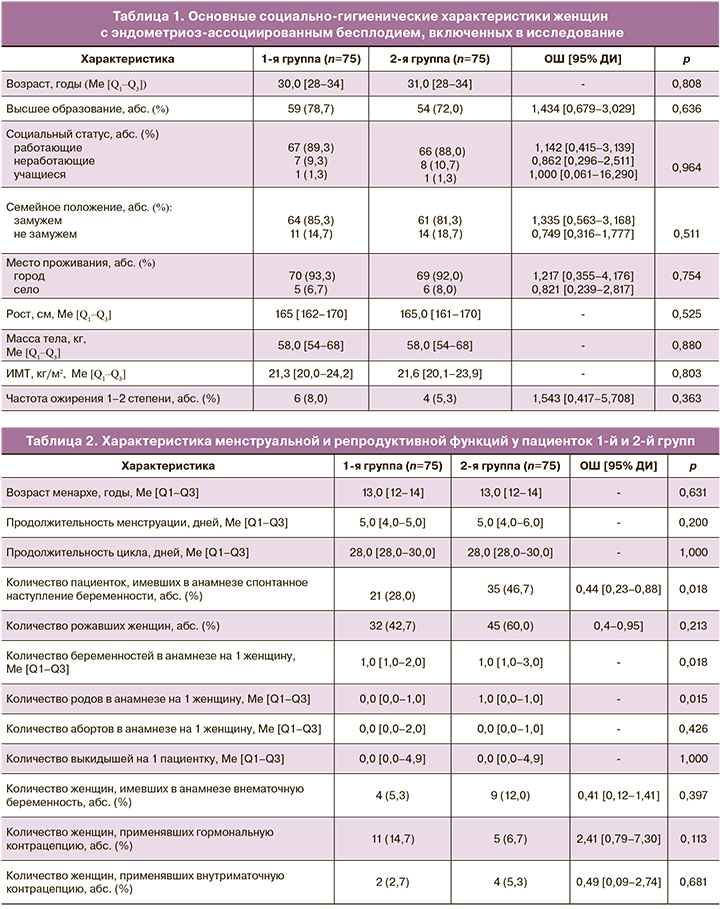
По основным социально-гигиеническим характеристикам пациентки с эндометриоз-ассоциированным бесплодием, включенные в 1-ю и 2-ю группы, статистически значимо не различались. Средний возраст женщин составил 30,0 и 31,0 года (р=0,808). Рост, масса тела, индекс массы тела (ИМТ), частота ожирения также существенно между группами не различались. Особенности менструальной и репродуктивной функций у пациенток, включенных в исследование, представлены в табл. 2.
По основным характеристикам менструального цикла (возрасту менархе, длительности менструального цикла и продолжительности менструации, количеству женщин, применявших гормональную и внутриматочную контрацепцию) пациентки обеих групп статистически значимо не различались. Во 2-й группе зарегистрировано большее количество женщин, имевших спонтанную беременность в анамнезе и большее количество беременностей и родов в расчете на 1 пациентку.
Частота клинических проявлений эндометриоза у пациенток обеих групп представлена в табл. 3.
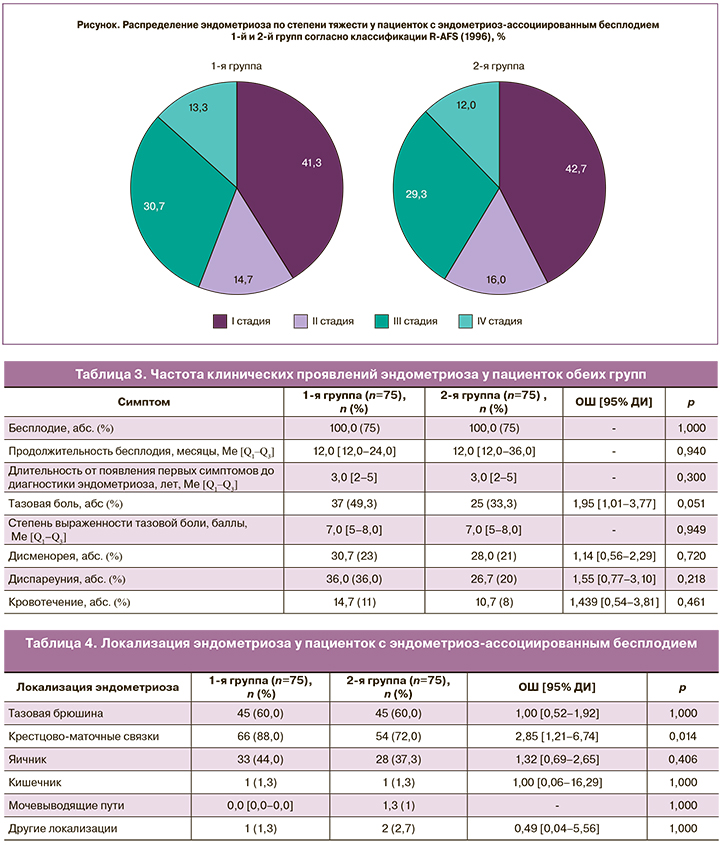
Все женщины в обеих группах страдали бесплодием продолжительностью в среднем 3 года (р=0,300). Частота синдрома тазовых болей статистически значимо не различалась между группами и составила 49,3 и 33,3% при одинаковой степени выраженности, оцениваемой в 7 баллов по шкале боли. Приблизительно ⅓ пациенток обеих групп страдали дисменореей и диспареунией, кровотечения имела каждая десятая женщина.
Распределение эндометриоза по степени тяжести, согласно классификации R-AFS (1996), у пациенток 1-й и 2-й групп не имело статистически значимых различий (р=0,987) и представлено на рисунке.
Почти половина пациенток 1-й и 2-й групп (45,3 и 45,3% соответственно), страдающих эндометриоз-ассоциированным бесплодием, имели III и IV стадии заболевания.
Локализация эндометриоза у пациенток с эндометриоз-ассоциированном бесплодием представлена в табл. 4.
Преимущественной локализацией очагов эндометриоза у бесплодных пациенток обеих групп были тазовая брюшина (60%), крестцово-маточные связки (88%) и яичник (44%). У пациенток 1-й группы имела место статистически значимо более высокая частота поражения крестцово-маточных связок (р=0,014).
Первичные исходы у пациенток с эндометриоз-ассоциированным бесплодием при комбинированном лечении с применением аГнРГ и диеногеста представлены в табл. 5.

Частота наступления беременности в течение года в обеих группах существенно не различалась и составила 53,3 и 54,7%, OШ 0,948 [0,49–1,80] (р=0,870). Частота регистрации сердцебиения плода в 12 недель и живорождения статистически значимо между группами не различались, однако у пациенток, получавших аГнРГ, имелась тенденция к увеличению частоты неразвивающейся беременности – в 17,3 и 9,3% случаев (OШ 2,04 [0,76–5,43]) и более низкой частоте живорождения (р=0,489).
Вторичные исходы лечения пациенток с эндометриоз-ассоциированным бесплодием с применением аГнРГ и диеногеста не имели статистически значимых различий и представлены в табл. 6.
В обеих группах зарегистрировано статистически значимое уменьшение частоты клинических проявлений заболевания. Бесплодие через год после отмены медикаментозной терапии отмечалось менее чем у половины женщин (р<0,001), дисменорея и диспареуния отсутствовали в обеих группах (р<0,001), частота кровотечений уменьшилась и наблюдалась только в 2,7% (р=0,003; р=0,002).
Частота побочных эффектов при лечении пациенток с эндометриоз-ассоциированным бесплодием с применением аГнРГ была, напротив, статистически значимо выше, чем при лечении диеногестом (табл. 7).
Клинически значимые побочные эффекты имели 69 (92%) пациенток, которым проводилось лечение аГнРГ, и 12 (16%) женщин, получавших лечение диеногестом (OШ 60,375 [21,387–70,441]; р<0,001). Наиболее значимыми побочными эффектами в 1-й группе были приливы 62 (82,7%), снижение либидо 56 (74,7%) и потливость 45 (60,0%), во 2-й группе – снижение либидо 30 (40%).
Обсуждение
В исследование были включены только пациентки с верифицированным гистологически диагнозом эндометриоз-ассоциированного бесплодия при исключении других форм инфертильности. Ранее несколько контролируемых испытаний показали снижение фертильности у женщин с эндометриозом в диапазоне от 2 до 10%. [1].
Результаты проведенного исследования показали, что почти половина женщин с эндометриоз-ассоциированным бесплодием имеют III–IV стадии эндометриоза. Преимущественной локализацией очагов эндометриоза у бесплодных пациенток обеих групп были тазовая брюшина, крестцово-маточные связки и яичник. Ранее проведенное исследование Meuleman C. и соавт. [15] показало, что у 37% пациенток с бесплодием, без предварительного хирургического диагноза эндометриоза, подвергшихся диагностической лапароскопии, выявляется III–IV стадия эндометриоза.
Несмотря на проведенную рандомизацию, пациентки 1-й группы имели статистически значимо более высокую частоту поражения крестцово-маточных связок – 66 (88%) (р=0,014), а пациентки 2-й группы – большее количество женщин со спонтанной беременностью в анамнезе и большее количество беременностей и родов в расчете на 1 пациентку. По остальным характеристикам группы были сходными.
В настоящее время общепринято, что хирургический и медикаментозные методы лечения эндометриоза не должны противопоставляться. Преимущества и недостатки каждого метода должны быть тщательно взвешены до начала лечения с учетом индивидуальных особенностей случая. Это позволит свести до минимума отрицательные результаты и, напротив, максимально достичь положительных [16]. Общепризнано, что медикаментозное лечение после операции не улучшает фертильность, однако все пациентки, включенные в исследование, имели проявления болевого синдрома (межменструальные тазовые боли, дисменорею, диспареунию), в связи с чем было принято решение о назначении медикаментозной терапии после проведения хирургического лечения.
После комбинированного подхода, включавшего хирургическое лечение (аблацию и/или эксцизию) очагов эндометриоза с последующей медикаментозной терапией аГнРГ или диеногестом, беременность в обеих группах спонтанно наступила более чем в половине случаев – 40–41 (53,3–54,7%). Проведенное ранее ретроспективное когортное исследование продемонстрировало значительно более низкую вероятность беременности в течение трехлетнего периода у пациенток с бесплодием, связанным с эндометриозом, по сравнению с пациентками, страдающими необъяснимым бесплодием (27 (36%) против 42 (56%), р<0,05) [1].
Вопрос комбинированного подхода к лечению эндометриоз-ассоциированного бесплодия до настоящего времени однозначно не решен и широко обсуждается в литературе. В исследовании, проведенном в Китае He L.Q. и соавт. [17], показано, что терапия аГнРГ после консервативной лапароскопической операции может значительно увеличить частоту наступления беременности у бесплодных женщин с умеренным или тяжелым эндометриозом. Однако доказано, что у пациенток с легкими формами эндометриоза терапия аГнРГ не улучшает прогноз. Первые 6 месяцев после лапароскопической операции или после прекращения лечения аГнРГ являются оптимальным временным интервалом для наступления беременности, а более длительное время от прекращения терапии связано с меньшей вероятностью спонтанной беременности.
Исследование случай-контроль, проведенное Yang Y. и соавт. на 130 пациентках, продемонстрировало преимущества комбинированного подхода в отношении обшей эффективности, частоты наступления беременности, частоты рецидивов, а также уровней сывороточных маркеров IL-17, IL-6 и TNF-α. Статистически значимой разницы в частоте побочных реакций между двумя группами выявлено не было (р=0,730) [18].
В исследовании Артымук Н.В. и соавт. [19, 20] показана сходная эффективность комбинированного подхода к лечению эндометриоз-ассоциированного бесплодия с применением диеногеста и аГнРГ после хирургического лечения. Частота спонтанной беременности в течение года составила около 23 (30,7%) в обеих группах, однако у пациенток, получавших аГнРГ, имелись значительные побочные эффекты, а также статистически значимо чаще регистрировалась неразвивающаяся беременность, что, вероятно, было обусловлено гипоэстрогенным влиянием препарата на эндометрий
В исследовании Muller V. и соавт. [21] у 144 пациенток после проведения цистэктомии по поводу эндометриомы, которым планировалось проведение экстракорпорального оплодотворения (ЭКО), были получены сходные результаты. После хирургического лечения пациентки были распределены в 3 группы: в одной группе был назначен диеногест, в другой – агонисты ГнРГ, третья группа женщин лечения не получала. В результате у пациенток, получавших диеногест, беременность была зарегистрирована в 2,5 раза чаще (44,7% против 16,7%, р=0,012), а частота родов была в три раза выше (36,8% против 11,1%, р=0,013) по сравнению с пациентками, получавшими аГнРГ.
В исследовании, проведенном Xue H. и соавт. [22], напротив, показаны преимущества при комбинированном подходе трипторелина перед гестриноном и мифепристоном. У пациенток, получавших трипторелин, была выше частота наступления беременности, меньше частота рецидивов при сходной частоте побочных эффектов. Тем не менее гормональную терапию антигонадотропинами большинство профессиональных ассоциаций не рекомендуют пациенткам с эндометриозом и бесплодием для увеличения шансов на самопроизвольную беременность, в том числе после операции [8, 13, 14].
Лечение эндометриоз-ассоциированного бесплодия должно быть междисциплинарным и учитывать наличие болевого синдрома, продолжительность бесплодия, общую оценку бесплодной пары, различные фенотипы эндометриоидных поражений, желание применять «агрессивные» методы лечения [23, 24].
Заключение
Таким образом, результаты проведенного исследования показали, что комбинированное лечение эндометриоз-ассоциированного бесплодия с применением хирургического метода (коагуляции и иссечения очагов эндометриоза) с последующим назначением аГнРГ или диеногеста является высокоэффективным в уменьшении клинических проявлений эндометриоза (тазовых болей, дисменореи, диспареунии, кровотечений). Спонтанная беременность наступает более чем у половины пациенток вне зависимости от типа медикаментозной терапии. У пациенток, получавших аГнРГ, зарегистрирована значительно более высокая частота побочных эффектов (92%), тенденция к большей частоте неразвивающейся беременности (17,3%) и меньшей частоте живорождений (82,7%), чем у пациенток, получавших диеногест. Для подтверждения преимуществ назначения гестагенов в комбинированной терапии пациенток с эндометриоз-ассоциированным бесплодием и тазовой болью требуется проведение дальнейших расширенных рандомизированных многоцентровых исследований.



