Необходимость сдерживания употребления антибактериальных препаратов озвучена Всемирной организацией здравоохранения (ВОЗ) два десятилетия назад и представлена в общемировой Глобальной стратегии борьбы с антибиотикорези- стентностью [1, 2].
Массовое «увлечение» антибактериальными препаратами запустило неуправляемый пандемический процесс формирования устойчивости возбудителей инфекционных заболеваний к применяемым антибактериальным препаратам. Данное явление приводит к многочисленным последствиям для общественного здравоохранения, в том числе и в экономической сфере. Это определило необходимость разработки Глобального плана действий по борьбе с устойчивостью к антимикробным препаратам, опубликованного ВОЗ в 2016 г. [3]. В числе пяти стратегических целей, провозглашенных в документе, озвучена необходимость оптимизации использования противомикробных препаратов в охране здоровья человека и животных. Создание эффективных и безопасных лекарственных средств отвечает данной глобальной цели.
Сегодняшние реалии подчеркивают актуальность сохраняющегося нерационального применения антимикробных препаратов. В документе ВОЗ указано, что только в Евросоюзе ежегодные потери от нескольких устойчивых штаммов составляют 25 тыс. человек. При прежних подходах к 2030 г. ВОЗ прогнозирует преждевременную гибель 100 млн человек, а к 2065 г. — 300 млн [4-7].
На фоне недостаточной активности в разработке новых антибактериальных средств и сохраняющегося роста антибиотикорезистентности перед акушером-гинекологом возникает сложная клиническая задача [8]. Патологические выделения из влагалища, сопровождающие большинство заболеваний генитального тракта, как правило, инициированы несколькими условно-патогенными типами возбудителей. Наиболее распространенным заболеванием, проявляющимся патологическими вагинальными выделениями, является бактериальный вагиноз (БВ), роль которого в увеличении риска гестационных осложнений, воспалительных заболеваний органов малого таза и рака шейки матки доказана многочисленными исследованиями [9, 10].
Наиболее распространенные способы коррекции нарушенной вагинальной микробиоты предполагают применение препаратов с антибактериальной активностью, клиническая эффективность которых ограничивается их воздействием на условнопатогенные микроорганизмы, снижения концентрации которых недостаточно для выздоровления. Антисептики и дезинфектанты, наряду с антибактериальными препаратами, не восстанавливают уровень облигатных представителей влагалищной микробиоты — лактобактерий, а значит, и оптимальный рН влагалищной жидкости. Применение для восстановления микробиоты влагалища препаратов, содержащих штаммы лактобацилл, зачастую также малоэффективно вследствие их низкой адгезивной активности к влагалищному эпителию [11].
Альтернативой антибиотикотерапии является восстановление эубиотического состояния влагалищной микробиоты селективными пребио- тиками — питательным субстратом для лактобацилл, состоящим из растительных полисахаридов. Данные полисахариды имеют структуру, схожую с гликогеном, синтезируемым влагалищными эпителиоцитами. Расщепляясь в процессе естественного
метаболизма, полисахариды остаются непригодным субстратом для других (условно-патогенных) представителей микробиоты влагалища. Дотация во влагалищный биотоп селективных пребиоти- ков сопровождается быстрым и существенным увеличением популяции индигенных лактобактерий, обладающих высокой адгезивной способностью к клеткам влагалищного эпителия. Продуцируемая лактобактериями молочная кислота создает при этом уровень рН (3,5—4,5), который является крайне неблагоприятным для размножения и вегети- рования условно-патогенной флоры (бактерии, грибы). Кроме того, бактериальная масса лактобацилл, проявляя свою высокую антагонистическую активность, синтезирует в высокой концентрации бактериоцины, которые оказывают прямое антимикробное воздействие на транзиторных представителей микробиоты влагалища. Совокупным результатом является существенное снижение титра условно-патогенной микрофлоры до физиологического уровня, что способствует восстановлению нормального соотношения представителей влагалищной микробиоты.
Цель исследования: представить собственный опыт клинической эффективности и комплаентно- сти монотерапии БВ вагинальным гелем (Вапигель) у пациенток репродуктивного возраста.
Материалы и методы
В исследование включены 30 пациенток в возрасте от 18 до 43 лет (средний возраст 29,4±4,5 года), обратившихся в амбулаторные лечебно-профилактические учреждения гинекологического профиля с жалобами на патологические выделения из влагалища, зуд/жжение, диспареунию.
На первом приеме выполнены: сбор анамнеза, осмотр шейки матки и влагалища в зеркалах, бимануальное гинекологическое исследование.
Для постановки предварительного диагноза БВ были использованы критерии Амселя: наличие гомогенных сероватых влагалищных выделений; рН вагинальной жидкости >4,5; наличие ключевых клеток по результатам микроскопии влагалищного мазка.
Для оценки состояния влагалищной микробиоты применяли исследование ПЦР и «Фемофлор-16» (оценка общего количества бактерий в материале, идентификация 16 показателей биоценоза урогенитального тракта: нормофлора — Lactob accillus spp., Gardnerella vaginalis, Prevotella bivia/ Porphyromonas spf., Ureaplasma (urealyticum+parvum), Mycoplasma hominis, Mycoplasma genitalium, Candida spp., Enterobacterium spp., Streptococcus spp., Staphylococcus spp., Streptococcus agalactia, Enterococcus spp., Atopobium vaginae, Sneathia spp./ Leptotrichia spp./Fusobacterium spp., Megasphaera spp./ Veillonella spp./Dialister spp., Lachnobacterium spp./ Clostridium spp., Mobiluncus spp./Corynebacterium spp., Peptostreptococcus spp.).
Забор влагалищного отделяемого производили при гинекологическом осмотре до проведения бимануального исследования. Соскоб выполняли стерильным одноразовым зондом, который помещали в пробирки с реагентом «Проба-Рапид» (ООО «НПО ДНК-Технология»). Предобработку, транспортировку и хранение материала, выделение ДНК проводили в соответствии с инструкцией к комплекту реагентов для выделения ДНК из биологического материала. Оценку количественного и видового состава представителей влагалищной микробиоты проводили до и после проведенной терапии.
Все диагностические методики в рамках проводимого исследования являлись рутинными, применяемыми в рутинной клинической практике, что определяло наблюдательный (неинтервенционный) характер исследования.
Критерии включения в исследование: репродуктивный возраст; БВ, подтвержденный на основании клинических и лабораторных данных; использование барьерных методов контрацепции во время участия в исследовании; информированное согласие пациентки на участие в исследовании и публикацию полученных результатов в соответствии с Правилами проведения качественных клинических испытаний в Российской Федерации (2020).
Критерии исключения: нарушения влагалищной микробиоты, обусловленные заболеваниями, передаваемыми половым путем (Chlamydia trachomatis, Trichomonas vaginalis, Neisseria gonorrhoeae, Mycoplasma genitalium, Cytomegalovirus, Herpes simplex virus 1, Herpes simplex virus 2); воспалительные заболевания органов малого таза на момент начала исследования; заболевания, требующие назначения антисептиков, антимикотиков, антибиотиков и бактериофагов на момент включения и менее чем за 30 дней до начала исследования; беременность и период лактации; отсутствие приверженности пациентки к терапии; непереносимость компонентов, входящих в состав препарата; одновременное участие в другом клиническом исследовании.
После гинекологического осмотра, бактериоскопии, рН-метрии влагалищной жидкости, оценки состояния влагалищной микробиоты (ПЦР и «Фемофлор-16») всем пациенткам назначали вагинальный гель (Вапигель) в соответствии с утвержденной инструкцией к препарату: по 1 тюбику ежедневно во влагалище в течение 10 дней.
После лечения оценивали клиническую и микробиологическую эффективность монотерапии БВ препаратом «Вапигель» по динамике субъективных симптомов БВ (неприятный запах, зуд/жжение, патологические влагалищные выделения, диспаре- уния); критериям Амселя; изменению состава вагинальной микробиоты по данным теста «Фемофлор».
Для оценки безопасности терапии анализировали нежелательные явления в динамике лечения, их связь с приемом препарата и выраженность. Для оценки комплаентности всего курса лечения каждую пациентку просили оценить удобство использования препарата Вапигель по шкале комплаентности Мориски—Грина.
Исследование одобрено Этическим комитетом ФГБОУ ВО «Рост ГМУ» Минздрава России (Протокол №16/6 от 02 ноября 2020 г.).
Результаты и обсуждение
Характерные для БВ патологические выделения из половых путей с неприятным «рыбным» запахом отмечали до лечения все женщины (100%), включенные в исследование. Зуд и жжение в интимной зоне до лечения были у 25/30 больных (83,3%), диспареуния — у 17/30 пациенток (56,7%) (рис. 1).

По итогам монотерапии БВ Вапигелем отмечалась положительная динамика субъективных клинических симптомов, характеризующаяся снижением частоты жалоб больных на патологические выделения из половых путей: отсутствие таковых отметили 25/30 пациенток (83,3%). Только 5/30 больных (16,7%) отмечали прежний характер влагалищных выделений. Удобство применения препарата и ощущение комфорта, отмечаемое большинством женщин, обеспечивали стабильное психоэмоциональное состояние, что формировало приверженность к лечению. После лечения Вапигелем ни у одной из женщин не сохранялись жалобы на наличие неприятного запаха; зуд и жжение в интимной зоне сохранялись только у 1/30 пациенток (3,3%), прежний дискомфорт при половых контактах отмечали 3/30 больных (10%).
После оценки субъективных признаков БВ проводили объективный осмотр и лабораторную диагностику с использованием критериев Амселя до и после лечения (рис. 2).
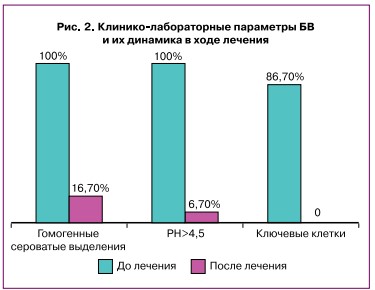
При объективном осмотре до лечения наличие гомогенных сероватых влагалищных выделений выявляли у всех пациенток (рис. 2). Кислотность влагалищной жидкости (рН) >4,5 отмечена у 30 (100%) женщин. Наличие «ключевых клеток» по результатам микроскопии до лечения выявлено в 26/30 образцов (86,7%).
После проведенного лечения характерные для БВ гомогенные влагалищные выделения сохранялись только у 5/30 пациенток, уровень рН>4,5 — у 2/30 больных (6,7%). Большинство участниц проведенного исследования отмечали быстрое купирование имеющихся ранее симптомов заболевания. Патогномоничный для БВ признак — «ключевые клетки» после монотерапии Вапигелем не обнаруживали.
У всех 30 участниц исследования до лечения выявлены количественно низкие концентрации (менее 105 КОЕ/мл) Lactobacillus spp., значимый уровень количества факультативно-анаэробных и облигатно-анаэробных микроорганизмов (таблица). После монотерапии Вапигелем частота обнаружения Lactobacillus spp. в концентрации 107 КОЕ/мл увеличилась до 86,6% (у 26/30) пациенток, а доля больных с клинически значимым количеством факультативно-анаэробных и облигатно-анаэробных микроорганизмов существенно снизилась (таблица).

Оценка комплаентности всего курса лечения показала высокую приверженность пациенток к применению Вапигеля: 25/30 пациенток (83,3%) набрали 4 балла по шкале комплаентности Мориски—Грина, что свидетельствовало о достижении цели лечения у большинства больных. В ходе исследования нежелательных явлений не выявлено ни у одной из 30 больных.
Рецидив клинических симптомов БВ в течение месяца после проведенной монотерапии БВ Вапигелем отметила только 1/30 пациенток (3,3%). Диспареуния и повышенный уровень pH влагалищного отделяемого у 3/30 больных (10,0%) потребовали продления основного курса лечения Вапигелем до 3 недель (1-2 раза в неделю).
Заключение
Результаты исследования показали, что применение Вапигеля — комплексного препарата, содержащего молочную кислоту и растительные полисахариды, устраняет субъективные жалобы и объективные клинические симптомы БВ (обильные влагалищные выделения, зуд/жжение, неприятный запах), восстанавливает оптимальные значения pH, формирует естественную среду для вегетирования эндогенных лактобактерий и сопровождается низкой частотой рецидивов заболевания.
Отсутствие нежелательных явлений и отказов от лечения, наряду с высокой эффективностью, демонстрирует безопасность, высокую комплаен- тность и целесообразность применения Вапигеля в качестве монотерапии БВ у женщин репродуктивного возраста как важного компонента в реализации мероприятий по сокращению назначения антимикробных препаратов в клинической практике.



