На сегодняшний день проблема бесплодия является одной из наиболее острых в сфере репродуктивного здоровья. Согласно данным Всемирной организации здравоохранения, заболевание касается от 48 млн пар до 186 млн человек в мире [1]. Следует отметить, что женское бесплодие наблюдается в 50–80% случаев. В разных регионах Российской Федерации частота бесплодия составляет от 17,2 до 24% и не имеет тенденции к снижению [2].
Для лечения женского бесплодия активно используются вспомогательные репродуктивные технологии (ВРТ). Их эффективность определяет ряд факторов – возраст пациенток, состояние эндометрия, качество и количество получаемых ооцитов и другие. Нужно подчеркнуть, что недостаточный ответ яичников на стимуляцию гонадотропинами может отмечаться и у молодых женщин с нормальным овариальным резервом. Такой неожиданный и неблагоприятный исход лечения служит причиной отмены цикла терапии, приводит к увеличению числа попыток ВРТ, что повышает медицинские риски и экономические издержки.
Одним из факторов, определяющих качество и количество получаемых ооцитов, служит состояние эндотелия, клетки которого синтезируют ряд биологически активных веществ, участвующих в регуляции работы репродуктивных органов. При эндотелиальной дисфункции, сопровождающей некоторые патологии репродуктивной системы, наблюдается увеличение образования вазоконстрикторов (эндотелин-1) и уменьшение количества вазодилататоров, например, оксида азота (NO), который продуцируется NO-синтазами (NOS). Показано, что у женщин с синдромом поликистозных яичников (СПКЯ) в гранулезно-лютеиновых клетках в 2,2 раза повышается экспрессия мРНК эндотелина-1 по сравнению с женщинами с нормальной овуляцией [3]. В метаанализе, проведенном Meng C. (2019), выявлено, что у пациенток с СПКЯ снижается уровень нитритов в сыворотке крови относительно данных контрольной группы [4].
В этой связи исследование вазорегулирующих факторов, продуцируемых эндотелием, у женщин, проходящих лечение бесплодия методами ВРТ, будет способствовать повышению эффективности ВРТ и увеличению частоты наступления беременности у пациенток с бедными и субоптимальным ответом.
Цель: исследовать содержание вазоактивных факторов эндотелия – эндотелина-1 и конечных метаболитов оксида азота в крови и фолликулярной жидкости, а также уровень эндотелиальной и индуцибельной NO-синтаз (eNOS и iNOS) в кумулюсных клетках у женщин с различными исходами гормональной стимуляции яичников при лечении бесплодия методами ВРТ.
Материалы и методы
Было проведено простое открытое сравнительное клиническое испытание в параллельных группах с участием 71 женщины Волгоградской области, проходящих лечение бесплодия методами ВРТ в Клинике №1 ФГБОУ ВО ВолгГМУ Минздрава России (Волгоград, Россия). Средний возраст составил 34,79 (4,26) года.
Критерии включения: возраст от 18 до 42 лет (включительно), уровень антимюллерова гормона (АМГ) более 1,2 нг/мл, наличие письменно оформленного добровольного информированного согласия на участие в клиническом испытании, протокол стимуляции с антагонистами и гонадотропинами в дозе не менее 100 МЕ в сутки.
Критерии исключения: возраст менее 18 и более 42 лет, «мягкие» протоколы стимуляции яичников, отказ от участия в клиническом испытании.
Дизайн исследования
У пациенток, проходящих лечение бесплодия методами ВРТ, перед стимуляцией были собраны данные о показателях овариального резерва, включающие оценку уровня АМГ и фолликулостимулирующего гормона.
Гормональная стимуляция яичников назначалась врачами Клиники №1 ФГБОУ ВО ВолгГМУ Минздрава России (Волгоград, Россия) в соответствии с клиническими рекомендациями, стандартами и интересами пациента. Были включены случаи гормональной стимуляции яичников, которая проводилась с применением протокола с антагонистами с использованием препаратов гонадотропинов (фоллитропин альфа или фоллитропин бета) в ежедневной дозе не менее 100 МЕ до достижения преовуляторными фолликулами диаметра от 17 мм с последующим введением триггера финального созревания в стандартных дозах препаратом хорионического гонадотропина.
После получения кумулюс-ооцитарных комплексов была проведена оценка результатов гормональной стимуляции: методом микроскопии произведен подсчет кумулюс-ооцитарных комплексов, определено количество зрелых ооцитов. В дальнейшем полученные ооциты использовались в рамках стандартной процедуры экстракорпорального оплодотворения или интрацитоплазматической инъекции сперматозоида в соответствии с клинической ситуацией и интересами пациента.
По результатам стимуляции были сформированы группы:
1) женщины с высоким и нормальным ответом яичников – получено 10 и более ооцитов (контрольная группа);
2) женщины с субоптимальным ответом яичников – получено 5–9 ооцитов;
3) женщины с бедным ответом – получено 4 и менее ооцитов.
Однократный забор крови из локтевой вены, фолликулярной жидкости и кумулюсных клеток производили с 8:00 до 11:00 утра. После венепункции, которая выполнялась в рамках подготовки к стандартному анестезиологическому пособию, кровь помещали в стерильные пробирки без антикоагулянта. Далее пробы центрифугировали 20 минут при 1000g и комнатной температуре. Фолликулярная жидкость и кумулюсные клетки не применяются в процедуре оплодотворения, а являются побочным продуктом, который обычно утилизируется после получения кумулюс-ооцитарных комплексов. Пробирку с фолликулярной жидкостью и кумулюсными клетками центрифугировали 20 минут при 1000g. Далее отбирали фолликулярную жидкость, а кумулюсные клетки отмывали 3 раза в охлажденном фосфатно-солевом буферном растворе (pH=7,0–7,2) («Иммунотэкс», Россия). После этого производили подсчет клеток в камере Горяева согласно стандартной методике [5] и лизировали клетки с использованием Lysis Buffer 1 Specific for ELISA (Cloud-Clone Corp., США) и Lysis Buffer 2 Specific for ELISA (Cloud-Clone Corp., США) для определения eNOS и iNOS соответственно.
Собранные после центрифугирования сыворотку, фолликулярную жидкость и лизаты помещали в пробирки типа эппендорф и замораживали при -20°С до момента проведения анализа. Для количественной оценки методом иммуноферментного анализа уровня эндотелина-1, а также количества eNOS и iNOS использовали наборы ELISA Kit for Endothelin 1 (Cloud-Clone Corp., США), ELISA Kit for Endothelial NOS (eNOS) (Cloud-Clone Corp., США) и ELISA Kit for Nitric Oxide Synthase 2, Inducible (NOS2) (Cloud-Clone Corp., США) соответственно. Оптическую плотность определяли на планшетном спектрофотометре SPECTROstar Nano (BMG Labtech, Германия) при длине волны 450 нм.
Для определения концентрации конечных метаболитов оксида азота – нитрит- и нитрат-ионов в сыворотке крови и фолликулярной жидкости использовали скрининг-метод в модификации Метельской В.А. и Гумановой Н.Г. [6], который основан на одновременном восстановлении нитратов в нитриты с помощью хлорида ванадия (III) (Sigma, США) и реакции диазотирования нитритом сульфаниламида с развитием окраски раствора и последующей спектрофотометрией при 540 нм.
Дизайн клинического испытания был одобрен локальным этическим комитетом ФГБОУ ВО ВолгГМУ Минздрава России, протокол №049 от 13 февраля 2023 г. Все женщины, принимавшие участие в клиническом испытании, дали письменное добровольное информированное согласие на участие.
Статистический анализ
Статистическую обработку данных проводили с помощью пакета программ GraphPad Prism 8 (GraphPad Software, США). Нормальность распределения проверяли по критерию Шапиро–Уилка. При нормальном распределении изучаемых параметров использовали критерий Тьюки, при распределении, отличном от нормального, – тест Крускала–Уоллиса с пост-хок-тестом Данна. Кроме того, была проведена оценка равенства дисперсий (equal SDs) – при различии дисперсий использовали Brown–Forsythe и Welch tests. Статистически значимыми считали различия при р<0,05. Данные, подчиняющиеся нормальному распределению, представлены в виде М (SD), где М – среднее арифметическое значение, SD – стандартное отклонение. Описание непараметрических данных проводилось с помощью медианы (Ме) и нижнего-верхнего квартилей (Q1; Q3). Для оценки клинического эффекта использовали разность средних с 95% ДИ для данных, распределенных по нормальному закону, и разность медиан с 95% ДИ (оценка Ходжеса–Лемана) для непрерывных данных, распределенных непараметрически.
Результаты
У женщин всех групп, проходящих лечение бесплодия методами ВРТ, уровень АМГ превышал 1,2 нг/мл. Тем не менее наблюдался разный ответ на стимуляцию овуляции гонадотропинами. Было выявлено, что у пациенток с бедным и субоптимальным ответом данный показатель был статистически значимо меньше по сравнению с контрольной группой. Другие показатели овариального резерва – количество пунктированных фолликулов, кумулюс-ооцитарных комплексов и полученных зрелых ооцитов – также были существенно ниже во 2-й и 3-й группах относительно показателей женщин с высоким и нормальным ответом (табл. 1).
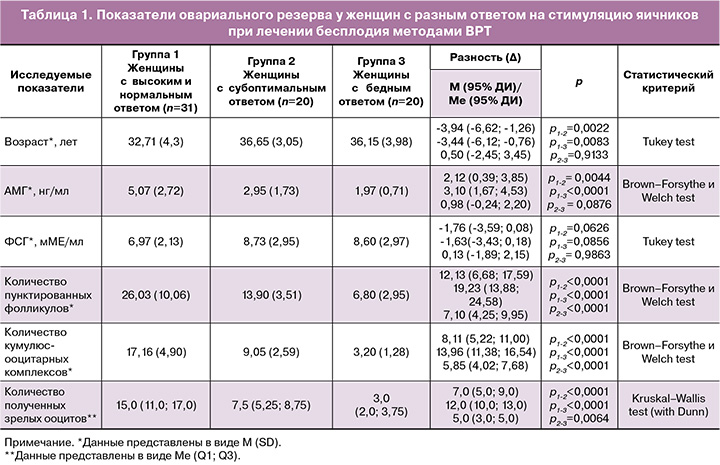
При исследовании уровня эндотелина-1 в сыворотке было обнаружено, что его количество у женщин с бедным ответом было статистически значимо больше по сравнению с контрольной группой. При этом концентрация конечных метаболитов NO в крови у женщин 3-й группы также была значительно выше относительно данных пациенток с высоким и нормальным ответом.
Статистически значимых различий в уровнях эндотелина-1 и конечных метаболитов NO в фолликулярной жидкости между группами выявлено не было (табл. 2).
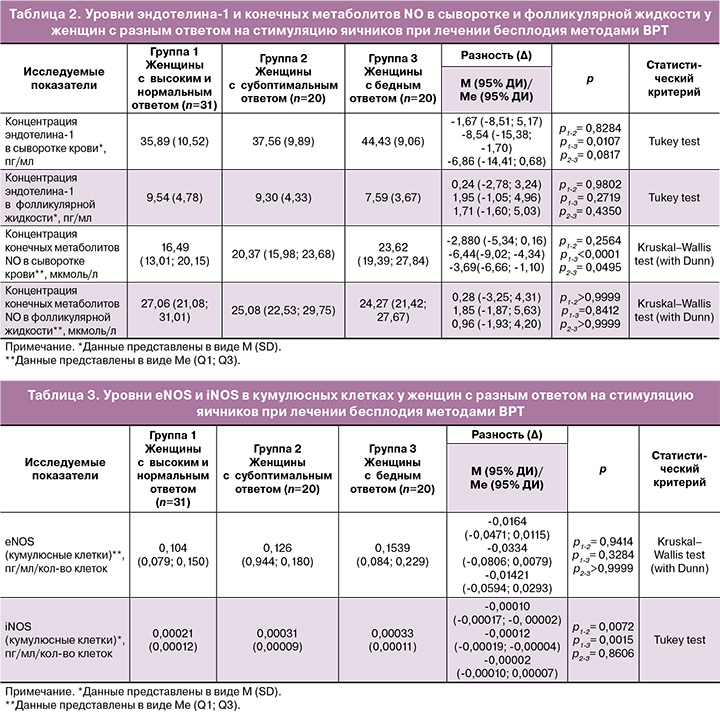
Уровень iNOS в кумулюсных клетках у женщин с субоптимальным и бедным ответом был статистически значимо больше по сравнению с контрольной группой (табл. 3), что в совокупности с повышенной концентрацией конечных метаболитов NO в сыворотке крови может свидетельствовать об образовании сильного окислителя пероксинитрита, способного вызывать необратимые повреждения в клетках у пациенток с бедным ответом.
Обсуждение
Сосудистый эндотелий принимает участие в регуляции функционирования женской репродуктивной системы. Было показано, что совместное культивирование эндотелиальных клеток-предшественников человека с ооцитами увеличивало скорость созревания последних и образования бластоцист за счет модуляции экспрессии генов, участвующих в увеличении количества кумулюсных клеток, формировании ооцитов и апоптозе [7]. В экспериментальном исследовании Man L. et al. (2018) было выявлено, что совместная трансплантация экзогенных эндотелиальных клеток (ExECs) с криоконсервированной тканью яичников в модели ксенотрансплантата мыши увеличивала объем и улучшала развитие антральных фолликулов. Кроме того, экзогенные эндотелиальные клетки, экспрессирующие AМГ, способствовали сохранению покоящихся примордиальных фолликулов [8].
При эндотелиальной дисфункции отмечается изменение уровня вазоактивных факторов, принимающих участие в регуляции работы женской репродуктивной системы. Одним из таких веществ является эндотелин-1, который продуцируется, в том числе, женскими половыми железами. При его взаимодействии с соответствующими рецепторами типа А наблюдается пролонгированная вазоконстрикция, в то время как активация эндотелинового рецептора типа В ассоциирована с расширением сосудов через индукцию сигнальных путей NO [9]. Изменение экспрессии эндотелина-1 ассоциировано с развитием СПКЯ. Было обнаружено, что в гранулезно-лютеиновых клетках у женщин с этим синдромом, проходящих процедуру ЭКО, экспрессия мРНК эндотелина-1 была увеличена более чем в 2 раза относительно контрольной группы [3].
В нашей работе сывороточная концентрация эндотелина-1 была статистически значимо больше у женщин с бедным ответом по сравнению с группой пациенток с нормальным и высоким ответом.
NO – молекула, которая участвует во многих физиологических процессах женской репродуктивной системы, включая развитие фолликулов, контроль стероидогенеза в яичниках и мейотического созревания кумулюс-ооцитарных комплексов [10]. Было показано, что NO играет ключевую роль в поддержании качества ооцитов [11]. Согласно полученным нами результатам, концентрация конечных метаболитов NO в крови у женщин с бедным ответом была больше по сравнению с контрольной группой.
Известно двойственное влияние оксида азота на созревание ооцитов. В экспериментальном исследовании Bu S. et al. (2003) показано, что обработка культивированных мышиных ооцитов, заключенных в кумулюсные клетки, низкими концентрациями донора NO нитропруссида натрия (10-7, 10-6, 10-5 M) приводила к стимуляции мейотического созревания ооцитов. Добавление же высоких концентраций нитропруссида натрия (0,1–4 мМ) способствовало дозозависимому уменьшению количества ооцитов на стадии образования первого полярного тельца PB1 и высокому проценту атипичных ооцитов [12]. Избыточная продукция NO приводит к образованию пероксинитрита и окислительному стрессу, который пагубно влияет на репродуктивные функции [13]. Показано, что высокие уровни активных форм кислорода в культуральной среде при проведении ЭКО/ИКСИ связаны с низкой скоростью развития бластоцист, оплодотворения, дробления и фрагментацией эмбриона [14]. Кроме того, избыточное количество NO в сыворотке крови было обнаружено среди небеременных пациенток с трубным или перитонеальным бесплодием, а высокий уровень NO в фолликулярной жидкости ассоциирован с неудачей имплантации и снижением частоты наступления беременности [15]. Оксид азота участвует в патогенезе СПКЯ, который является причиной бесплодия у женщин репродуктивного возраста [16].
В нашей работе также было показано, что количество iNOS в кумулюсных клетках у женщин с субоптимальным и бедным ответом было статистически значимо больше по сравнению с пациентками с высоким и нормальным ответом.
Важный регулятор сосудистого тонуса in vivo, NO, синтезируется тремя видами синтаз – нейрональной (nNOS), eNOS и iNOS. Следует отметить, что, как правило, iNOS не экспрессируется в физиологических условиях, а индукция синтеза этого фермента ассоциирована с воспалением и иммунным ответом. При этом количество NO, продуцируемое iNOS, значительно превышает образующееся при активации eNOS и nNOS, что способствует образованию пероксинитрита и последующему повреждению клеток [17].
Заключение
Таким образом, у женщин с бедным ответом наблюдается повышение уровня эндотелина-1 и NO, а также увеличение количества iNOS в кумулюсных клетках по сравнению с пациентками с высоким и нормальным ответом, что может служить причиной сниженного ответа на стимуляцию яичников гонадотропинами при лечении бесплодия методами ВРТ. Дальнейшее изучение механизмов, определяющих качество и количество получаемых ооцитов, позволит адаптировать подходы к лечению бесплодия с учетом индивидуальных потребностей и увеличить частоту наступления беременности.



