При нарушениях фертильности распространенность хронического эндометрита (ХЭ) регистрируется в диапазоне от 2,8 до 56% [1]. У пациенток с ХЭ, по сравнению с женщинами с его отсутствием, наблюдается более низкая частота наступления беременности (30,8% против 63,0%) и живорождений (7,7% против 51,9% соответственно) [2]. Снижение фертильности, обусловленное ХЭ, исследователи связывают с изменением рецептивности эндометрия (РЭ) и нарушением имплантации яйцеклетки [3].
В оценках эффективности терапии ХЭ с целью восстановления фертильности существуют противоречия; однако в метаанализе 12 исследований сделан вывод, что лечение при условии разрешения ХЭ, в отличие от персистирующего ХЭ, обеспечивает больше шансов для успешного наступления беременности и живорождения (OШ=6,82 и 9,75 соответственно, p<0,0001) [4]. С другой стороны, отсутствие разрешения ХЭ после лечения, вероятно, определяет необходимость повторных курсов и/или применения иных методов лечения для нормализации эндометрия и восстановления его рецептивности, поскольку даже вспомогательные репродуктивные технологии (ВРТ) в случае неподтвержденного излечения ХЭ не обеспечивают положительного результата.
Оценка перспектив лечения бесплодия, связанного с дефектом имплантации яйцеклетки, по конечным результатам (наступление спонтанной беременности, частота живорождения) в клинической практике является неопределенной; вопрос прогнозирования успеха или неудачи лечения остается открытым, а текущие руководства по ХЭ не дают никаких рекомендаций для пар, планирующих зачатие, в плане прогноза.
Интерес практикующих врачей к маркерам РЭ обусловлен тем, что они могут способствовать прогнозированию наступления беременности и позволяют осуществлять контроль эффективности терапии, направленной на улучшение рецептивных свойств эндометрия. По мнению Краснопольской К.В. (2016), для рутинного использования в этих целях, вероятно, пригодно лишь ультразвуковое исследование (УЗИ) с показателями толщины и макроструктуры эндометрия [5]. В настоящее время в качестве маркеров РЭ активно изучаются такие методы, как электронно-микроскопические, иммунологические, молекулярно-генетические и многие другие параметры; однако все они, скорее, дают представления о фундаментальных аспектах процесса имплантации, но не пригодны для рутинного использования в клинической практике [5]. Кроме того, предполагается, что в окне имплантации существуют различные уровни РЭ и разные сигнатуры могут отражать разные уровни восприимчивости эндометрия, что может быть связано с тем или иным исходом беременности. Крайние значения биомаркера (в отличие от средних значений) могут иметь значительные прогностические и диагностические различия, которые не отражены в средних значениях [6]. Очевидно, что трудоемкость выполнения, дополнительные материальные расходы и сомнительная диагностическая ценность всех этих методов ограничивают их клиническое использование.
В настоящее время разработаны несколько программ для определения предикторов зачатия, но исключительно для прогнозирования успешности экстракорпорального оплодотворения (ЭКО) [7–9]. Некоторые прогностические модели, описанные в литературе, основаны на современных алгоритмах, таких как алгоритмы ранжирования, байесовские сети и нейронные сети, которые начинают активно внедрять в медицинскую практику. Модели глубокого машинного обучения или нейронных сетей с многочисленными уровнями функций или переменных, которые предсказывают результаты, являются наиболее перспективными [10]. Однако научный и практический интерес относительно оценки вероятности наступления спонтанной беременности у пациенток с ХЭ остается неудовлетворенным.
Таким образом, необходимость поиска моделей прогноза успешности лечения ХЭ для пациенток с нарушением репродуктивной функции является актуальным вопросом современной медицины.
Цель исследования: разработать прогностическую модель вероятности спонтанного наступления беременности у пациенток с ХЭ и нарушением репродуктивной функции с помощью нейросетевой технологии и оценить ее эффективность.
Материалы и методы
Дизайн. Настоящая работа представляет собой вторичный анализ результатов исследования «Течение и исходы беременности у пациенток с ХЭ и нарушением репродуктивной функции, получавших комплексное лечение с использованием препарата «Суперлимф» (рандомизированное контролируемое испытание в параллельных группах «ТЮЛЬПАН»)» [11].
Материал представлен электронной базой данных, куда были включены сведения о пациентках (n=2252), обратившихся с сентября 2019 г. по февраль 2023 г. в женскую консультацию ГБУЗ ТО «Перинатальный центр» (Тюмень, Россия) с жалобами на отсутствие беременности в течение 1–10 лет, с установленным диагнозом: Маточная форма бесплодия (N97.2 Женское бесплодие маточного происхождения, дефект имплантации яйцеклетки) с гистологически и иммуногистохимически подтвержденным диагнозом ХЭ (N71.1 Хроническая воспалительная болезнь матки), отвечавшие критериям включения/исключения. Из базы данных были отобраны 875 пациенток, отвечавших целям настоящего исследования. Для анализа использовались результаты комплексного обследования пациенток – клинических, принятых в гинекологии, функциональных и лабораторных методов, таких как метод полимеразной цепной реакции в режиме реального времени для идентификации микроорганизмов, вирусов и исключения инфекций, передающихся половым путем; морфологическое исследование аспиратов эндометрия; иммуногистохимическое исследование для определения плазмоцитов (CD138+); иммуноферментное исследование с определением цитокинов в сыворотке крови; лазерное конверсионное тестирование (аппарат «Фотон-Био», Россия).
Пациентки получали лечение, включавшее антибактериальную терапию (АБ) в течение 10 дней (875 пациенток, 100%), комплекс экзогенных природных цитокинов и хемокинов (Суперлимф 25 ЕД 1 раз в день вагинально, 20 дней) (476/875, 54,4%), гестаген во вторую фазу цикла на протяжении 1–6 циклов (до наступления беременности) (428/875, 48,9%).
Распределение в группы сравнения. I группа (n=461, 52,7%) была сформирована из пациенток, у которых не наступила спонтанная беременность; II группа (n=414, 47,3%) – из пациенток, у которых после лечения беременность наступила спонтанно (наблюдение проводилась в течение 6 месяцев после полученного лечения).
Основные результаты. Прогностическая модель и предикторы наступления спонтанной клинической беременности (по данным УЗИ в сроке 7–8 недель) у женщин с нарушением репродуктивной функции, обусловленной ХЭ. Программа клинического прогнозирования (онлайн-калькулятор) для оценки индивидуальной вероятности наступления спонтанной беременности у пациенток с ХЭ.
Статистический анализ
Использовали пакет программ SPSS Statistics Version 25.0 (IBM, США; лицензия № Z125-3301-14). Критерий Колмогорова–Смирнова применяли для оценки распределения признаков. Количественные показатели представлялись в формате медианы (Ме) с межквартильным диапазоном (Q1; Q3), качественные признаки указывали в абсолютных числах (n) и относительных величинах (%). Анализ различий количественных показателей в независимых выборках проводили с помощью U-критерия Манна–Уитни, качественных – при помощи критерия χ2. Значимость динамических изменений количественных показателей оценивали с помощью критерия Уилкоксона. Различия считали значимыми при р<0,05 (ошибки первого и второго рода α=5% и β=20% соответственно).
Нейросетевой анализ проводили по 12 параметрам, выбранным на основании их важности, что было определено с помощью нейросетевого анализа данных; далее указанные параметры вносили в программу SPSS с входящим в его структуру модулем Neural Networks: получали оценку вероятности наступления спонтанной беременности.
Результаты
Общие сведения о пациентках. Возраст пациенток варьировал от 18 до 45 лет (36,0 (35,0; 36,0) года). Социальная и клиническая характеристики пациенток представлены в таблице 1, анализ которой показал отличие пациенток между группами I и II по уровню образования и частоте лапароскопических вмешательств на органах малого таза; по остальным параметрам статистически значимые различия отсутствовали.
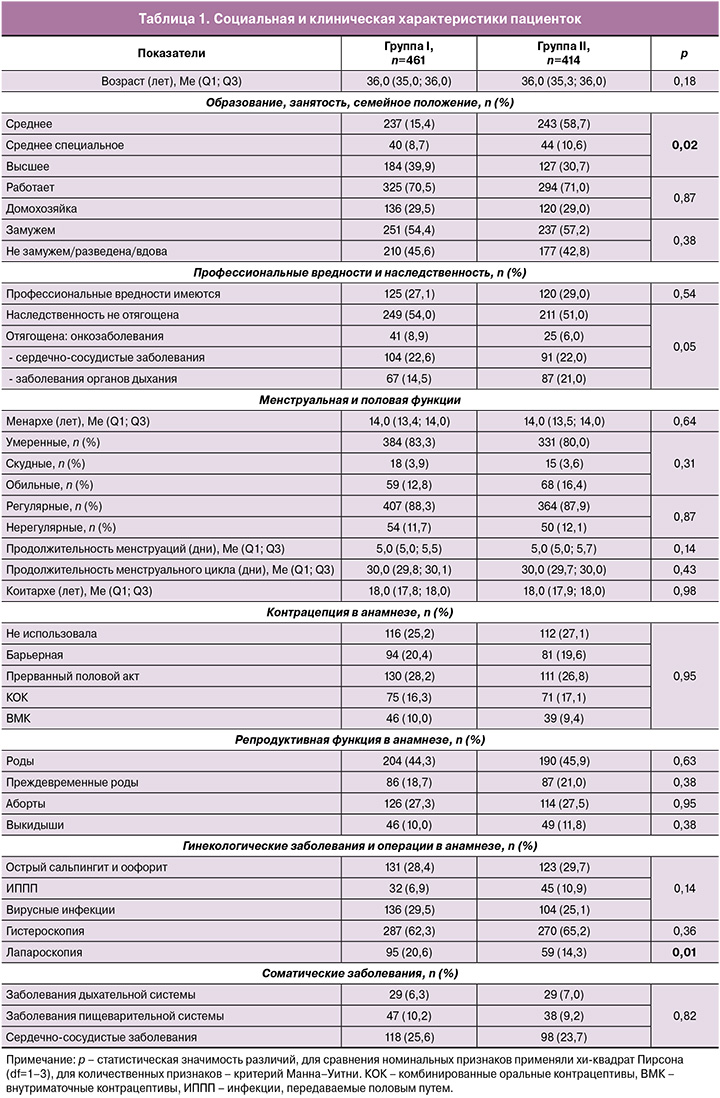
Средняя продолжительность бесплодия составила 2,0 (2,0; 2,8) и 1,0 (1,0; 2,5) года соответственно, р=0,06. Продолжительность бесплодия до 5 лет была у 79,0% (367/461) и 84,5% (350/414) пациенток, 5 лет и более – у 21,0% (97/461) и 15,5% (64/414) соответственно, р=0,03, т.е. во II группе пациенток с бесплодием 5 лет и более было статистически значимо меньше.
Лечение, выполненное в прегравидарном периоде, имело статистически значимые различия по составу, а именно: пациенток, получавших комплекс природных антимикробных пептидов и цитокинов (препарат «Суперлимф»), было больше во II группе (212/414, 62,6%), чем в I (217/461, 47,1%), р<0,001. По остальным видам лечения различий не было.
Результаты функциональных методов исследования и их динамика после лечения представлены в таблице 2.
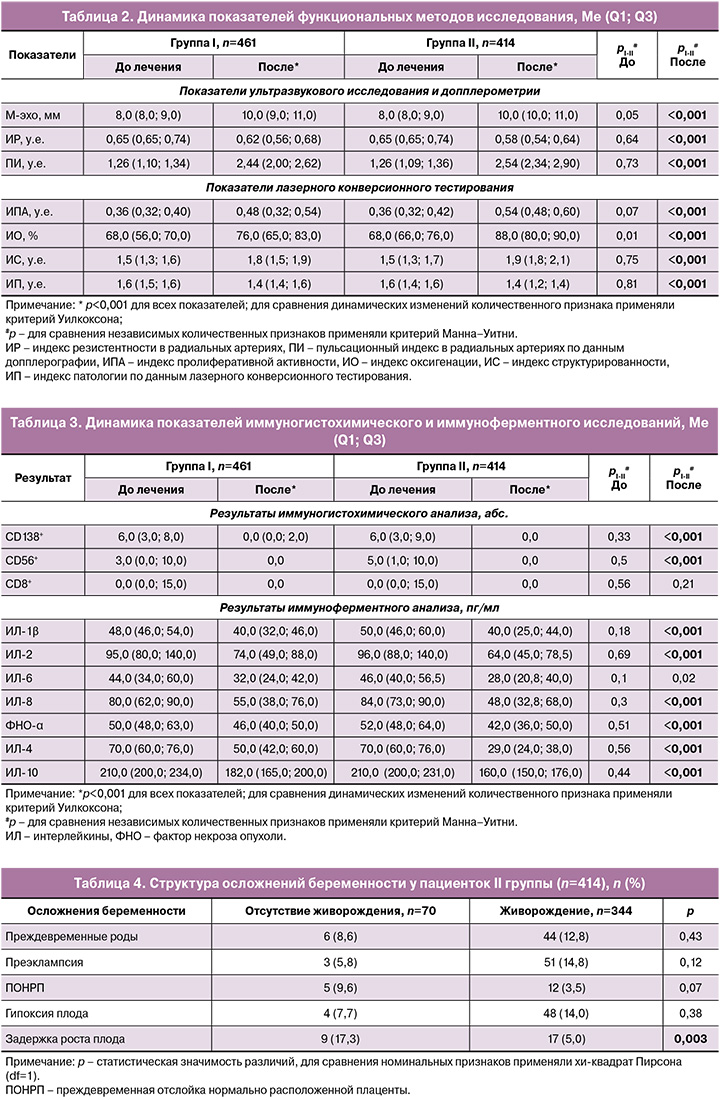
Показатели УЗИ и допплерометрии, равно как и лазерного конверсионного тестирования, после лечения значительно улучшились в обеих группах, но у пациенток II группы отличались статистически значимо в лучшую сторону по сравнению с I группой.
Аналогичное заключение можно сделать и в отношении результатов иммуногистохимического и иммуноферментного исследований (табл. 3).
Наступление спонтанной беременности у пациенток с благоприятным исходом произошло в среднем через 3,0 (3,0; 3,5) месяца, у пациенток с неблагоприятным исходом – через 2,0 (2,0; 2,5) месяца от момента завершения курса лечения (U=6868,0, p<0,001). Завершение беременности в среднем произошло через 39,0 (38,5; 39,0) и 14,0 (14,0; 19,6) недели гестации соответственно (U=509,5, p<0,001).
Из числа наступивших беременностей живорождением завершились 83,1% (344/414), или от общего количества пролеченных пациенток – 39,3% (344/875). Отсутствие живорождения было связано с самопроизвольным выкидышем до 12 недель в 67,1% (47/70) наблюдений, до 22 недель – в 14,3% (10/70), антенатальной гибелью плода – в 18,6% (13/70). Структура прочих осложнений беременности представлена в таблице 4, откуда видно, что только задержка роста плода явилась причиной его потери, статистически значимо отличавшейся от живорождения, – 17,3% против 5,0% (р=0,003).
Вес плодов у пациенток с живорождением составил 3500,0 (3288,3; 3508,9) г (U=378,5, p<0,001). Оценка состояния новорожденных по шкале Апгар в конце первой минуты составляла 8,0 (7,6; 8,0) балла, в конце пятой минуты – 8,0 (8,0; 8,1) балла.
Модель прогноза спонтанного наступления беременности. Учитывая необходимость исключения мультиколлинеарности между коррелирующими параметрами используемых методов исследования, было решено при создании модели прогноза спонтанного наступления беременности у пациенток с бесплодием после лечения ХЭ использовать только наиболее важные параметры. Для этой цели использовался нейросетевой анализ данных, и на основании его результатов для создания модели прогноза спонтанного наступления беременности была выбрана процедура многослойного персептрона. Число входных нейронов составило 12 единиц, в качестве которых выступали параметры исследования (бесплодие продолжительностью до 5 лет или 5 лет и более, уровень образования женщины, наличие или отсутствие в структуре лечения комплекса антимикробных пептидов и цитокинов, числовые значения пульсационного индекса в радиальных артериях по данным допплерографии, индекса оксигенации по данным лазерного конверсионного тестирования, CD138, интерлейкинов (ИЛ)-1β и ИЛ-4 после лечения), имеющие не только значимые различия при сравнении исследуемых групп, но и патогенетическое значение.
В архитектуру многослойного персептрона, учитывая число входных нейронов, включено 2 скрытых слоя. Выбор архитектуры выполнялся автоматически, что позволило вычислить оптимальное количество нейронов в указанных скрытых слоях, равное 8 и 6 соответственно, и максимально эффективно прогнозировать исход.
В обоих скрытых слоях и в выходном слое использовалась сигмоидная функция активации, что определяло взаимосвязь взвешенных сумм объектов с последующим слоем значений данных объектов. Сигмоидная функция в выходном слое переводила действительные переменные в диапазон (0; 1), что соответствует дизайну исследования. Сумма квадратов выступала в качестве функции ошибки. Выходной слой содержал 2 целевые (зависимые) переменные – наличие или отсутствие спонтанного наступления беременности. Архитектура разработанной нейронной сети представлена на рисунке 1.
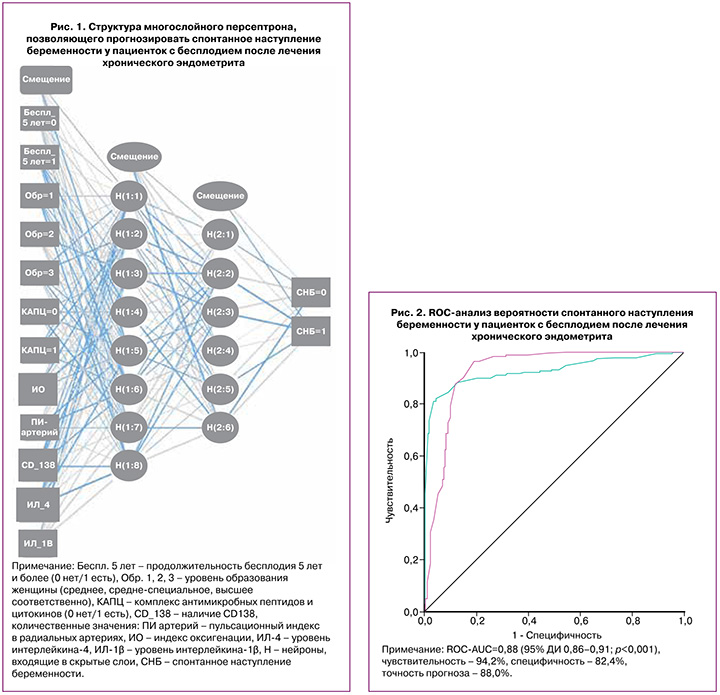
Результаты прогноза. Из 461 пациентки I группы прогноз оказался положительным у 81 (17,6%), отрицательным – у 380 (82,4%); из 414 пациенток II группы прогноз был положительным у 390 (94,2%), отрицательным – у 24 (5,8%). Точность прогноза разработанной модели составила 88,0% (чувствительность – 94,2%, специфичность – 82,4%). Информативность нейросетевого анализа данных в прогнозировании спонтанного наступления беременности у пациенток с бесплодием, обусловленным ХЭ, представлена ROC-анализом (рис. 2) – площадь под кривой (ROC-AUC) составила 0,88; p<0,001)
Оценка важности выбранных параметров в структуре разработанной нейронной сети, позволяющей прогнозировать вероятность спонтанного наступления беременности у пациенток с бесплодием и ХЭ, показала, что из лабораторных и функциональных показателей наибольший вес имеют ИЛ-4 по данным иммуногистохимического исследования (26%) и индекс оксигенации, полученный методом лазерного конверсионного тестирования (22%). Отметим, что важность параметров определяется не только их долей в структуре всех параметров, но и влиянием всей их совокупности друг на друга, что и учитывает нейронная сеть.
Таким образом, из числа пациенток с бесплодием, обусловленным ХЭ, вошедших в анализ, беременность наступила спонтанно в течение 6 месяцев после лечения у 47,3%, показатель живорождения составил 39,3%. Выделены 12 наиболее значимых параметров, которые были использованы для создания модели прогноза спонтанного наступления беременности на основе нейросетевой технологии. Разработанная модель является эффективной в плане прогноза наступления спонтанной беременности и характеризуется высокой точностью прогноза, равной 88,0%, с чувствительностью – 94,2%, специфичностью – 82,4%.
Для целей практического применения модели прогноза спонтанного наступления беременности у пациенток с ХЭ разработан онлайн-калькулятор, который содержит все показатели, вошедшие в модель прогноза, рассчитанную с помощью нейросетевой технологии, для точного его определения и решения вопроса о проведении лечения, необходимости повторных курсов, планирования спонтанной беременности или использования ВРТ.
Интерфейс калькулятора представлен на рисунке 3.

Врач акушер-гинеколог вводит параметры исследования (которые входят в исходную нейросеть и представлены выше), нажимает кнопку «Оценить»; калькулятор рассчитывает вероятность наступления спонтанной беременности и выдает результат (вероятность наступления спонтанной беременности высокая или низкая).
Прогноз позволяет принять решение о планировании спонтанной беременности (при положительном прогнозе) либо определить необходимость проведения повторного/-ых курсов лечения ХЭ (при отрицательном).
Обсуждение
Некоторые предыдущие исследования оценивали индивидуальную или комбинированную прогностическую ценность ряда переменных в программах ВРТ [12–14]. Переменные включали антимюллеров гормон, фолликулостимулирующий гормон, тесты овариального резерва, количество антральных фолликулов, возраст, ингибин В, количество извлеченных ооцитов и концентрации лютеинизирующего гормона в сыворотке в первый день стимуляции, однако давали ограниченную точность прогноза – менее 60% [13, 14]. Xu T. et al. (2022) представили предикторы наступления беременности после первого цикла ЭКО и переноса свежего эмбриона с использованием электронной медицинской карты eIVF [9]. Hansen K.R. et al. (2016) определили исходные характеристики у пар с необъяснимым бесплодием, прошедших лечение методом внутриматочной инсеминации после четырех циклов стимуляции яичников, которые могут предсказать такие исходы, как зачатие, клиническую беременность и живорождение. Они определили, что возраст, окружность талии, уровень дохода, продолжительность бесплодия и потеря беременности в анамнезе были значительно связаны по крайней мере с одним из указанных исходов беременности [15]. Вместе с тем исследования по поиску предикторов спонтанного наступления беременности после лечения ХЭ не проводились.
В отличие от исследования Hansen K.R. et al. и многих других, в которых указывается возраст как важный фактор, определяющий зачатие как в естественных, так и в циклах ВРТ, в настоящем исследовании мы не смогли его выделить в качестве прогностического параметра, поскольку возрастной диапазон пациенток, вошедших в анализ, был очень узок (35,0; 36,0 года).
Напротив, параметр «продолжительность бесплодия» оказался весьма значимым, что совпадает с мнением других авторов [16–18]. Так, выявлена нелинейная зависимость между продолжительностью бесплодия и частотой оплодотворения в программах ЭКО, которая уменьшалась с годами бесплодия вплоть до «переломного» момента, равного 4,8 года [17]. Abdelazim I. et al. (2018) считают, что по прошествии 2 лет, если беременность не наступила, то каждый дополнительный год бесплодия снижает вероятность беременности на 25% ежегодно [18]. В нашем исследовании этот факт подтвердился: показатель наступления беременности был ожидаемо и значимо выше при продолжительности бесплодия менее 5 лет и зависел от проведенного лечения, составив 51,0% против 19,2% (р<0,001). У пациенток с продолжительностью бесплодия 5 лет и более выявлена значимая связь между приемом комплекса природных антимикробных пептидов и цитокинов (Суперлимф) в составе комплексного лечения с увеличением шансов наступления беременности почти в 3 раза, по сравнению с теми, кто получал только гестаген/АБ (ОР=2,91; 95% ДИ 1,55–5,47) [11].
Разрешение ХЭ с отсутствием плазматических клеток в микропрепарате эндометрия наблюдалось нами (исследование «ТЮЛЬПАН») в группе с применением комплекса «Суперлимф», гестагена и АБ в 86,0% против 58,0% у пациенток, лечившихся гестагеном/АБ (р<0,001; ОР=1,61; 95% ДИ 1,52–1,71) с одновременным снижением выраженности фиброза по данным гистологического исследования аспиратов эндометрия, что закономерно приводило к увеличению частоты спонтанной беременности и живорождения [11]. Изучение результатов в течение 12 месяцев после комплексного лечения с использованием Суперлимфа показало, что из 563 пациенток беременность наступила у 83,3% (472/563), из них спонтанно – у 78% (368/472), живорождением завершились 87,7% (323/368) случаев. Данное наблюдение совпадает с выводами других исследователей о том, что лечение при условии разрешения ХЭ обеспечивает больше шансов для успешного наступления беременности и живорождения в отличие от персистирующего ХЭ [4], причем применение Суперлимфа демонстрирует превосходящую эффективность по сравнению с другими видами лечения, применявшимися другими авторами.
Такие показатели, как использование комплекса природных пептидов и цитокинов, пульсационный индекс в радиальных артериях матки по данным допплерометрии, уровни ИЛ-4 и ИЛ-1β по данным иммуноферментного анализа сыворотки крови, индекс оксигенации по данным лазерного конверсионного тестирования, в качестве предикторов наступления беременности ранее не изучались. Их значимость для цели прогноза была определена с помощью нейросетевого анализа, и они выделены нами как важные с точки зрения патогенеза ХЭ.
В качестве важных параметров для прогноза спонтанной беременности были определены наличие или отсутствие в программе комплексного лечения ХЭ препарата «Суперлимф». Отметим, что использование Суперлимфа в лечении ХЭ является патогенетически обоснованным, поскольку в патогенезе данного заболевания ведущую роль в настоящее время отводят иммунологической реакции на инфекцию с избыточной локальной продукцией цитокинов и лейкоцитов, что было показано в систематическом обзоре 2020 г. [19] и отражено в отечественных исследованиях последних лет [20–22]. В этих работах показано положительное влияние комплекса на элиминацию возбудителей и разрешение ХЭ, экспрессию определенных генов, восстановление экспрессии факторов врожденного иммунитета, нормализацию баланса про- и противовоспалительных цитокинов, увеличение экспрессии рецепторов к прогестерону в эпителии и строме эндометрия в 3 и 2,7 раза соответственно, улучшение показателей ангиогенеза и васкуляризации ткани эндометрия. Суперлимф получают из мононуклеарных клеток периферической крови (МКПК) – лейкоцитов крови свиней. Ранее в сетевом метаанализе 16 рандомизированных клинических испытаний было показано, что внутриматочное введение аутологичных МКПК приводит к увеличению шансов на наступление беременности в программах ЭКО в 2,4 раза по сравнению с контролем (без введения МКПК) (ОШ=2,44; 95% ДИ 1,67–3,57) и в 2,9 раза – для живорождения (ОШ=2,86; 95% ДИ 1,64–5,00) [23]. Преимуществами Суперлимфа, в отличие от внутриматочного введения аутологичных МКПК, являются локальное действие и удобство применения пациентками самостоятельно в виде вагинальных или ректальных свечей, при большем увеличении шансов на наступление беременности после ЭКО – в 3 раза (ОШ=3,08, 95% ДИ 2,31–4,10) и живорождения – в 3,8 раза (ОР=3,75, 95% ДИ 2,86–4,92) по сравнению с контролем (лечение без Суперлимфа).
Пульсационный индекс по данным допплерографии отражает уменьшение резерва эндометриального кровотока, что также указывается среди причин нарушения репродуктивной функции при ХЭ [19].
Значение диагностики состояния эндометрия с помощью лазерного конверсионного тестирования с использованием спектрометра «Фотон-Био» в настоящее время активно изучается и дает обнадеживающие результаты [24–26]. Этот новый экспресс-метод диагностики, разработанный отечественными учеными, основан на частотном анализе отраженного от тканей эндометрия света (спектральный анализ), который позволяет оценивать состояние эндометрия и его готовность к имплантации яйцеклетки у пациенток с ХЭ с помощью четырех параметров – индексов оксигенации, пролиферативной активности, структурированности и патологии. Индекс оксигенации, как нами было выявлено, – значимый показатель, выступающий в качестве прогностического фактора, вес которого в структуре наиболее важных параметров, наряду с ИЛ-4, составляет более 20%. Индекс оксигенации демонстрирует насыщение эндометрия кислородом (выражается в процентах, норма – более 80%) и косвенно отражает степень васкуляризации эндометрия. Максимальный уровень падения содержания кислорода в тканях до 46–50% наблюдался у женщин с ХЭ и внутриматочными синехиями [24]. Ранее нами был разработан метод прогноза в циклах ЭКО у пациенток с бесплодием, обусловленным ХЭ, на основании двух показателей – индексов оксигенации и пролиферативной активности эндометрия с вероятностью положительного прогноза наступления беременности и живорождения 80% [26]. Обращает на себя внимание тот факт, что при исключении из структуры нейронной сети индекса оксигенации точность прогноза снижается до 83,2%, что определяет его значимую диагностическую роль.
С использованием Суперлимфа тесно связаны другие три показателя, выделенные нейросетевым анализом, как важные для целей прогноза – CD138, отсутствие которого свидетельствует о разрешении ХЭ, ИЛ-1β и ИЛ-4, значения которых свидетельствуют об активности воспалительного и противовоспалительного звеньев локального иммунитета соответственно. Ранее нами также было показано значение ИЛ-4 как предиктора рецидивов бактериального вагиноза у пациенток, инфицированных вирусами герпеса [27]. Высокие концентрации ИЛ-1β и ИЛ-4 после проведенного лечения свидетельствуют о незавершенности процесса элиминации возбудителей, что и создает предпосылки для персистенции ХЭ.
Таким образом, разработанная нами прогностическая модель спонтанного наступления беременности после лечения у пациенток с ХЭ и нарушением репродуктивной функции с помощью нейросетевой технологии является уникальным инструментом, позволяющим предсказать успешность лечения с положительным результатом и точностью прогноза 88%, что превышает все известные модели (разработанные для ВРТ).
Для целей практического применения модели прогноза наступления спонтанной беременности у пациенток с бесплодием, обусловленным ХЭ, разработан онлайн-калькулятор, который позволяет либо определить необходимость в проведении повторного/-ых курсов лечения ХЭ (при отрицательном прогнозе успешности спонтанного наступления беременности), либо принять решение о планировании беременности (при положительном).
Заключение
Модель прогноза наступления спонтанной беременности у пациенток с бесплодием, обусловленным ХЭ, с помощью нейросетевой технологии имеет точность прогноза 88% (чувствительность – 94,2%, специфичность – 82,4%) и позволяет либо принять решение о планировании спонтанной беременности, либо определить необходимость проведения повторного/-ых курсов лечения ХЭ.
Перспективы дальнейших исследований
Учитывая наш опыт создания модели прогноза наступления спонтанной беременности у пациенток с нарушением репродуктивной функции, обусловленной ХЭ, с помощью нейросетевой технологии, считаем перспективным диагностическим решением выявление прогностических биомаркеров успешности ЭКО до переноса эмбрионов для женщин с маточной формой бесплодия и проведение дальнейших исследований в этом направлении. Модель прогноза наступления беременности и живорождения в результате ЭКО с помощью нейросетевой технологии позволит улучшить возможности прогнозирования, по сравнению с уже существующими зарубежными моделями, а программа для онлайн-калькулятора успеха ЭКО, разработанная на ее основе, позволит широко использовать ее в рутинной клинической практике, что является предметом нашей дальнейшей работы.



