Сниженный овариальный резерв (СОР) является одной из наиболее распространенных и сложно преодолеваемых причин бесплодия, при которой наблюдается более низкая частота наступления беременности и живорождения в программах вспомогательных репродуктивных технологий (ВРТ) по сравнению с женщинами с нормальным овариальным резервом (НОР) [1]. Этиологических и патогенетических механизмов снижения овариального резерва множество, так как на любом из этапов фолликулогенеза участвуют гормоны, их гены и рецепторы, являющиеся белковыми молекулами, структурным элементом которых являются аминокислоты.
В фолликулярной жидкости, как микросреде для роста и развития фолликулов и ооцитов, происходит обмен веществами и энергией между ооцитами и внеклеточной средой, что, возможно, отражает уровень метаболизма и потенциал развития ооцитов [2]. Решающее значение для фолликуло- и оогенеза имеют метаболиты, содержащиеся в фолликулярной жидкости и предоставляющие важную информацию о росте и дифференцировке фолликула [3]. К ним относят гормоны, факторы роста, цитокины, белки, стероиды, аминокислоты и полисахариды [4]. Таким образом, изучение изменений метаболитов фолликулярной жидкости может выявить факторы, оказывающие влияние на развитие ооцитов, как возможные предикторы их компетентности в развитии и жизнеспособности эмбриона и исходе беременности у пациенток с СОР [5].
Технология, позволяющая качественно и количественно оценить содержание низкомолекулярных соединений в биологическом материале, определена как метаболомный анализ, при проведении которого с помощью жидкостной хроматографии с масс-спектрометрическим детектированием (ЖХ-МС) предоставляется возможность оценки клеточного метаболизма на молекулярном уровне [6, 7]. Разные стадии развития фолликула характеризуются различными метаболомными характеристиками, которые меняются в зависимости от возраста женщины [8]. В последние годы внимание исследователей привлечено к изучению аминокислотного состава фолликулярной жидкости как биомолекул, вовлеченных в патогенез заболеваний репродуктивной системы, в том числе при СОР, синдроме поликистозных яичников и эндометриозе [9, 10] для выявления потенциальных диагностических и прогностических биомаркеров, так как нарушение метаболизма аминокислот, возможно, приводит к изменению процессов фолликулогенеза и оогенеза [11, 12].
Аминокислоты являются органическими веществами, содержащими аминогруппу (-NH2) и кислотную группу (-COOH) (рис. 1). Из-за различий в их боковых цепях аминокислоты имеют совершенно разные биохимические свойства и функции [13].
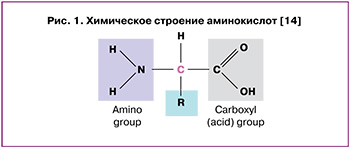
Из более чем 300 аминокислот, существующих в природе, только 20 служат строительными блоками белка; однако небелковые аминокислоты также играют важную роль в клеточном метаболизме. Интерес исследователей привлекает роль аминокислот в реализации репродуктивной функции на всех ее этапах. Результаты исследований демонстрируют, что как дефицит, так и избыток отдельных аминокислот могут подавлять или повышать экспрессию генов, тем самым обеспечивая регуляцию синтеза белка и многих гормонов на всех этапах обмена [15]. Например, тирозин и фенилаланин являются субстратами для синтеза адреналина, норадреналина, дофамина и гормонов щитовидной железы [16]. Высокие концентрации аминокислот, в том числе аргинина, глутамина и лейцина при внутривенном введении фармакологических доз, в 10–20 раз превышающих их алиментарные концентрации, стимулируют секрецию гормонов [17, 18].
У женщин с СОР в исследованиях аминокислотного профиля в фолликулярной жидкости выявлены значимые изменения, которые были ассоциированы с количеством ооцитов и качеством эмбрионов в программах ВРТ, что свидетельствует о существенной роли аминокислот. Метаболомный профиль может быть использован как для оценки овариального резерва, так и прогнозирования эмбрионального развития. По данным исследований, аминокислоты, в особенности лейцин, глутамин, аргинин и пролин, играют важную роль в эмбриогенезе, развитии плаценты и плода во время беременности [1, 19].
В связи с этим целью данного исследования явилась оценка аминокислотного профиля плазмы крови и фолликулярной жидкости у женщин с бесплодием и СОР по сравнению с женщинами с НОР.
Материалы и методы
Было проведено обсервационное одномоментное исследование по типу «случай-контроль» 115 женщин с бесплодием в программах ВРТ (экстракорпоральное оплодотворение (ЭКО)/интрацитоплазматическая инъекция сперматозоида (ИКСИ)). Пациентки были разделены на группы в зависимости от уровня овариального резерва: 1-я группа – 50 пациенток с СОР (антимюллеров гормон (АМГ) <1,2 нг/мл, количество антральных фолликулов (КАФ)<5), 2-я группа – 65 пациенток с НОР (АМГ≥1,2 нг/мл, КАФ≥5). Средний возраст женщин составил 37,2±5,3 года.
Всем пациенткам проведены обязательное обследование перед вступлением в программу ВРТ согласно клиническим рекомендациям «Женское бесплодие» (2021) [20] и специальные исследования, включающие оценку аминокислотного профиля и уровней стероидных гормонов методом высокоэффективной ЖХ-МС. Исследование было одобрено комиссией по этике биомедицинских исследований ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России.
Критерии включения: возраст 25–42 лет; отсутствие наступления беременности в течение 1 года и более регулярной половой жизни без контрацепции; подписанное информированное добровольное согласие на участие в исследовании. Критерии невключения: отказ от участия в исследовании; противопоказания к ВРТ; операции на яичниках в анамнезе; ВИЧ-инфекция и другие иммунодефицитные состояния; системные заболевания соединительной ткани; ревматические заболевания; онкологические заболевания любой этиологии; наличие хромосомных и генетических аномалий; программа донорских ооцитов или эмбрионов и программа суррогатного материнства.
Для мониторинга фолликулогенеза выполняли ультразвуковое исследование. Программу ЭКО проводили стандартно в протоколе с антагонистами гонадотропин-рилизинг-гормона; в качестве индукторов фолликулогенеза использовали мочевые и рекомбинантные гонадотропины. Ежедневную дозу гонадотропинов определяли индивидуально в зависимости от состояния овариального резерва, но не менее 225 МЕ/сут; в качестве триггера овуляции использовали хорионический гонадотропин. Во время трансвагинальной пункции яичников производили забор крови и фолликулярной жидкости из первого фолликула.
Анализ аминокислотного профиля проводили посредством ЖХ-МС на системе, состоящей из тройного квадрупольного масс-спектрометрического детектора Agilent 6460 (Agilent), оснащенного источником электрораспылительной ионизации и жидкостного хроматографа Agilent 1260 II (Agilent). Приготовление образцов осуществлялось согласно следующей процедуре: к 100 мкл образца добавляли 480 мкл хлороформ-метанольной смеси (2:1, об./об.) при 4°C; образец подвергали ультразвуковому воздействию в течение 10 минут; добавляли 150 мкл воды; перемешивали в течение 5 минут; получившийся раствор центрифугировали при 13 000 g в течение 5 минут при комнатной температуре; отбирали 200 мкл верхнего водно-метанольного слоя; сушили в токе азота 30 минут при 60°C; добавляли 200 мкл 3N соляной кислоты в бутаноле; перемешивали в течение 3 минут; центрифугировали при 13 000 g в течение 15 с при комнатной температуре; выдерживали при 60°C в течение 15 минут для проведения реакции дериватизации; центрифугировали при 13000 g в течение 15 с при комнатной температуре; сушили в токе азота 30 минут при 60°C; перерастворяли в 200 мкл раствора ацетонитрил/вода (1/1 об./об.); перемешивали в течение 5 минут; центрифугировали при 13 000 g в течение 15 с при комнатной температуре в течение 10 минут; переносили 120 мкл полученного образца в виалу со вставкой для дальнейшего анализа.
Статистический анализ
Статистическую обработку экспериментальных данных проводили с помощью скриптов, написанных на языке R [R Core Team (2018). R: A language and environment for statistical computing. R Foundation for Statistical Computing, Vienna, Austria. URL https://www.R-project.org/] в RStudio [RStudio Team (2016). RStudio: Integrated Development for R. RStudio, Inc., Boston, MA URL http://www.rstudio.com/].
Перед проведением сравнительного анализа количественных данных в исследуемых группах определяли вид распределения данных (тест Колмогорова–Смирнова, графический анализ данных).
Содержание аминокислот в образце оценивали полуколичественно по относительному уровню аналита, который рассчитывали делением площади хроматографического пика соответствующего аналита на суммарную площадь пиков аналитов в данном образце.
Перед статистической обработкой уровни аминокислот подверглись преобразованию так, чтобы среднее значение было равным 0, стандартное отклонение было равным 1 для лучшего графического представления анализируемых данных, поскольку уровни аминокислот распределены в широком диапазоне [21]. Формула преобразования:
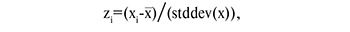
где zi – стандартизованное значение параметра; xi – исходное значение параметра; х‒ – среднее значение параметра; stddev(x) – стандартное отклонение совокупности.
При нормальном виде распределения данных определяли среднее значение со стандартным отклонением M (SD), для оценки различий в группах применяли t-тест. При распределении, отличном от нормального, данные представлены в формате медианы с межквартильным интервалом Ме (Q1; Q3), сравнение уровней аминокислот проводилось с помощью непараметрического критерия Уилкоксона–Манна–Уитни. Для оценки корреляционной зависимости применяли непараметрический корреляционный анализ Спирмена. Величину порогового уровня значимости p принимали равной 0,05.
Результаты
В исследование были включены женщины репродуктивного возраста с бесплодием, обратившиеся для достижения беременности в программе ЭКО/ИКСИ в ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России. Средний возраст женщин – 37,2±5,3 года. У всех пациенток был регулярный менструальный цикл. Средний показатель индекса массы тела составил 23,9±4,8 кг/м2. У пациенток с СОР отмечались статистически значимо более короткий менструальный цикл и более ранний возраст наступления менопаузы у матери (табл. 1).
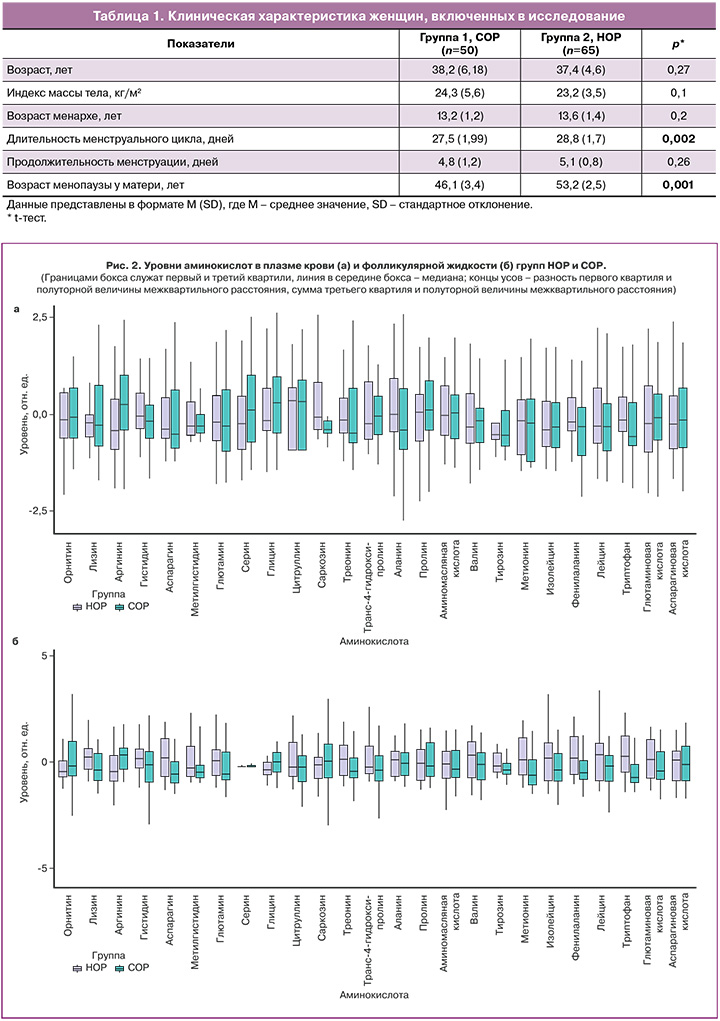
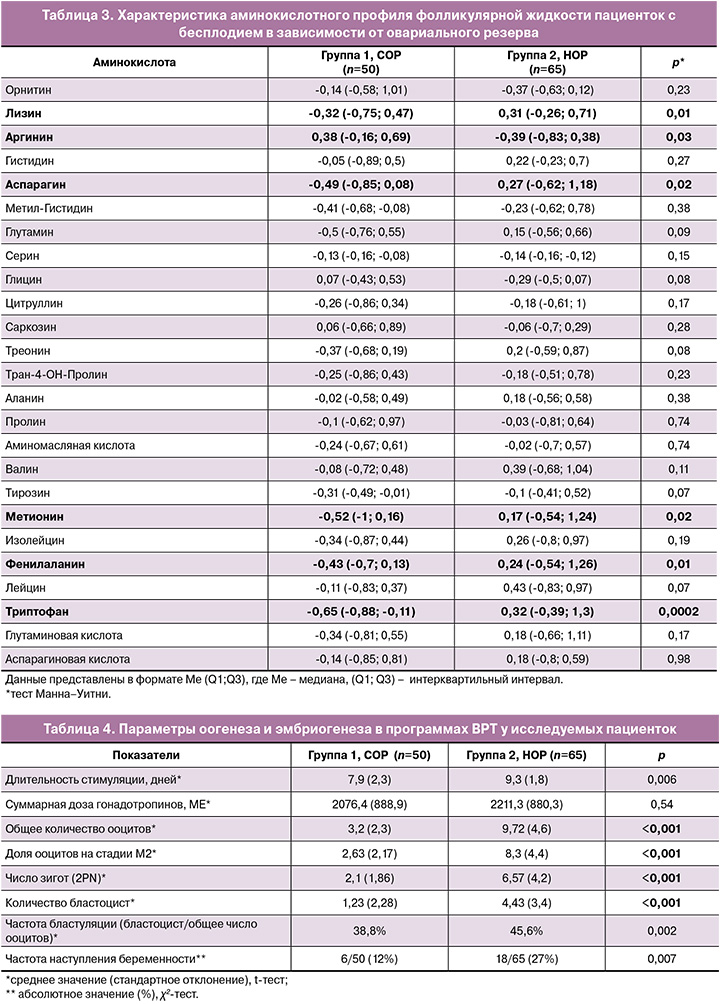
Был проведен сравнительный анализ данных о концентрациях аминокислот, полученных методом ЖХ-МС, в плазме крови и фолликулярной жидкости в день аспирации ооцитов. В плазме крови женщин с СОР обнаружено статистически значимое понижение показателей саркозина – -0,41 (-0,51; -0,22) и триптофана – -0,59 (-0,82; 0,3) по сравнению с женщинами с НОР (саркозин – -0,1 (-0,41; 0,7), триптофан – -0,19 (-0,48; 0,42)) (p<0,05) (табл. 2).
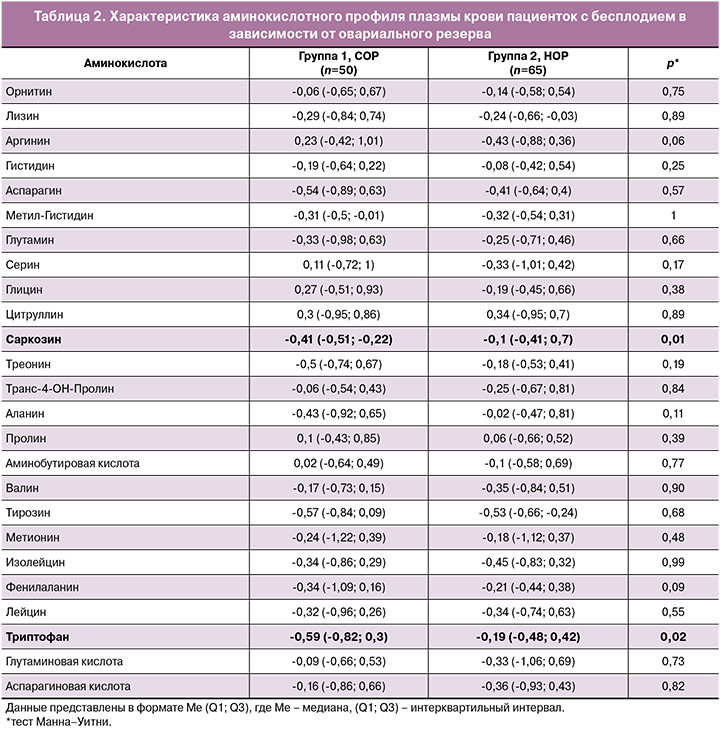
В фолликулярной жидкости женщин с СОР выявлено статистически значимое снижение концентрации лизина (НОР – 0,31 (-0,26; 0,71), СОР – -0,32 (-0,75; 0,47), p=0,01), аспарагина (НОР – 0,27 (-0,62; 1,18), СОР – -0,49 (-0,85; 0,08), p=0,02), метионина (НОР – 0,17 (-0,54; 1,24), СОР – -0,52 (-1; 0,16) p=0,02), фенилаланина (НОР – 0,24 (-0,54; 1,26), СОР – -0,43 (-0,7; 0,13), p=0,01) и триптофана (НОР – 0,32 (-0,39; 1,3), СОР – -0,43 (-0,7; 0,13), p=0,0002) (табл. 3) и повышенные уровни аргинина (НОР – -0,39 (-0,83; 0,38), СОР – 0,38 (-0,16; 0,69), p=0,03).
На рисунке 2 представлено графическое изображение изменений аминокислотного профиля в плазме крови и фолликулярной жидкости.
При сравнительном анализе параметров оо- и эмбриогенеза было выявлено статистически значимое снижение количества ооцитов, в том числе зрелых, показателей раннего эмбриогенеза и бластуляции и частоты наступления беременности в группе пациенток с СОР (табл. 4).
Также проведен корреляционный анализ уровней аминокислот в плазме крови и фолликулярной жидкости в день аспирации ооцитов и параметров оогенеза и раннего эмбриогенеза в каждой из групп (рис. 2, 3).
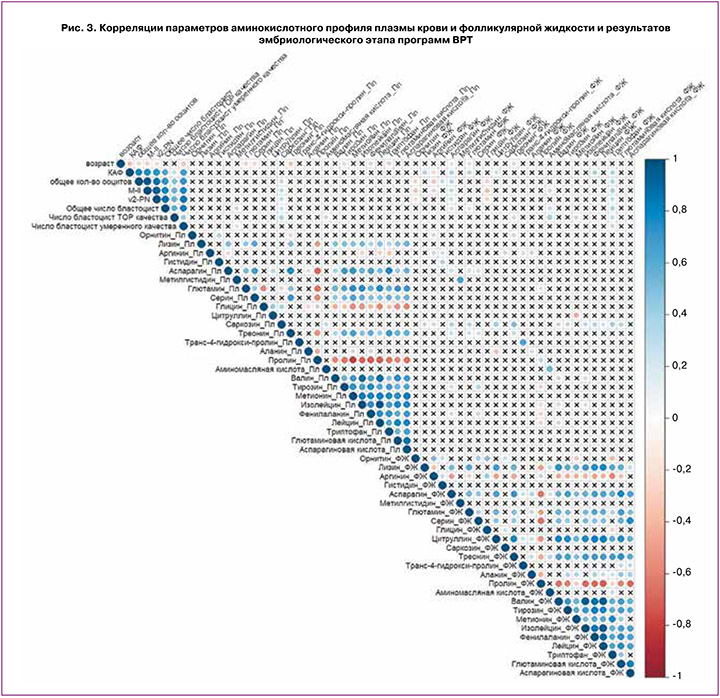
Как в группе СОР, так и НОР наблюдались сильные корреляционные взаимосвязи между уровнями аминокислот в плазме крови и фолликулярной жидкости (рис. 3). Наблюдается умеренная положительная корреляционная связь между КАФ и показателями оогенеза и раннего эмбриогенеза и уровнем аминокислот лизина и саркозина в плазме крови; аспарагина, триптофана и аминомасляной кислоты – в фолликулярной жидкости.
Обсуждение
В данной работе с помощью ЖХ-МС был проанализирован аминокислотный состав плазмы крови и фолликулярной жидкости и выполнено его сравнение между пациентками с бесплодием с СОР и пациентками с бесплодием с НОР.
В исследовании Li J. et al. при исследовании метаболомного профиля фолликулярной жидкости женщин с СОР было выявлено снижение уровня триптофана и продуктов его распада (5-гидрокси-L-триптофана, 5-гидроксииндолуксусной кислоты (конечный продукт метаболизма серотонина), индола, индолуксусного альдегида и индолуксусной кислоты), а также отмечены положительные корреляции их уровней с количеством ооцитов, эмбрионов и их качеством [22], что также выявлено в данной работе. Снижение содержания триптофана и продуктов его распада, особенно в ткани яичника, может влиять на количество и качество ооцитов и эмбрионов. Незаменимая аминокислота триптофан участвует в различных метаболических путях, задействованных в синтезе белков, серотонина (5-НТ) и кинуренинов. Триптофан и его метаболиты вовлечены во многие физиологические процессы, такие как поддержание роста клеток и регуляция иммунной функции. Одним из основных метаболитов триптофана является серотонин, который играет важную роль, в том числе, в регуляции функции плаценты и развитии плода [23]. Серотонин может влиять на развитие ооцитов, регулируя секрецию прогестерона гранулезными клетками. В экспериментальном исследовании Dube F. et al. показано, что снижение уровня серотонина, являющегося основным источником мелатонина в крови, приводит к нарушению раннего эмбрионального развития [24].
В данном исследовании обнаружены более высокие концентрации лизина, аспарагина, фенилаланина и метионина в фолликулярной жидкости женщин с НОР.
Эти данные согласуются с результатами исследования Li J. et al. женщин с СОР, в котором обнаружены сниженные уровни глицина, фенилаланина и DL-2-аминооктановой кислоты и повышенные уровни аспарагиновой кислоты, пролина, L-глютамина и пироглутамата в фолликулярной жидкости. Эти изменения аминокислотного профиля фолликулярной жидкости пациенток с СОР коррелировали с изменениями оо- и эмбриогенеза, что свидетельствует о роли аминокислот в созревании ооцитов и раннем эмбриональном развитии за счет снижения окислительного стресса и усиления функции митохондрий [22].
В исследовании D’Aniello G. et al. обнаружено, что концентрации D-аспарагиновой кислоты в фолликулярной жидкости напрямую коррелируют с морфологией ооцитов, их созреванием, процентом зрелых ооцитов и скоростью оплодотворения [25].
Нами было показано, что снижение концентрации аминокислот сопряжено с СОР, что позволяет рассматривать их в качестве потенциального биохимического маркера уровня овариального резерва. Полученные результаты свидетельствуют о вовлеченности аминокислот в процессы фолликулогенеза и формирования овариального резерва.
Подавляющее большинство работ о вовлеченности аминокислот в процесс фолликулогенеза подтверждают их стимулирующую роль на этапах раннего роста фолликула, поддерживающую роль в динамике его развития и их участие в инициации развития фолликулов на поздней стадии. Эти находки обосновывают концепцию о роли аминокислот и их применении для улучшения исходов программ ВРТ у женщин с бесплодием и СОР.
Заключение
Полученные данные о значимом снижении уровней аминокислот плазмы крови и фолликулярной жидкости у женщин с бесплодием и СОР и их взаимосвязь с параметрами оо- и эмбриогенеза позволяют предположить возможность определения аминокислотного профиля в качестве маркера для оценки овариального резерва и потенциала развития ооцитов и эмбрионов в программах ВРТ.



