Согласно стандартам проведения фетальной эхокардиографии от 2020 г. Американского института ультразвука в медицине [1], брадикардия плода определяется как устойчивая частота сердечных сокращений (ЧСС) плода ниже 110 уд/мин в течение как минимум 10-минутного периода.
При этом кратковременные и клинически незначимые эпизоды замедления ЧСС плода менее 100 уд/мин, которые разрешаются в течение нескольких минут, часто наблюдаются в течение I и II триместров и считаются доброкачественными [2, 3].
Брадикардия плода во II и III триместрах часто случается при задержке роста плода, при маловодии и в процессе родов. Существуют ситуации, когда снижение ЧСС менее 110 уд/мин в течение нескольких минут может являться физиологическим явлением. Однако когда ЧСС снижается ниже 80 уд/мин в течение более 10 минут во время родов, риск неонатальной ацидемии увеличивается быстро и значительно; это характеризует дистресс-синдром плода и служит показанием для экстренного родоразрешения [4].
Постоянная ЧСС ниже третьего процентиля может быть маркером значительного нарушения проведения импульса по проводящей системе сердца плода [5].
По механизму формирования брадикардия может быть синусовой, низкопредсердной или узловой брадикардией, блокированной предсердной бигеминией или атриовентрикулярной (АВ) блокадой. Поскольку выслушиваемая ЧСС у плода при этих вариантах аритмий одинакова, для дифференциальной диагностики характера брадикардии требуется тщательная пошаговая эхографическая интерпретация работы сердца плода. Это включает в себя оценку частоты и регулярности сокращений предсердий и желудочков и соотношения AВ/ВA-интервалов [2, 6, 7].
Фетальная синусовая и нижнепредсердная брадикардия
Брадикардия плода, которая характеризуется сердечным ритмом, возникающим в синоатриальном (СА) узле, c ЧСС 100 уд/мин и менее, составляет примерно 5% всех аритмий плода [8] (рис. 1). При этом сокращения в предсердиях и желудочках происходят одинаково медленно с проведением 1:1. Характерной особенностью низкопредсердной брадикардии является укорочение AВ-интервала на фоне низкой ЧСС [9].

Преходящая синусовая брадикардия плода определяется как дисфункция синусового узла и характеризуется нарушением формирования сердечного импульса. Наиболее распространенные причины такого состояния: стимуляция блуждающего нерва (например, вызванная сдавливанием пуповины), гипотензия или судороги матери, лечение матери бета-блокаторами, седативными и другими лекарственными препаратами [10]. Синусовая брадикардия может развиваться на фоне гипоксии плода и являться показанием к досрочному родоразрешению с диагнозом «дистресс- синдром плода» [11].
Стойкая брадикардия плода встречается относительно редко. Основными механизмами формирования стойкой синусовой брадикардии могут быть врожденный изомеризм предсердий со смещением СА-узла или приобретенные повреждения СА-узла вследствие воспаления и фиброза у пациентов с вирусным миокардитом. Также синусовая брадикардия может развиться при дисфункции ионных каналов и при редких метаболических нарушениях [12]. При отсутствии явной причины синусовая брадикардия может быть расценена как идиопатическая [10].
Еще одной причиной синусовой брадикардии у плода может быть дисфункция СА-узла, вызванная повреждающим воздействием материнских антител классов SSA/Ro и/или SSB/La [13]. Ранняя диагностика стойкой синусовой брадикардии (манифестация в 19–22 недели) помогает направить диагностический поиск в сторону выявления материнских антител к Ro/SSA или анти-La/SSB и своевременно начать этиопатогенетическое лечение [14].
В целом ни синусовая, ни низкопредсердная брадикардия не требуют специального лечения и обычно не связаны с гемодинамическими нарушениями пре- и постнатально.
Учитывая разнополярность причин редкого ритма у плода, эхокардиография плода имеет колоссальное значение в определении типа сердечного ритма, вызвавшего внутриутробную брадикардию. Диагностика причины синусовой брадикардии лежит не только в основе последующей адекватной терапии, но и позволяет значимо снизить процент преждевременного родоразрешения в связи с предполагаемым дистрессом плода [7, 15].
Как критерий для дифференциальной диагностики синусовой брадикардии при дистрессе плода от других видов синусовых аритмий можно использовать нестрессовый тест: при устойчивой синусовой брадикардии его применение не изменит характер и ЧСС, а при брадикардии, не связанной с патологией проводящей системы сердца, может вызвать вариабельность сердечного ритма.
Врожденный синдром удлиненного интервала QT
Это наследственное заболевание сердца, которое характеризуется удлинением интервала QT и клинически проявляется злокачественными аритмиями, синкопальными эпизодами, желудочковой тахикардией типа пируэт и повышенным риском внезапной сердечной смерти. Распространенность заболевания составляет около 1 случая на 2500 живорождений [16].
Генетическая основа заболевания была определена в середине 90-х гг., что позволило достоверно установить наследственный характер заболевания. На сегодняшний день идентифицировано по меньшей мере 7 различных генов, мутации в которых ответственны за развитие типичных клинических проявлений заболевания [17].
С 1975 г. под объединяющим названием «синдром удлиненного интервала QT» (СУИQT) (LQTS) существуют два наследственных варианта: аутосомно-доминантный синдром Романо–Уорда [18] и аутосомно-рецессивный синдром Джервелла–Ланге–Нильсена, который связан с врожденной нейросенсорной глухонемотой [19].
Наиболее частым проявлением синдрома удлиненного интервала QT у плода является брадикардия плода; но этот синдром также может быть связан с перемежающейся или персистирующей желудочковой тахикардией типа пируэт или АВ-блокадой II степени [7].
Синусовая брадикардия является наиболее частым проявлением нарушения ритма при LQTS у плода, однако часто может оставаться нераспознанной [20]. На LQTS приходится 15–17% брадикардий плода с ЧСС <110 уд/мин при нормально сформированном сердце. Тахикардия типа пируэт и/или необъяснимая АВ-блокада второй степени являются сложными характерными ритмами LQTS плода, но о них сообщается только примерно в 25% случаев LQTS плода [16].
В части случаев нарушения ритма сердца плода при синдроме LQTS плода могут быть кратковременными и клинически незначимыми внутриутробно, в то время как в других случаях они могут быть продолжительными и приводить к тяжелой сердечной недостаточности, обуславливающей преждевременные роды или гибель плода [11, 21–23].
Постнатальный диагноз может быть поставлен путем верификации на ЭКГ удлиненного интервала QT, скорректированного по ЧСС. В то же время известно о вариантах СУИQT, имеющих скрытое течение, не имеющих характерных электрокардиографических признаков. Генетическое тестирование подтверждает диагноз у 70–80% больных [24].
Диагностика LQTS у плода затруднена прежде всего ввиду отсутствия возможности регистрации ЭКГ плода [24, 25]. ЧCC плода ниже третьего процентиля для гестационного возраста характерна для LQTS, но чувствительность данного показателя низкая, ≈50% [5]. При этом часто легкая синусовая брадикардия (100–115 уд/мин) у плодов с LQTS не оценивается врачами как «не норма» [20].
Согласно результатам исследований Clur S.B. et al. (2018), у плодов с синдромом LQTS время изоволюметрического расслабления левого желудочка (L-IVRT) значительно длиннее, чем в контрольной группе плодов с нормальным ритмом сердца во всех сроках гестации, и достоверно ассоциируется с удлинением интервала QT на постнатальной ЭКГ (рис. 2, а и б). Авторы пришли к выводу, что наряду с обнаружением синусовой брадикардии плода удлиненный показатель изоволюметрического расслабления левого желудочка (L-IVRT) может улучшить пренатальное выявление СУИQT [26].
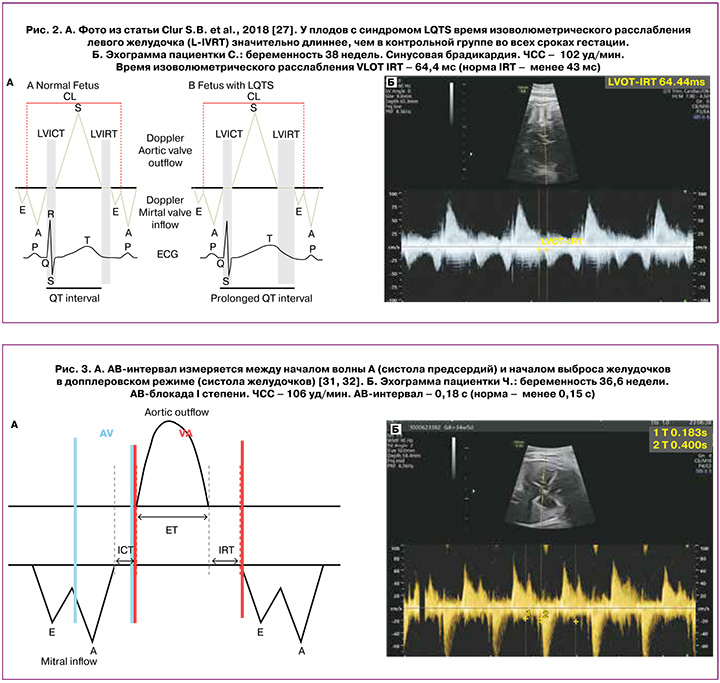
Важно помнить, что первичная профилактика злокачественных аритмий чрезвычайно эффективна при LQTS [27]. Кроме того, своевременное и адекватное внутриутробное лечение желудочковых тахикардий позволяет пролонгировать беременность и способствует разрешению водянки плода [22]. Своевременная дородовая диагностика СУИQT c признаками фетальной синусовой брадикардии снижает вероятность преждевременного родоразрешения в связи с дистресс-синдромом у плода [11]. Адекватная маршрутизация беременной с подозрением на наличие у плода синдрома LQTS предполагает родоразрешение в акушерском стационаре 3-го уровня с последующим оказанием помощи новорожденному [28–30].
Атриовентрикулярная блокада
АВ-блокадой обозначают замедление, частичное и полное прекращение проведения возбуждения от предсердий к желудочкам. Частота сокращений предсердий при этом остается нормальной, а желудочковая замедляется из-за АВ-диссоциации [7, 15]. АВ-блокада является наиболее распространенным типом брадикардии плода и встречается в 1 на 15000– 20000 живорождений [15]. Выделяют три степени АВ-блокады: I, II и III (полная) [8, 15, 31].
АВ-блокада I степени – это, по сути, не блокада, а задержка проведения возбуждения от предсердий к желудочкам, наблюдаемая как удлиненный интервал PR.
Интервал PR – это время между систолой предсердий и систолой желудочков; у плодов известен как интервал времени АВ-сокращения (АВ-интервал) (рис. 3а). АВ-интервал получают в рамках одного сердечного цикла путем одновременного совмещения курсора синхронизированного импульсно-волнового допплера с притоком и оттоком левого желудочка (выводным трактом левого желудочка и митральным клапаном). Временной допплеровский интервал измеряется между началом волны А (систола предсердий) и началом выброса желудочков в допплеровском режиме (систола желудочков) [32, 33]. Нормальные значения АВ-интервала у плода составляют 0,12±0,02 с. Верхним пределом AВ-интервала считают 0,14 с, и 0,15 с рассматривают как 99-й процентиль для нормального диапазона на поздних сроках беременности [5] (рис. 3б).
Во время ультразвуковых исследований и при проведении эхокардиографии плода обычно не проводится измерение AВ-интервала, поэтому АВ-блокада плода I степени редко диагностируется в общей популяции. В то же время при наличии у матерей предрасполагающих к формированию АВ-блокады сердца плода аутоиммунных заболеваний (системная красная волчанка, синдром Шегрена, недифференцированный аутоиммунный синдром) рекомендуется измерять AВ-интервал в период от 18 до 28 недель беременности для своевременного распознавания и, по возможности, устранения повреждения проводящей системы сердца плода [34].
АВ-блокадой II степени обозначают периодические прерывания проведения предсердных импульсов на желудочки. Различают два типа блокады II степени.
При I типе (Мобитц типа I) характерно постепенное замедление АВ-проводимости от цикла к циклу, которое заканчивается полным перерывом проводимости (выпадение желудочкового сокращения). Затем проводимость восстанавливается, и описанный комплекс повторяется снова. Такой периодический процесс называется периодикой Самойлова–Венкебаха (рис. 4, а и б).
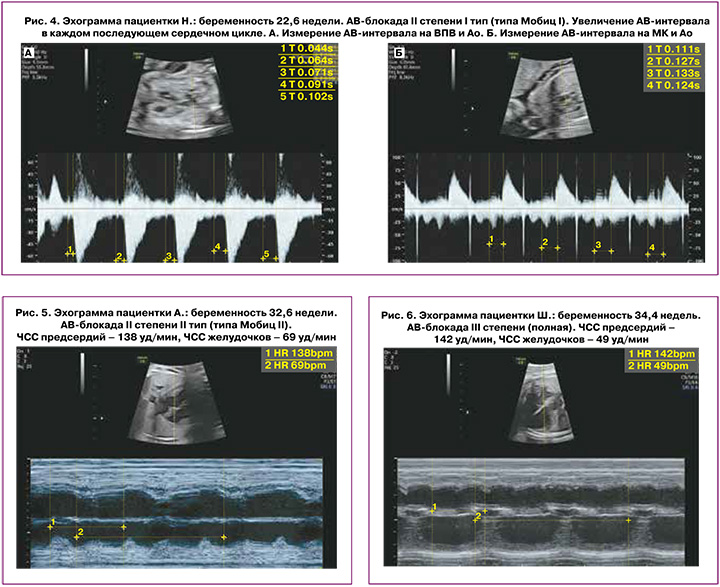
АВ-блокада II степени типа Мобитц II характеризуется внезапной (без предварительного удлинения времени проведения по АВ-узлу) блокадой изолированного импульса. Временной интервал между последовательными предсердными сокращениями при этом типе АВ-блокады одинаковый, но распространение электрического импульса к желудочкам прерывается, каждое второе (третье) сокращение предсердий не проводится на желудочки, частота сокращений желудочков в кратное число раз меньше, чем частота сокращений предсердий (например, 2:1, 3:1) [35] (рис. 5).
АВ-блокада плода II степени часто переходит в АВ-блокаду III степени. Прогрессирование до полной АВ-блокады может произойти быстро, в течение короткого периода времени, часто в течение нескольких дней [36, 37].
Полная АВ-блокада (III степени) возникает при полном прекращении передачи импульсов возбуждения из предсердий в желудочки сердца. Предсердия сокращаются в своем ритме под влиянием импульсов из синусового узла, желудочки сокращаются в более редком ритме под действием импульсов из автоматических центров второго или третьего порядка (АВ- диссоциация). При этом частота сокращений желудочков составляет 50–80 уд/мин, но может быть ниже (рис. 6). При такой частоте сокращений желудочков могут развиваться сердечная дисфункция и водянка плода. Полный АВ-блок встречается с частотой 1:15000–22000 новорожденных [35].
Различают наследственную, врожденную и приобретенную формы полной АВ-блокады. Они отличаются не только по генезу, но имеют различный характер течения и прогноз.
АВ-блокада может возникать при полностью структурно нормальном сердце или в сочетании с сопутствующим врожденным пороком сердца. Анатомические аномалии сердца встречаются в 14–42% случаев и включают дефекты АВ-перегородки, изомерию левого предсердия и аномалии магистральных артерий, которые нарушают электрофизиологическую непрерывность между предсердиями и желудочками [38].
Аутоиммунная врожденная АВ-блокада представляет собой пассивно приобретенное аутоиммунное поражение проводящей системы сердца, связанное с трансплацентарным переходом материнских аутоантител к развивающемуся плоду. У плодов аутоантитела прикрепляются к рибонуклеотидам, которые экспрессируются на кардиомиоцитах фетального миокарда. Антитела продуцируются против пептида SSB/La 48 кДа и двух пептидов SSA/Ro молекулярной массой 52 и 60 кДа и, по-видимому, являются наиболее разрушительными для проводящей системы плода и новорожденного [38, 39].
Поражение сердца плода, ассоциированное с аутоантителами, проявляется воспалением, фиброзом, кальцификацией, отложением иммунных комплексов на клетках AВ-узла, что приводит к блокировке проведения сигнала из предсердий в желудочки [40]. Это повреждение происходит после окончания эмбрионального периода формирования сердца плода, что подтверждается отсутствием структурных и анатомических аномалий в сердцах с аутоиммунной блокадой.
У серопозитивных женщин при наличии у них в крови аутоантител риск рождения ребенка с АВ-блокадой сердца составляет примерно 2% [34]. Риск повторного рождения ребенка с поражением проводящей системы в этой группе женщин составляет 12–25% и приближается к 50% в случае третьей беременности [41].
Примерно у трети детей с врожденной АВ-блокадой у матерей есть клинические проявления аутоиммунных заболеваний, но женщины не были обследованы и лечение во время беременности не получали. Однако в подавляющем большинстве случаев АВ-блокада возникает у плодов «здоровых» матерей, несущих молчащие анти-Ro/SSA-антитела. Таким образом, диагноз материнской серопозитивности обычно ставится только после обнаружения врожденной АВ-блокады у плода [41]. При этом 9% матерей могут быть даже серонегативными на момент диагностики заболевания у плода и только позже становятся серопозитивными [42].
Поражение сердца у плода может зависеть от уровня антител Ro и La в сыворотке беременной женщины. Уровни антител Ro и La в сыворотке крови были в 6 раз выше у матерей, дети которых имели поражение проводящей системы, в сравнении с женщинами, дети которых родились без патологии сердца. При этом при двойном положительном тесте, когда в сыворотке матери определяются одновременно положительные аутоантитела против Ro и La, формирование аутоиммунной блокады у этих плодов выше (3,92%), чем у детей матерей с положительным результатом теста на изолированные анти-Ro-антитела (2,25%) [40].
У женщин с системной красной волчанкой распространенность антител Ro оценивается в 40%, а у пациентов с синдромом Шегрена она составляет от 60 до 100%. Материнские аутоантитела обнаружены более чем у 95% плодов или новорожденных с АВ-блокадой [43].
Клинические признаки чаще всего развиваются в период с 18-й по 24-ю неделю беременности. Диагностика АВ-блокады у плода, связанной с аутоантителами, возможна первоначально на стадии I или II степени, но в большинстве случаев беременные с поражением проводящей системы сердца у плода выявляются при сформированной полной АВ-блокаде при регистрации фетальной брадикардии 50–70 уд/мин [44].
АВ-блокада I и II степени имеет короткие окна обратимости, и раннее выявление данного вида нарушения ритма важно для лечения, так как в этой стадии процесса остается возможность купирования патологических изменений в миокарде сердца плода. При этом АВ-блокада III степени считается необратимой [45]. Предполагается, что первоначально имеет место обратимое изменение кальциевых каналов L-типа с последующим апоптозом и гибелью клеток [46].
Вероятность летального исхода у новорожденных с полной АВ-блокадой составляет от 15 до 30%. Риск внутриутробной смерти составляет 6%, а общая 10-летняя выживаемость – 86%. В 5–30% случаев в неонатальном периоде развивается дилатационная кардиомиопатия, и большинству новорожденных требуется имплантация кардиостимулятора [47].
Прогностическими факторами высокой вероятности внутриутробной смерти являются водянка плода и более ранний срок беременности на момент манифестации фетальной брадикардии. В то же время риск неонатальной смерти ассоциируется с неиммунной водянкой и эндокардиальным фиброэластозом [48].
Врожденная АВ-блокада без положительных антител к SSA/Ro или SSB/La встречается редко, с зарегистрированной частотой 1 случай на 20 000 живорождений [49]. При этом такая АВ-блокада протекает доброкачественно и имеет лучший долгосрочный прогноз. Baruteau А.Е. et al. (2012) сообщили о 100% выживаемости у 120 детей с изолированной АВ-блокадой, из которых у 23 детей поражение сердца развилось внутриутробно или в первый месяц жизни [42].
На сегодняшний день достигнуты значительные успехи в понимании клинических, генетических и молекулярных характеристик в развитии идиопатической АВ-блокады. Опубликованные родословные показали аутосомно-доминантное наследование с неполной пенетрантностью и переменной экспрессивностью. Наследственная изолированная АВ-блокада в структурно нормальных сердцах представляет собой первичное нарушение проводимости импульса в сердце и связана с генетическими вариантами строения генов, ответственных за работу ионных каналов, – SCN5A, SCN1B, SCN10A, TRPM4 и KCNK17, а также с генами, кодирующими белки сердечного коннексина [42].
При врожденной неиммунной АВ-блокаде у детей следует анализировать семейный анамнез; он может предоставить веские аргументы в пользу наследственности даже у пациентов, у которых расстройство представляется спорадическим и идиопатическим.
Заключение
Необходимо подчеркнуть, что аритмии у плода могут быть диагностированы с высокой точностью и подлежат терапевтическому воздействию. Обследование всех плодов с нерегулярным ритмом или не соответствующей гестационному возрасту ЧСС является оправданным и позволяет выявить причину заболевания, влияет на тактику лечения и дальнейший прогноз. Как правило, чем более выражены нарушения сердечного ритма у плода и чем меньше гестационный срок, при котором развилась аритмия, тем тяжелее это заболевание будет переноситься плодом, тем выше вероятность развития неиммунной водянки и антенатальной гибели плода. Следовательно, максимально ранняя диагностика и правильная оценка гемодинамических последствий аритмии играют решающую роль в терапии и прогнозе заболевания у плода.



