Проблема выхаживания детей, родившихся в сроке сверхранних преждевременных родов, остается чрезвычайно актуальной. В крупных мировых перинатальных центрах с высоким уровнем оказания помощи около 80–85% детей с экстремально низкой массой тела (ЭНМТ) и очень низкой массой тела при рождении выживают и выписываются домой [1]. Однако в течение двух лет после выписки 2–5% из них умирают от осложнений, связанных с преждевременным рождением. О неудовлетворительных исходах для детей, родившихся в сроке беременности 22–25 недель, указывают и отечественные авторы [2]. Считается, что в этих сроках существует некий биологический «барьер», препятствующий выживанию этих детей [3]. Во многих современных работах уделяется большое внимание анализу состояния здоровья, показателей физического и нервно-психического развития детей, рожденных в сроках сверхранних родов, зависимости этих критериев от массы тела при рождении и факторов, приводящих к рождению в сроках гестации 22–28 недель [4–6]. Несомненно, щадящие режимы искусственной вентиляции легких с ранним переходом на неинвазивную вентиляцию со снижением параметров оксигенации, попытки раннего энтерального питания, сокращение длительного постнатального применения стероидов значительно улучшили прогноз качества жизни детей с ЭНМТ [7, 8].
Актуальность проблемы сохраняется не только в связи с переходом российского здравоохранения с 1 января 2012 года на рекомендуемую ВОЗ регистрацию детей с массой тела при рождении от 500 грамм и включением их в государственную статистику (Приказ МЗ РФ №1687н от 27 декабря 2011 г.) [9], но и Приказом Министерства здравоохранения РФ от 29 декабря 2012г. №1705н «О порядке организации медицинской реабилитации». Медицинская реабилитация детей, родившихся с ЭНМТ, осуществляется в плановой форме в рамках специализированной медицинской помощи. Для этого организуется пролонгированное катамнестическое наблюдение за развитием глубоко недоношенного ребенка [7–13]. Однако перинатальные центры, осуществляющие I и II этапы выхаживания недоношенных детей, в большинстве своем не имеют III этапа, осуществляющего помощь детям с ЭНМТ до 3 лет жизни в условиях дневного и круглосуточного стационара, где оценивается клиническое состояние ребенка, формируется программа реабилитации в ранний восстановительный период.
Цель исследования: изучить результаты лечения и выхаживания детей, родившихся с ЭНМТ в сроках гестации 22–28 недель в НИИ ОММ за период 2010–2013 гг.
Материал и методы исследования
В научном педиатрическом отделе был разработан регистр катамнеза детей с ЭНМТ при рождении. В данный регистр заносится вся информация об особенностях соматического и гинекологического анамнеза матери, течения данной беременности, наличие осложнений и особенностей родов. Следующим этапом описывается весь период пребывания ребенка в отделении реанимации и интенсивной терапии (ОРИТН): длительность и характер респираторной помощи, антропометрические показатели в постконцептуальном возрасте 38–40 недель гестации, начало и характер вскармливания, структура заболеваемости, количество плазмо- и гемотрансфузий, параметры функциональной диагностики. Подобные исследования проводятся и в декретированные сроки 3, 6, 9, 12 месяцев: антропометрические показатели, с определением соматотипа и гармоничности развития характер вскармливания, структура соматической и неврологической патологии, параметры функциональной диагностики, наличие прививок. В регистр также внесены данные об этих детях в возрасте 1,5–2 года и 3 лет. Данный регистр позволяет отслеживать судьбу ребенка с ЭНМТ от родового зала до 3-летнего возраста. Своевременное раннее выявление патологических симптомокомплексов позволяет эффективнее проводить реабилитационные мероприятия и соответственно приводит к снижению формирования инвалидизирующей патологии у данной категории детей.
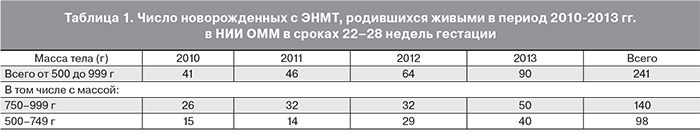
На первом этапе на основе электронной формализованной карты проведен анализ детей с ЭНМТ, родившихся живыми с 2010 по 2013 г. (n=241). Из них были сформированы две сравнительные группы по исходной массе тела при рождении: I группа – 500–749 г (n=98; 40,6%); II группа – 750–999 г (n=140; 58,09%). В табл. 1 представлены данные о динамике числа детей с ЭНМТ с 2010 по 2013 г., поступающих в отделение I этапа (ОРИТН) института. Как видно из табл. 1, за 4 года в 2 раза увеличилось число детей с массой тела 750–999 г и в 2,6 раза – детей с массой тела 500–749 г.
В методы исследования входили: анамнестический (сбор данных по обменной карте беременной – форма 113/у), аналитический (анализ истории развития и болезни новорожденного – форма 027/у, истории развития ребенка – форма 112/у).
В электронную формализованную карту были внесены данные об особенностях течения гестационного периода, интра-, неонатального периодов, постнеонатального развития, соматической заболеваемости. Физическое развитие детей в возрасте от 1 до 15 месяцев оценивалось по оценочным таблицам [14] и регрессионным шкалам физического развития, в которых предусмотрено выделение границ 3, 10, 25, 50, 75, 90, 97-го центилей распределения или 8 коридоров. Психомоторное развитие детей оценивалось по таблицам Лексиной и по скрининговой шкале КАТ/КЛАМС (CAT/CLAMS – the Clinical Adaptike Tect/ Clinical Linguistic and Auditory Milestone Scale), разработанной Американской академией педиатрии как унифицированное скрининговое тестирование для детей до 2 лет.
Результаты исследования и обсуждение
Проанализированы социальный статус, состояние здоровья, особенности акушерского анамнеза и течения гестационного периода у матерей наблюдаемых детей. В экстрагенитальной патологии матерей исследованных новорожденных доминировали болезни системы кровообращения в форме артериальной гипертензии II–III степени, вегетососудистой дистонии (53,9%), патологии эндокринной системы (гипотиреоз – 15,4%), инфекции мочеполовой системы (75,2%). Рождению детей в сверхранних сроках предшествовало осложненное течение настоящей беременности и родов: угроза прерывания беременности (59,6%), преэклампсия средней и тяжелой степени (46,2%), хроническая фетоплацентарная недостаточность субкомпенсированной формы (50,0%), декомпенсированной (19,2%), нарушение маточно-плацентарного кровотока II–III степени (53,9%). Наступление настоящей беременности у 18,5% матерей произошло в результате применения методов вспомогательных репродуктивных технологий, 35% детей были из многоплодной беременности. Роды у всех женщин наступили самопроизвольно. Оперативное родоразрешение осуществлено в 86,5% случаев.
Рождение ребенка с ЭНМТ является серьезным стрессовым фактором для семьи. В ФГБУ НИИ ОММ практически каждый случай родоразрешения пациенток в сроке сверхранних преждевременных родов обсуждается коллегиально. В состав консилиума помимо акушеров-гинекологов входит неонатолог-реаниматолог и перинатальный психолог. К чувству тревоги и страха за жизнь такого ребенка присоединяется недоверие к возможностям его выхаживания и дальнейшего благополучного развития. Одной из важных задач, стоящих перед врачами-перинатологами, является оказание помощи и поддержки матери в преодолении психологического барьера между ней и ее недоношенным ребенком. Необходимо научить мать воспринимать недоношенность ребенка как временное состояние, внушить ей оптимизм в отношении его последующего полноценного роста и развития [15].
В институте разработана программа психологической адаптации семьи к прогнозу рождения экстремально-недоношенного новорожденного, включающая в себя как пренатальный, так и постнатальный этапы. При этом на пренатальном этапе работа ведется строго индивидуально, поскольку уровень тревожности у беременных на этом этапе чрезвычайно высок, а на постнатальном этапе возможны как индивидуальные, так и групповые занятия для родителей экстремально недоношенных новорожденных. Основная цель таких занятий – адаптация семьи к прогнозу, позитивный настрой на выхаживание новорожденного, на грудное вскармливание, на совместное пребывание на втором и третьем этапах выхаживания. При анализе предварительных результатов применения этой программы установлено, что у матерей экстремально-недоношенных новорожденных уровень ситуационной тревожности на пренатальном этапе в 100% случаев высокий: по шкале Ханина–Спилбергера в среднем составляет 64,4±1,4 балла. После проведения этапной психологической адаптации к 30-м суткам послеродового периода уровень ситуационной тревожности снижается на 30 % и составляет в среднем 46,1±0,8 балла (p<0,001). На этом этапе у 50% женщин уровень ситуационной тревожности соответствует умеренному, что является нормой. Это свидетельствует об адаптации семьи, приобретению навыков ухода за ребенком и способствует сохранению грудного вскармливания.
Уровень личностной тревожности, как более глубинной психологической характеристики, практически не меняется – 42,1±1,6 балла на дородовом этапе и 44,2±1,9 на 30-е сутки после родоразрешения (p>0,05).
В структуре заболеваемости детей в неонатальный период преобладала сочетанная патология: респираторный дистресс-синдром (РДС) различной степени тяжести отмечен практически у каждого ребенка, что потребовало проведения традиционной пациент-триггерной искусственной вентиляции легких (ИВЛ) с контролем дыхательного объема у 59,6% детей. Фактически 50% детей нуждались в респираторной поддержке с помощью моно- или биназального СРАР до или после проведения ИВЛ; только на респираторной поддержке СРАР оказались 13,5% детей.
Как показало наше исследование, в структуре заболеваемости новорожденных с ЭНМТ на первое-второе места традиционно выходит РДС, асфиксия и гипоксия, на третье место – инфекционная патология. В структуре инфекционной патологии основную долю занимает внутриутробная генерализованная инфекция (ранний сепсис). Тяжелые формы внутрижелудочкового кровоизлияния (ВЖК) занимают четвертое место, частота ВЖК III степени среди выживших пациентов с ЭНМТ составляла 10,2%. У этих детей в последующем развилась постгеморрагическая гидроцефалия, потребовавшая хирургической коррекции. Частота ВЖК III степени на фоне генерализованных инфекций среди умерших составила в среднем 45,7%.
Структура летальности новорожденных с ЭНМТ зависела от гестационного возраста и массы тела при рождении (табл. 2): в группе 500–749 г она была в 3 раза выше, чем в группе 750–999 г.
В структуре всех «потерь» за 2013 г. 71,8% в отделении реанимации НИИ ОММ составили младенцы с ЭНМТ.
Таким образом, за 4 года из числа 241 родившихся с ЭНМТ умерли 57 детей, 184 ребенка прошли лечение в отделении патологии (II этап) и реабилитации (III этап).
В течение 2–3 месяцев жизни сохранялась высокая частота неврологической патологии: у 40,6% детей исходом церебральной ишемии явился перивентрикулярный глиоз и формирование лейкомаляционных псевдокист.
К 38–40 неделям постконцептуального возраста у всех детей, родившихся с ЭНМТ, отмечался синдром двигательных нарушений и синдром вегето-висцеральных дисфункций; гидроцефалия – у 21,2%; 56,1% детей формировали бронхо-легочную дисплазию, 24,8% – в тяжелой форме. Группа риска по ретинопатии составила 76,6%.
На III этапе выхаживания в стационарных условиях прошли обследование и лечение 198 детей (175 детей, родившихся в НИИ ОММ, 23 – из других перинатальных центров), которые были разделены на 4 возрастные группы:
- I – в возрасте 5–6 месяцев жизни – n=51; 25,7%;
- II – в возрасте 7–9 месяцев жизни – n=44; 22,2%;
- III – в возрасте 10–15 месяцев жизни – n=62; 31,3%;
- IV – старше 15 месяцев жизни – n=41; 20,7%.
В перечисленных группах дети были разделены на весовые подгруппы, как и в периоде новорожденности (500–749 г; 750–999 г).
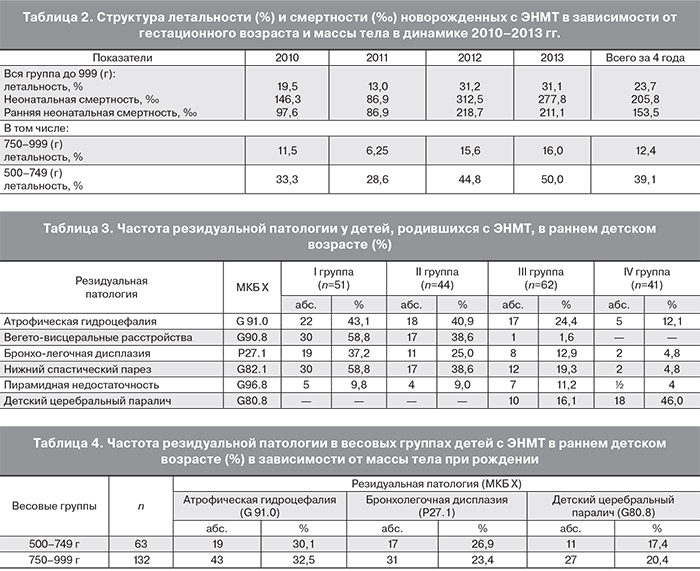
Резидуальная патология, которая формировалась в раннем детском возрасте, доминировала в центральной нервной системе и легких (табл. 3).
Атрофическая гидроцефалия формируется у детей с ЭНМТ вследствие перенесенных субэпендимально-интравентрикулярных кровоизлияний с формированием внутричерепных гипертензий (гидроцефалии). У детей массой тела при рождении 500–749 г эта патология отмечена у каждого третьего ребенка. Однако с такой же частотой эта патология выявлена у детей массой тела при рождении 750–999 г.
Таким образом, выживаемость детей весовой категории 750–999 г выше, но отягощенность резидуальной патологией такая же, как и у детей весовой категории 500–749 г (табл. 4).
Сопутствующие этой основной патологии другие заболевания диагностированы в небольшом проценте случаев. Так, ретинопатия III степени отмечена в 10 случаях (5% обследованных); нейросенсорная тугоухость – у 12 детей (6%). В первом полугодии жизни у 27 детей с ЭНМТ (13,6%) выявлена персистенция цитомегаловирусной инфекции, во втором полугодии – только у 18 детей (9%).
Одной из составляющих программы ведения и реабилитации детей с ЭНМТ на первом году жизни является оценка их физического развития. Исследования последних лет показывают важность этих показателей как при рождении, являясь исходным уравнением, отражающим особенности внутриутробного развития, так и прогностически значимыми на последующие годы жизни. Прерывание беременности в сроках сверхранних родов прекращает беспрецедентное четырехкратное увеличение массы тела плода, наблюдающееся с 26 по 40 недели беременности. Эти изменения сказываются не только на показателях физического развития, но и на психомоторном, соматическом статусе детей в ближайшем и отдаленном будущем [16].
Для объективизации оценки физического развития был использован центильный метод. Критерием оценки физического развития ребенка с ЭНМТ был параметр роста. С учетом центильных коридоров в постконцептуальном возрасте 38–40 недель значения роста в пределах 3–5 центильных коридоров, что соответствовало средним показателям в популяции, были отмечены у 38% детей, родившихся с ЭНМТ, у 13,5% величина роста относилась к зоне низких величин, у 48,5% – к зоне очень низких величин (1–2 центильных коридора).
Показатели массы тела, находящиеся в зоне средних величин (то есть от 25 до 75 центилей), были у 67,2% детей, у 32,8% – в пределах 3–10-го центиля и даже ниже 3-го центиля. Распределение показателей окружности груди у детей с ЭНМТ соответствовало распределению значений длины тела.
В возрасте скорригированных 6 месяцев разброс показателей массы тела, роста, окружности груди по центильным коридорам представляется следующим образом: величина роста у 53,5% детей располагалась в зоне средних величин, 46,5% имели низкие и очень низкие значения.
Дефицит массы тела в возрасте 6 месяцев отмечался у 60,5% детей, то есть величина массы располагалась в области низких и очень низких величин.
В скорригированном возрасте 1 года (фактический возраст 14–15 месяцев) 51,43% детей имели средние показатели роста, 48,57% сохраняли отставание в росте, причем у 31,43% величина роста располагалась в зоне очень низких значений, у 17,14% детей – в зоне низких значений. Распределение величины массы тела по центильным коридорам показало увеличение числа детей с формированием дефицита массы тела до 71,43% (у 60% из них в пределах очень низких значений).
Учитывая распределение величины роста, массы тела, окружности груди была определена гармоничность физического развития ребенка.
К 6 месяцам скорригированного возраста (фактически к 8–9 месяцам) низкое физическое развитие было отмечено у 44,2% детей, у 34,9% – среднее и гармоничное, у 20,9% – среднее дисгармоничное с формирование дефицита массы тела.
К возрасту 1 года (15 месяцев жизни) 47,7% имели низкое гармоничное развитие, число детей с дефицитом массы тела при средних параметрах роста увеличилось до 25,7%.
Таким образом, к 2–3 месяцам жизни дети с ЭНМТ удваивают или утраивают начальную массу тела, длина тела увеличивается на 9–12 см. К 8–9 месяцам дети увеличивали свою массу тела в 4–7 раз от первоначального веса, а к 14–15 месяцам – увеличивали в 7–9 раз. Достаточно высока и скорость роста у недоношенных детей. К 8–9-месячному возрасту, что соответствует скорригированным 6 месяцам, длина тела увеличивается на 29–30 см, к 15 месяцам (скорригированный год жизни) – 38–40 см.
Несмотря на интенсивность процессов нарастания массы тела и роста, крайне незрелые дети по абсолютным показателям роста и массы тела значительно отстают («миниатюрные» дети) от сверстников. Соматические показатели этих детей располагаются в 1–2 «коридорах» центильных таблиц, то есть их развитие чаще оценивается как низкое или очень низкое. По результатам нашего исследования таких детей было около 30% из всех наблюдений. И в последующие годы жизни глубоко недоношенные дети могут сохранять своеобразную гармоническую «поддержку» физического развития.
На формирование задержки роста у детей с ЭНМТ к постконцептуальному возрасту 38–40 недель и к скорригированному возрасту одного года, как установили наши исследования [16], влияет наличие хронической фетоплацентарной недостаточности декомпенсированной формы (r=0,28; р<0,01); нарушение маточно-плацентарного кровотока III степени (r=0,36; р<0,01), анемия матери во время беременности (r=0,37; р<0,01), эндокринная патология (r=0,25; р<0,05).
В институте проведено исследование кислородного статуса крови детей с ЭНМТ [16] и выявлено, что развитие хронической тканевой и клеточной гипоксии с признаками эндогенной интоксикации препятствует адекватному росту недоношенного ребенка, не позволяя ему достичь к постконцептуальному возрасту 38–40 недель антропометрических параметров, соответствующих доношенным детям. Среди лабораторных параметров была выявлена достоверно значимая корреляция между отставанием в росте ребенка в год и следующими параметрами кислородного статуса в возрасте 38–40 недель гестации: напряжение кислорода (рO2, r=-0,34; р<0,01); уровень фракции деоксигемоглобина (r=0,36; р<0,01); уровень лактата (r=0,35; р<0,01); сатурация кислорода (sO2, r=-0,36; р<0,01), общая концентрация кислорода (ctO2, r=-0,4; р<0,01); значение внутрилегочного шунта (Tshunt, Т/с – r=0,36; р<0,01), уровень дыхательного индекса (RI, r=0,62; р<0,01), альвеоло-артериальный градиент по кислороду (pO2 (А-а), r=0,33; р<0,01).
На основании этих исследований методом дискриминантного анализа были выделены информативные признаки и сформирован способ прогнозирования дефицита роста у детей с ЭНМТ в постконцептуальном возрасте 38–40 недель (Патент на изобретение № 2467328 от 20 ноября 2012 г.).
Восстановление показателей обменных процессов не происходит и к году жизни. При формировании программы реабилитации на III этапе на основании правила прогноза нарушения роста определяются сроки поступления детей с ЭНМТ на реабилитацию с обязательной коррекцией изменений в кислотно-основном состоянии (уровень лактата крови и уровень напряжения кислорода при 50% насыщении), выявленных в капиллярной крови с последующей адекватной коррекцией. Это позволяет улучшить метаболизм детей, уменьшить дефицит массы тела.
Заключение
Таким образом, основными синдромами, выявленными при катамнестическом обследовании, остаются нарушения мышечного тонуса, изменение ликвородинамики, снижение интеллектуально-анамнестических функций, дефекты общения. У таких детей болезнь рассматривается как последовательность смены симптомов. Поэтому в алгоритм обследования наряду с клинической симптоматикой неврологического заболевания должен входить анализ соматического, физического и психологического статуса. Для этого в институте разработан метод поэтапного выхаживания детей с ЭНМТ и медико-психологической адаптации семьи этих детей: совместное пребывание матери с глубоко недоношенным ребенком предполагает деонтологические аспекты диагноза для семьи. Комплексная терапия включает лекарственную терапию (приоритетность назначения в зависимости от доминантного симптома: антиконвульсанты, ноотропы, ноотрофы, антиспастические средства и др.); физические факторы, санаторно-курортное лечение.
На каждом этапе реабилитации (II и III этапы госпитализации) в программе помощи формируется «многоступенчатый диагноз», в который включаются сопутствующие осложнения со стороны всех органов и систем. Это помогает определить в дальнейшем программу санаторно-курортного лечения с использованием природных лечебных факторов в адекватных дозировках, что повышает резервные возможности функциональных систем организма недоношенного ребенка и способствуют улучшению приспособительных реакций. По программе санаторно-курортного лечения «Озеро Горькое» был пролечен 141 ребенок с детским церебральным параличом, из них 12 детей – с ЭНМТ, получены положительные результаты.



