На сегодняшний день воспалительный патогенез многих пролиферативных гинекологических заболеваний (аденомиоз, миома матки (ММ), эндометриоз-ассоциированное бесплодие и другие) не вызывает сомнений [1, 2].
В литературе представлены убедительные данные о том, что хроническое активное иммунное воспаление играет существенную роль в формировании ММ [3, 4]. Известно, что в случае наличия хронического воспалительного иммунного профиля (вследствие хронического слабовыраженного системного воспаления) в матке, подвергающейся воздействию ряда повреждений, включая внутриматочные инфекции, внутриматочные вмешательства и менструации, иммунная система включает механизмы пролиферации и фиброза, что приводит к формированию миомы [5, 6]. Обнаружено достоверное повышение провоспалительных медиаторов и цитокинов, а также профибротических субстанций при ММ [1, 7].
В последние годы существенное значение воспалению придается и в репродуктологии. Известно, что ряд репродуктивных процессов, таких как овуляция, менструация, плацентация и беременность, во многом зависят от статуса воспалительной системы [8]. Очевидно при этом, что дисрегуляция степени или длительности воспаления напрямую сопряжена с патофизиологией инфертильности. Это и позволяет предположить, что ряд заболеваний, ассоциированных с бесплодием, также связаны с хроническим слабовыраженным системным воспалением. Роль хронического воспаления изучена при бесплодии и синдроме поликистозных яичников, эндометриоз-ассоциированном бесплодии, первичной яичниковой недостаточности и ряде других заболеваний [9–11].
Пока до конца непонятно, каким образом хроническое асептическое воспаление влияет на фертильность. В качестве гипотезы рассматриваются предположения о воздействии на фолликулогенез посредством оксидативного стресса [12], а также влияние на рецептивность эндометрия [13].
Для хронического асептического воспаления характерны накопление и повышение концентрации эндогенных молекул, высвобождаемых из поврежденных или погибших клеток, называемых молекулярными паттернами, связанными с повреждением (damage-associated molecular pattern, DAMPs), которые могут являться ценными биомаркерами для изучения степени воспаления. DAMPs могут формироваться из различных источников и включают внеклеточные белки, такие как бигликан и тенасцин С, и внутриклеточные белки, такие как высокомобильная группа box 1 (HMGB1), гистоны, белки S100, белки теплового шока (HSP) и белки плазмы, такие как фибриноген, Gc-глобулин и сывороточный амилоид А и проч. [14].
На наш взгляд, с учетом данных литературы, представляет интерес изучение системного содержания DAMPs как маркеров системного асептического воспаления (фактор некроза опухоли альфа (ФНО-α), белок S100, интерлейкин-10, глутатион, мочевая кислота, холестерин липопротеинов низкой плотности (ХC-ЛПНП), фибриноген) у фертильных женщин с ММ, пациенток с ММ и бесплодием в сравнении с контрольной группой здоровых женщин.
Цель исследования: изучить содержание DAMPs у пациенток с ММ при фертильности и инфертильности.
Материалы и методы
В соответствии с поставленной задачей в исследование были включены 90 пациенток репродуктивного возраста с ММ (FIGО 3–6 тип).
Проведено одноцентровое проспективное исследование, в которое были включены 90 женщин.
В ходе исследования пациентки были разделены на 2 группы. Основную группу составили 60 пациенток с интрамуральной ММ: из них 30 пациенток с ММ и бесплодием (основная группа); 30 фертильных пациенток с интрамуральной ММ составили группу сравнения. 30 здоровых женщин без ММ были включены в контрольную группу.
Обозначение обследованных групп: М+Б – основная группа с бесплодием; М-Б – группа сравнения без бесплодия; М- – контрольная группа.
Критерии включения в основную группу: возраст 20–35 лет; ММ (FIGO 3–6 тип); отсутствие беременности более 1 года регулярной половой жизни; регулярный менструальный цикл; отсутствие приема гормональных препаратов в течение последних 6 месяцев; неудачные попытки экстракорпорального оплодотворения в анамнезе; нормальный овариальный резерв (уровень антимюллерова гормона (АМГ)≥1,2 нг/мл); отсутствие оперативного лечения по поводу ММ в анамнезе; наличие информированного согласия на участие в исследовании.
Критерии включения в группу сравнения: возраст 20–35 лет; ММ (FIGO 3–6 тип); регулярный менструальный цикл; женщины, обратившиеся для планового и диспансерного наблюдения и подбора контрацепции в течение 12 месяцев после родов, у которых во время беременности и/или до беременности была диагностирована ММ; наличие информированного согласия на участие в исследовании.
Критерии исключения из основной группы: субмукозная ММ (по FIGO 0–2 тип) и субсерозная ММ (FIGO 7 тип); большие размеры миоматозного узла и матки (более 12 недель беременности) [15]; наличие острых воспалительных заболеваний органов малого таза; женское бесплодие трубного происхождения, верифицированное на момент исследования; женское бесплодие цервикального происхождения; женское бесплодие, связанное с мужскими факторами; женское бесплодие, связанное с отсутствием овуляции; низкий овариальный резерв (АМГ≥1,2 нг/мл); опухоли яичников; наличие в анамнезе оперативного лечения по поводу ММ; наличие распространенных форм эндометриоза, верифицированных при лапароскопии; онкологические заболевания, наличие у пациенток гиперпролактинемии, ассоциированной с макро- или микроаденомой гипофиза (по данным МРТ), дефицита массы тела (индекс массы тела < 19,9 кг/м2).
Критерии исключения из группы сравнения: субмукозная ММ (по FIGO 0–2 тип) и субсерозная ММ (FIGO 7 тип); большие размеры миоматозного узла и матки (более 12 недель беременности) [15].
Критерии включения в контрольную группу: отсутствие ММ при физикальном и ультразвуковом исследовании; в данную группу вошли женщины, обратившиеся для планового ежегодного осмотра, подбора контрацепции.
Локализацию миомы определяли с использованием классификации FIGO [16], а также особенностей влияния на фертильность узлов больших и небольших размеров (согласно клиническим рекомендациям МЗ РФ по ММ от 2020 г., большими следует считать узлы более 12 недель беременности) [15]. Ультразвуковая диагностика проводилась с использованием трансвагинального объемного датчика на аппарате Voluson E10 Expert. Исследование включало анализ социально-демографических и клинико-анамнестических данных пациенток обследуемых групп.
Забор проб крови для исследования проводился всем пациенткам в 1-ю фазу менструального цикла после окончания кровяных выделений для исключения искажения результатов вследствие физиологических воспалительных изменений в репродуктивной системе (менструация, овуляция, секреторная фаза цикла); а также на момент забора крови отсутствовали острые воспалительные заболевания или обострение хронических. Определяли содержание искомых DAMPs (ФНО-α, белок S100, интерлейкин-10, глутатион, мочевая кислота, ХС-ЛПНП, фибриноген) в сыворотке крови. Материалом для исследования являлись образцы сыворотки, полученной центрифугированием венозной крови в течение 20 минут со скоростью вращения 3500 оборотов в минуту (лабораторная центрифуга Elmi CM-6MT.02 (Латвия)).
Исследование ФНО-α, интерлейкина-10 проводилось методом иммуноферментного анализа. Содержание восстановленного глутатиона определяли посредством метода высокоэффективной жидкостной хроматографии. Указанный способ лабораторной диагностики позволяет распознать в образце биологического материала глутатион свободный и произвести точный подсчет его количественного содержания. Для определения белка S100 был использован иммунохемилюминесцентный анализ. Выявление мочевой кислоты в биохимическом анализе крови проводилось энзиматическим методом, фибриногена – клоттинговым методом, а оценка ЛПНП – колориметрическим методом.
Cтатистический анализ
Для анализа результатов использовали статистические компьютерные программы SPSS (версия 10.0.7) и Statistica (версия 10.0) for Windows, часть расчетов была осуществлена с помощью таблиц Excel. Различия между группами считали статистически значимыми при р<0,05.Для каждой группы пациенток распределение количественных показателей было проверено на соответствие нормальному распределению с помощью критерия Колмогорова–Смирнова. При описании нормально распределенных показателей использовали форму представления характеристик в виде среднего арифметического значения и стандартного отклонения М (SD); при распределении признаков, отличающихся от нормального, использовали описание в виде медианы (Me) и интерквартильного интервала в формате Me (Q1; Q3). Качественные показатели представлены как в абсолютных (n), так и в относительных (%) величинах.
При сравнении групп по количественным признакам, имеющим нормальное распределение и равенство дисперсий (по критерию Ливиня), применялись параметрические методы – критерий ANOVA с последующим попарным сравнением групп по t-критерию Стьюдента. В противном случае – при невыполнении данных требований – использовались непараметрические критерии Краскела–Уоллиса и Манна–Уитни. При множественных сравнениях использовали поправку Бонферрони для 3 независимых групп (p<0,017).
При сравнении качественных бинарных показателей в данной научной работе были использованы критерий Хи-квадрат (χ2) с поправкой максимального правдоподобия, двусторонний точный критерий Фишера или Z-критерий с поправкой для концевых точек (в случае сравнения 0% или 100%), которые позволяли определить, насколько независимо было распределение показателей в группах. При анализе факторов, влияющих на фертильность у женщин, и наличии ММ был рассчитан относительный риск заболевания с указанием 95% доверительного интервала (95% ДИ).
Зависимость между бинарными и количественными признаками оценивалась с помощью расчета коэффициента точечной бисериальной корреляции:
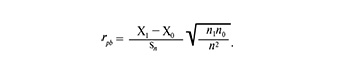
Результаты
Средний возраст обследованных пациенток основной группы составил 31,8 (3,7) года, группы сравнения – 31,4 (3,9) года, в контрольной группе – 32,3 (3,6) года (p>0,05).
Как следует из приведенных данных (табл. 1), у пациенток с ММ и бесплодием статистически значимо чаще регистрировали наличие оперативных вмешательств на органах малого таза, абортов и самопроизвольных выкидышей в сравнении с группой фертильных пациенток с ММ и группой контроля.
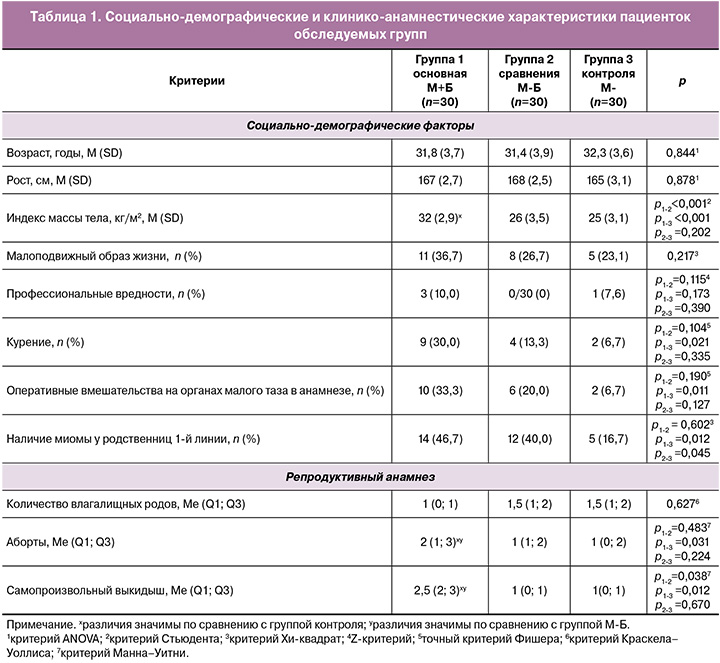
Результаты оценки DAMPs во всех обследованных группах представлены в таблице 2.
Полученные данные свидетельствуют о статистически значимом повышении уровней глутатиона, мочевой кислоты и ЛПНП при наличии ММ независимо от фертильности в сравнении с показателями контрольной группы. Более выраженные изменения показателей (повышение содержания белка S100, мочевой кислоты и ЛПНП, а также снижение содержания глутатиона) выявлены при наличии интрамуральной ММ и бесплодии в сравнении с фертильными и здоровыми пациентками. Статически значимых изменений показателей фибриногена, ФНО-α и интерлейкина-10 на системном уровне не зарегистрировано.
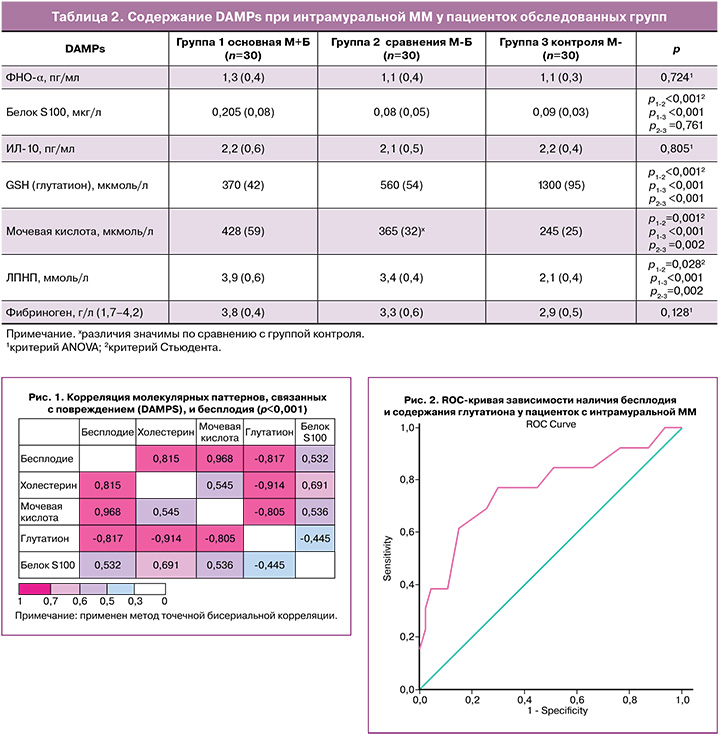
На следующем этапе исследования проведен корреляционный анализ методом точечной бисериальной корреляции, который показал сильную положительную зависимость между наличием бесплодия (качественный показатель, где 1 – есть бесплодие, 0 – нет бесплодия) и показателями ЛПНП (R=0,832, p<0,001), мочевой кислоты (R=0,985, p<0,001), белка S100 (R=0,739, p<0,001) и сильную отрицательную зависимость с показателем глутатиона (R=-0,821, p<0,001).
С помощью ROC- анализа были рассчитаны пороговые значения (точка «сut off») для исследуемых показателей, при достижении которых увеличивается риск формирования бесплодия при интрамуральной ММ.
Проведенный ROC-анализ (АUC=0,768±0,083, p=0,003) определил значение показателя GSH (глутатион), равное 413,0 мкмоль/л, как пороговое значение, ниже которого риск возникновения бесплодия возрастает в 2,56 раза (относительный риск (ОР)=2,56, 95% ДИ 1,43–4,57, p<0,001). Чувствительность данного фактора в качестве предиктора развития бесплодия у женщин с интрамуральной ММ составила 76,67% (95% ДИ 59,07–88,21%), специфичность – 70,0% (95% ДИ 59,07–88,21%), общая точность – 73,33% (95% ДИ 58,79–84,13%) (рис. 2).
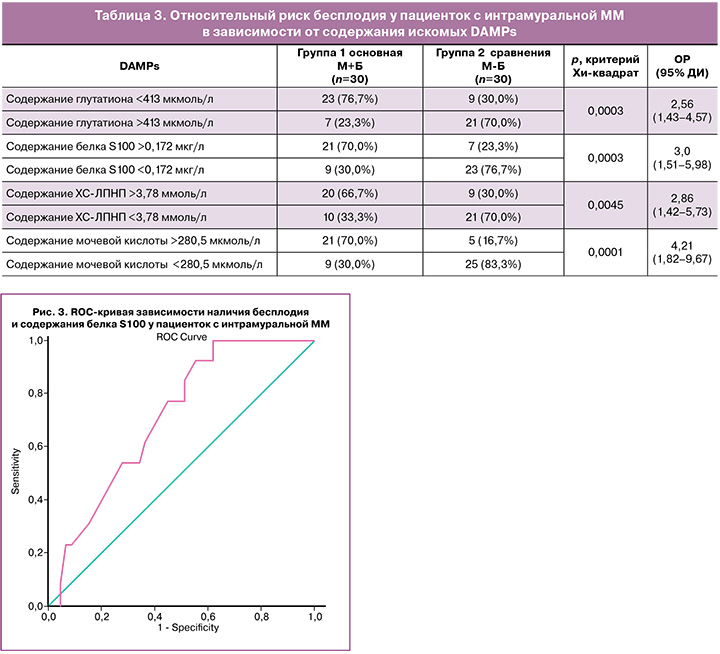
С помощью ROC-анализа (АUC=0,714±0,070, p=0,019) было определено значение показателя «белок S100», равное 0,172 мкг/л, в качестве порогового значения, выше которого риск возникновения бесплодия возрастает в 3 раза (ОР=3,0, 95% ДИ 1,51–5,98, p<0,001). Чувствительность данного фактора в качестве предиктора развития бесплодия у женщин с интрамуральной ММ – 70,0% (95% ДИ 52,12–83,34%), специфичность – 76,67% (95% ДИ 59,07– 88,21%), общая точность – 73,33% (95% ДИ 58,79–84,13%) (рис. 3).
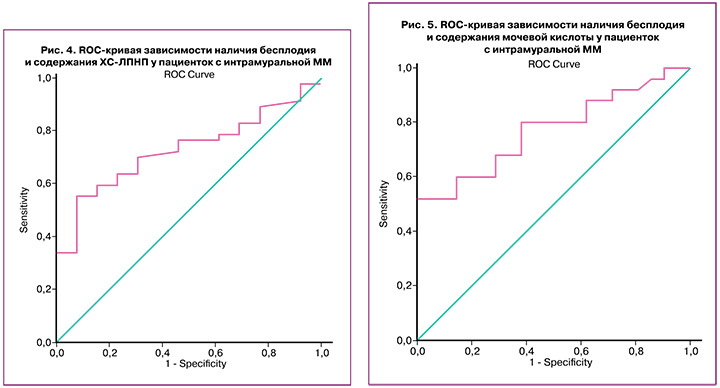
Используя ROC-анализ (АUC=0,730±0,067, p=0,012) для показателя ЛПНП, было определено пороговое значение, равное 3,78 ммоль/л, выше которого риск возникновения бесплодия возрастает в 2,86 раза (ОР=2,86, 95% ДИ 1,42–5,73, p<0,001). Чувствительность данного фактора в качестве предиктора развития бесплодия – 66,67% (95% ДИ 48,78–80,77%), специфичность – 76,67% (95% ДИ 59,07–88,21%), общая точность – 71,57% (95% ДИ 58,86–82,92%) (рис. 4).
Полученное с помощью ROC-анализа (АUC=0,772±0,069, р=0,002) значение мочевой кислоты, равное 280,5 мкмоль/л, можно считать фактором риска бесплодия у пациенток с интрамуральной ММ. Определено значение показателя мочевой кислоты равное 280,5 мкмоль/л,
выше которого риск возникновения бесплодия возрастает в 4,2 раза (ОР=4,20, 95% ДИ 1,82–9,67, p<0,001). Чувствительность данного фактора в качестве предиктора развития бесплодия у женщин с ММ составила 70,0% (95% ДИ 52,12–83,34%), специфичность – 83,33% (95% ДИ 66,44–92,66%), общая точность – 76,67% (95% ДИ 62,69–86,53%) (рис. 5).
Суммарный относительный риск бесплодия у пациенток с интрамуральной ММ в зависимости от содержания искомых DAMPs представлен в таблице 3.
Таким образом, проведенное исследование выявило ряд показателей – маркеров DAMPs (глутатион, ЛПНП, белок S100, мочевая кислота), которые могут быть использованы в качестве диагностических и прогностических маркеров инфертильности при наличии интрамуральной ММ.
Обсуждение
Проведенное исследование позволило установить статистически значимые уровни сывороточных концентраций молекулярных паттернов, связанных с повреждением (DAMPs), как биомаркеров хронического асептического воспаления у пациенток с ММ и бесплодием в сравнении с фертильными пациентками с ММ и группой контроля: повышение концентраций белка S100, мочевой кислоты, ХН-ЛПНП и снижение концентрации глутатиона. Рассчитан относительный риск бесплодия у пациенток с интрамуральной ММ в зависимости от содержания искомых DAMPs.
До настоящего времени интрамуральная ММ не рассматривается в качестве фактора бесплодия, однако может являться таковым в отсутствие других причин. Проведенное исследование подтверждает гипотезу о том, что, по всей вероятности, при наличии определенного уровня системного слабовыраженного асептического воспаления, эти изменения в сочетании с ММ приводят к нарушениям в репродуктивной системе в виде инфертильности.
С момента, как Полли Матцингер в 1994 г. предложила гипотезу («модель опасности») о новых механизмах активации естественного и адаптивного иммунного ответа, прошло уже более 30 лет [17]. Согласно этой теории, функцией врожденной иммунной системы защиты является идентификация «опасных сигналов», описанных как молекулярные паттерны, связанные с повреждением (DAMPs), и ответ на них посредством активации иммунной системы и создания провоспалительной среды. DAMPs – это молекулы, которые свойственны организму, но обладают крайне высокими провоспалительными свойствами в тех случаях, когда выявляются в несвойственных себе формах, таких как экстрацеллюлярная или свободная. Они и являются индикатором тканевого повреждения и системного воспаления [18].
Стрессорные факторы, способствующие высвобождению DAMPs, разнообразны и включают в себя широкую линейку физического воздействия (травма, радиация), химического воздействия (токсины, осмолярность), метаболического (ишемия, реперфузия), инфекционного (вирусы, бактерии и протозойные), а также запрограммированную клеточную гибель [19].
Уже в 2015 г. основательно была предложена гипотеза о том, что большинство заболеваний человека связаны с нарушенным/измененным («встревоженным») физиологическим гомеостазом под воздействием тканевого повреждения, клеточного стресса или даже незначительного метаболического нарушения вне- и внутриклеточного окружения. Заболевания человека на сегодняшний день могут в целом рассматриваться в свете индуцированного повреждением ответа врожденной иммунной системы. Принципиальная модель может выглядеть следующим образом: микробное/немикробное (стерильное) стрессовое воздействие > клеточный стресс/тканевое повреждение > выработка DAMPs > распознавание PRP-клетками иммунной системы > активация врожденной иммунной системы >инфекционный/стерильный воспалительный ответ. Вне стрессового воздействия DAMPs находятся внутриклеточно и не распознаются иммунной системой [20].
В настоящем исследовании получены данные об ассоциации изменения ряда DAMPs с бесплодием при интрамуральной ММ: повышение концентрации мочевой кислоты, белка S100, холестерина ЛПНП и снижение концентрации глутатиона в сравнении с пациентками контрольной группы и фертильными с ММ. Рассмотрим каждый из достоверно измененных показателей.
Глутатион – уникальная молекула, необходимая для жизни и принимающая участие в поддержании клеточного гомеостаза, а также первостепенной защите от оксидативного повреждения, которое регистрируется при ряде заболеваний. Эта молекула характеризуется как «мастер-антиоксидант» во всех тканях человеческого организма и задействована в антиоксидантной защите, детоксикации ксенобиотиков, регуляции внутриклеточного окислительно-восстановительного потенциала, сигнальной системе клетки, формировании и функционировании белков, экспрессии генов, дифференцировке/пролиферации, иммунном ответе и противовирусной защите [21]. Именно поэтому глутатион и называют «Самсоновской (могучей) маленькой молекулой» [22]. Глутатион обнаружен во всех компонентах клетки и циркулирует между компартментами как буфер для реактивных форм кислорода [23]. В последние годы стало известно, что глутатион может действовать и как антиоксидант, и как прооксидант, а также как кофактор антиоксидантных и детоксицирующих ферментов [24].
В настоящем исследовании верифицировано снижение сывороточных концентраций глутатиона у инфертильных пациенток с интрамуральной ММ. Подобные изменения концентрации глутатиона в литературе также выявлены при хронических заболеваниях легких [25]; болезни Паркинсона [26], кардиоваскулярных заболеваниях [27] и ряде других.
Несколько неожиданными являются результаты настоящего исследования в части верификации снижения концентрации глутатиона в основной группе пациенток наряду с повышением остальных показателей, поскольку, если рассматривать его как прооксидант, то более ожидаемым было бы выявление повышения его концентраций. Однако, учитывая его антиоксидантные свойства, можно предположить, что снижение концентрации обусловлено избыточным его длительным потреблением.
Белок S100 – не менее интересный DAMPs, открытый еще в 1965 г. Блейком Муром, который и назвал его так, поскольку это вещество на 100% растворялось в сульфате аммония в нейтральной pH среде [28]. Этот кальций-связывающий протеин, представленный в виде различных типов в органах и тканях, является одним из регуляторов Ca2+ концентрации внутри клеток организма.
Семейство этих протеинов называют «тревожными звоночками» [29]. Они играют существенную роль в процессах воспаления и иммунного ответа, обеспечивая защиту макроорганизма, запуская иммунный ответ. Как пример стерильного воспаления, выражающегося, в том числе, в повышении концентрации некоторых типов белка S100, возможно привести такие заболевания как подагра, аллергия, артрит, атеросклероз, аутоиммунные заболевания, заболевания кишечника [30].
Результаты настоящего исследования свидетельствуют о том, что у инфертильных пациенток с ММ повышены сывороточные концентрации белка S100 в сравнении с фертильными и здоровыми женщинами. По всей вероятности, этот протеин в данном случае обладает актиоксидантными свойствами и его повышение свидетельствуют о слабовыраженном системном асептическом воспалении. В литературе представлены данные о том, что белок S100 играет существенную роль в процессах успешной имплантации, развитии эмбриона и течении беременности. Интересно, что он присутствует в амниотической жидкости, ткани эндометрия и головном мозге плода, а изменения его концентрации могут приводить к осложнениям беременности [31, 32].
Мочевая кислота – является продуктом катаболизма пуринов и также относится к DAMPs, высвобождаемыми ишемизированными тканями и гибнущими клетками. Мочевая кислота присутствует во всех нормальных клетках, а также в биологических жидкостях [33].
C одной стороны, мочевая кислота действует как прооксидантная молекула, снижая доступность оксида азота, повышая продукцию реактивных форм кислорода, стимулируя хемотаксис [34]. С другой стороны, рассматривается как антиоксидант, обладающий выраженными защитными свойствами. Таким образом, этот DAMPs является неким двуликим Янусом и, по современным данным, ее свойства, по всей вероятности, зависят от конкретной клинической ситуации [35]. В фундаментальных исследованиях представлены данные о наличии антиоксидантных свойств мочевой кислоты только в гидрофильной среде, однако достоверно доказаны и ее биологически активные провоспалительные свойства [36].
Полученные нами данные о повышении концентрации мочевой кислоты при бесплодии у пациенток с интрамуральной ММ согласуются с гипотезой наличия системного хронического асептического воспаления, в котором мочевая кислота принимает участие как прооксидант и может являться одним из диагностических маркеров инфертильности.
Интересными являются также и обнаруженные нами данные в ходе подготовки к публикации данной работы о сходных изменениях концентрации мочевой кислоты у пациенток с бесплодием в ассоциации с возрастом и индексом массы тела [37, 38]. Опубликованные нами ранее данные о наличии метаболических нарушений у инфертильных пациенток с интрамуральной ММ, а также результаты этой работы, полностью согласуются с публикациями, представленными коллегами [39].
Холестерин – ЛПНП в качестве маркера хронического воспаления в рамках данного исследования тоже был предложен не случайно. Ведь метаболизм липидов, как известно, глубоко влияет на состояние как врожденного, так и адаптивного иммунного ответа. ЛПНП активируют иммунную систему посредством активации Toll-подобных рецепторов, что запускает провоспалительные механизмы защиты [40]. Фактически, фосфолипиды на поверхности ЛПНП распознаются организмом как DAMPs [41]. Известно, что в условиях хронического воспаления обычная провоспалительная среда повреждает молекулы, регулирующие эффероцитоз. Дефектный эффероцитоз приводит к тому, что апоптические клетки аккумулируются и подвергаются вторичному некрозу, что, в свою очередь, приводит к выработке остальных DAMPs. Эти звенья патогенеза уже достаточно подробно изучены при атеросклерозе [42].
В литературе представлены данные о том, что формирование ММ и рецидивы связаны с повышенным уровнем ЛПНП [43, 44]. В одной из работ доказана ассоциация между размером ММ и липидным профилем [45]. Полученные нами данные согласуются с литературными: у фертильных пациенток с ММ достоверно выше содержание ЛПНП в сыворотке крови в сравнении с группой контроля.
При этом обращают на себя внимание более выраженные изменения содержания ЛПНП в группе инфертильных пациенток с ММ. Известно, что измененный липидный метаболизм достоверно влияет на гормональный профиль, функцию яичников и матки, что без сомнений оказывает влияние на фертильность. Коллегами уже представлены результаты анализа, свидетельствующего о том, что измененные концентрации ЛПНП являются фактором риска формирования бесплодия [46].
Заключение
Таким образом, проведенное исследование позволяет сделать ряд выводов. Во-первых, при интрамуральной ММ выявлены изменения на системном уровне, характеризующиеся как системное слабовыраженное хроническое асептическое воспаление, что выражается в изменении показателей DAMPs в виде прооксидантного сдвига. Во-вторых, группа пациенток с интрамуральной ММ является неоднородной по степени выраженности системного стерильного воспаления. При этом степень провоспалительных изменений строго ассоциирована с наличием такого симптома как бесплодие. Это существенно расширяет представления о патогенезе бесплодия при ММ и верифицирует наличие системных метаболических нарушений как кофактора инфертильности. В-третьих, предложенные маркеры DAMPs (глутатион, ЛПНП, белок S100, мочевая кислота) могут быть использованы в качестве диагностических и прогностических маркеров инфертильности при наличии интрамуральной ММ. При достижении значений пороговых показателей (глутатион менее 413 мкмоль/л; белок S100 более 0,172 мкг/л; мочевая кислота более 280,5 мкмоль/л; ЛПНП более 3,78 ммоль/л) относительный риск бесплодия возрастает.



