Рак шейки матки (РШМ) остается одной из наиболее распространенных злокачественных опухолей, выявляемых во время беременности. Частота его составляет 1,8–4 случая на 100 000 беременных, то есть около 3% всех впервые выявленных случаев приходятся на гестационный период [1].
Возраст беременных с РШМ в среднем составляет 35 лет, а средний срок гестации при установлении диагноза – 19,5 недели [1].
При выявлении РШМ во время беременности необходимо принять решение об объемах лечения, целесообразности химиотерапии, сроках и методе родоразрешения. Стратегия зависит от срока гестации, стадии заболевания, размера опухоли, вовлеченности лимфатических узлов и желания пациентки сохранить беременность.
Клинические проявления РШМ во время беременности зачастую отсутствуют или могут быть похожи на типичные акушерские осложнения (кровотечение, боли внизу живота и по ходу седалищного нерва, анемия). При ранних стадиях РШМ сам по себе не влияет на течение беременности. Однако при распространенном процессе повышается риск прерывания беременности и преждевременных родов [2, 3].
Скрининговым методом в диагностике заболеваний шейки матки является цитологическое исследование мазков. Окончательный диагноз ставится только на основании гистологического исследования. При выявлении микроинвазивного процесса возможно проведение атипичной конизации шейки матки с высотой конуса не более 1,5 см, но без выскабливания цервикального канала. Конизация может быть выполнена в любом сроке, но до родов должно оставаться не менее 4 недель. После конизации шейки матки при условии негативного гистологического края возможны влагалищные роды [4–7].
Размер опухоли и вовлеченность лимфатических узлов являются главными прогностическими факторами для пациенток с РШМ. Выполнение стандартизированной лимфаденэктомии (или биопсии сторожевого узла) в I и начале II (до 22 недель) триместров беременности является безопасной и информативной процедурой [6, 8–10].
На рисунке представлен алгоритм ведения пациенток с РШМ, выявленным во время беременности [4–6].
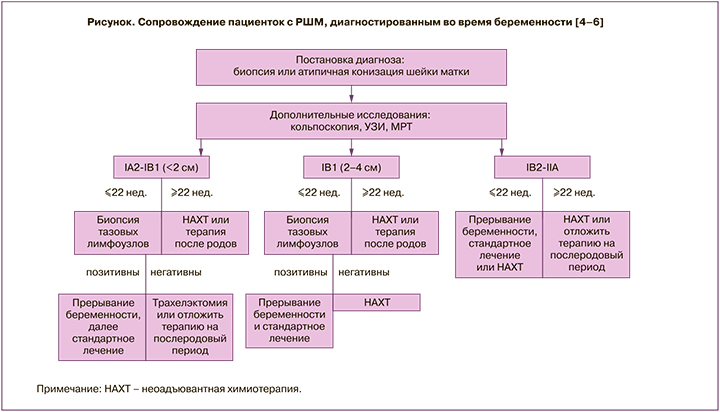
Vercellino G.F. et al. сообщили о 32 пациентках с РШМ, которым было проведено лапароскопическое стадирование. Только у 4 беременных были обнаружены метастазы в лимфатические узлы (у 3 – стадия по FIGO IB1, у одной – IIA). Ни в одном случае после лапароскопического вмешательства не развились акушерские осложнения [11].
Пациенткам с подтвержденными метастазами в лимфатические узлы показано проведение неоадъювантной химиотерапии (НАХТ). Трахелэктомия во время беременности сопряжена с множеством осложнений, в связи с чем целесообразность ее проведения в настоящее время обсуждается [8].
Химиотерапия противопоказана в I триместре в связи с риском прерывания беременности и формирования пороков развития у плода. Негативными последствиями ее являются риск задержки роста плода, преждевременных родов и маловесности новорожденных. Токсическое воздействие на плод включает возможное развитие снижения слуха и миелосупрессии [12, 13].
Согласно международным гайдлайнам, проведение химиотерапии во II и III триместрах беременности показано при [6, 9]:
- стадии IB1 с негативными лимфатическими узлами, при размере опухоли менее 2 см и желании пациентки сохранить беременность;
- стадии IB1 (размер опухоли 2–4 см) – до проведения исследования лимфатических узлов;
- стадии IB2–IIB – до родоразрешения.
Наиболее распространенными схемами НАХТ являются цисплатин (50–100 мг/м2) в качестве монотерапии или в комбинации с паклитакселом (175 мг/м2). Терапия должна проводиться 1 раз каждые 3 недели. Другим режимом является использование цисплатина 75 мг/м2 с ифосфамидом 2 мг/м2 каждые 2 недели [1, 6, 12].
Оптимальным временем для родоразрешения является промежуток между 37-й и 39-й неделями. Рекомендовано закончить курсы химиотерапии за 3 недели до родов в связи с риском развития миелосупрессии как у матери, так и у плода [10, 12, 14].
Метод родоразрешения определяется стадией процесса. При стадии IA1–2 (при условии проведения конизации шейки матки и негативном крае резекции) возможны роды через естественные родовые пути. При наличии опухолевой ткани в шейке матки показано родоразрешение путем операции кесарева сечения. Для предотвращения риска абдоминальных опухолевых имплантов рекомендовано проведение корпорального кесарева сечения. Кесарево сечение может сочетаться с проведением трахелэктомии или гистерэктомии [6, 14–16].
В ряде случаев сохранение беременности невозможно. В операбельных случаях может быть проведена радикальная гистерэктомия с плодом (в I и в начале II триместра беременности). В более поздних сроках вначале проводится опорожнение полости матки. При распространенном процессе химио- и лучевая терапия являются методом выбора. Лучевая терапия проводится после прерывания беременности или с плодом в полости матки. Спонтанное прерывание беременности обычно происходит в течение 4–6 недель после первого курса лучевой терапии и сопровождается повышенным риском развития инфекционных осложнений и диссеминированного внутрисосудистого свертывания [6, 15, 16].
Целью нашего исследования стало обобщение и анализ собственного опыта ведения беременных с инвазивным РШМ.
Материалы и методы
Проведено ретроспективное исследование всех случаев сочетания беременности и родов у пациенток с инвазивным РШМ, наблюдавшихся в родильном доме при ГКБ №40 за период с 2017 по 2020 гг. Анализ включал учет возраста пациенток, акушерских особенностей (паритет, акушерско-гинекологический анамнез, специфика течения беременности, родов), срока первичной диагностики РШМ. Также было проведено катамнестическое исследование новорожденных от матерей с выявленным во время беременности РШМ в течение 1 года жизни.
Результаты и обсуждение
Родильный дом при ГКБ №40 Департамента здравоохранения города Москвы с 2018 г. специализируется на помощи беременным с онкологическими заболеваниями.
За истекший период было выявлено 16 случаев инвазивного РШМ (таблица). Медиана возраста пациенток составила 34,5 года, а срок первичной постановки диагноза – 21,6 недели. Только в 1 случае диагноз РШМ (T3bN1M1) был поставлен на 50-й день после родов. Все женщины были повторнобеременными, 18,7% – первородящими.
Первичная диагностика во всех случаях включала цитологическое исследование мазков с шейки матки с последующей гистологической верификацией диагноза. В 4 случаях была выполнена атипичная конизация шейки матки.
В большинстве случаев течение беременности было физиологическим, у 3 пациенток развилась угроза прерывания беременности в сроках 12–14 недель. У 1 пациентки беременность закончилась самопроизвольным поздним выкидышем в сроке 16–17 недель после проведения биопсии шейки матки.
Две пациентки со стадией T2bN0M0 получали во время беременности НАХТ (доцетаксел+карбоплатин): 2 и 3 курса соответственно. У одной женщины развилась анемия легкой степени. Нарушений маточно-плацентарного и плодового кровотока на фоне химиотерапии не было.
Роды в срок произошли у 10 (62,5%) пациенток, преждевременно – у 5 (31,2%). В большинстве случаев (68,7%) выполнялась операция кесарева сечения. Медиана срока родоразрешения составила 36,3 недели (от 30 до 40 недель). Масса новорожденных в среднем была 3025±312 г (от 1600 до 4200 г).
В родильном доме при ГКБ №40 преимущественно проводится корпоральное кесарево сечение. У 7 (43,7%) пациенток после кесарева сечения проводилась операция Вертгейма, в 57% случаев – с транспозицией яичников.
Одной пациентке с РШМ T1b1NxMx в 14 недель была выполнена лапароскопия с биопсией тазовых лимфатических узлов. Метастазы в лимфатических узлах выявлены не были, и в дальнейшем течение беременности было неосложненным. От предложенной НАХТ пациентка отказалась. В доношенном сроке ей было выполнено корпоральное кесарево сечение и операция Вертгейма.
В таблице приведены данные о сроках диагностики и родоразрешения пациенток.
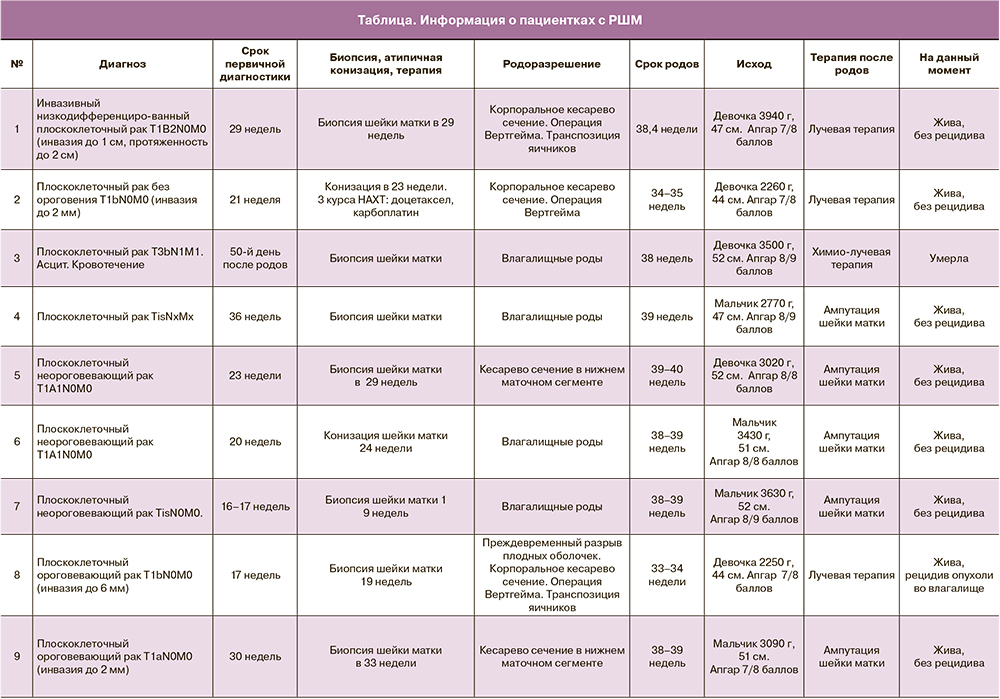
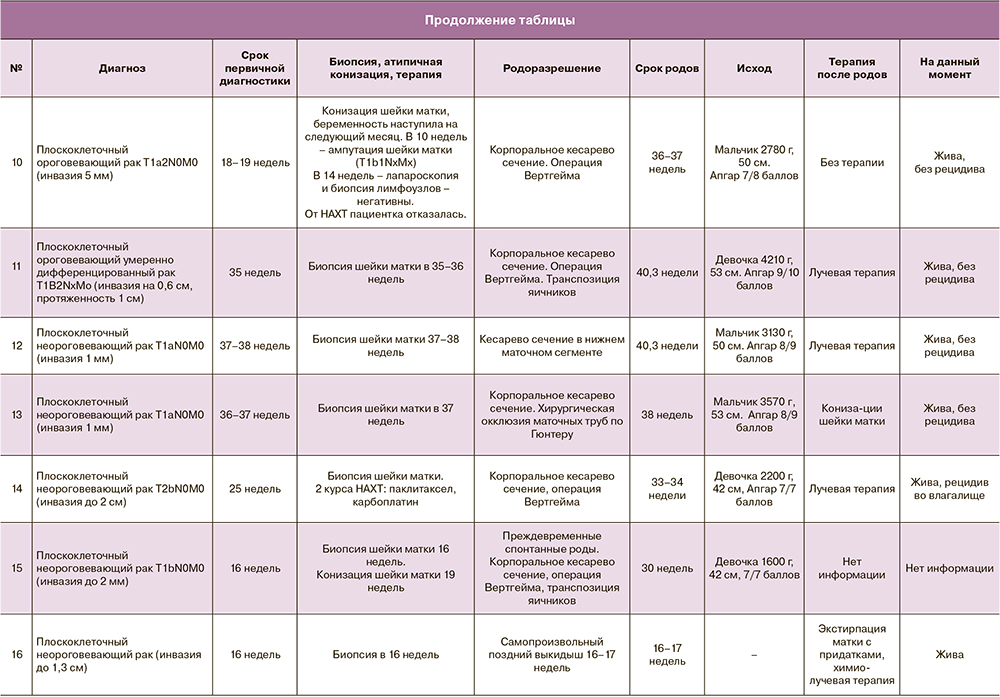
По настоящее время под наблюдением находятся 14 из исходных 16 пациенток. Рецидив опухоли выявлен у 2 (14,3%) женщин. Одна пациентка умерла через 8 месяцев после постановки диагноза (РШМ выявлен на 50-й день после родов, стадия T3bN1M1, асцит). Об одной пациентке нет информации.
В течение года после родов под наблюдением в кабинете катамнеза находились 12 детей, в том числе 2 – от матерей, получавших химиотерапию во время беременности. Рост и развитие всех детей соответствовали гестационному возрасту при рождении, дети от женщин с НАХТ не имели специфических отличий от других новорожденных.
Наш опыт ведения беременных с инвазивным РШМ пока немногочислен. Однако и на его основании можно сделать некоторые выводы.
Прежде всего диагностика заболеваний шейки матки должна проводиться на этапе прегравидарной подготовки или в I триместре беременности. Согласно базовому протоколу обследования беременных (приказ 572н от 2012 г.), цитологическое исследование мазков с шейки матки не проводится. Это связано с тем, что цитологическое исследование включено в обязательный объем диспансерного обследования, проводимого 1 раз в 3 года (приказ 36ан от 2015 г.) или ежегодно (приказ 572н от 2012 г.). В связи с этим изучение анамнеза и своевременное, при необходимости, дополнительное обследование должно проводиться с момента постановки на учет по беременности. Наши данные свидетельствуют о том, что средний срок выявления РШМ составляет 21,6 недели, что, безусловно, поздно.
Течение беременности у пациенток с инвазивным РШМ часто сопровождается сукровичными выделениями из половых путей или контактными кровотечениями, зачастую трактуемыми как симптомы начавшегося выкидыша или угрожающих преждевременных родов. Обязательный осмотр шейки матки при помощи зеркал может позволить своевременно вывить макроскопические изменения шейки матки и ускорить постановку верного диагноза [4, 14–16].
При цитологическом подозрении на РШМ обязательно выполняется биопсия. Возможно проводить ножевую или радиохирургическую биопсию из нескольких точек с размером участка не менее 7 мм. Целесообразность получения нескольких биоптатов обусловлена тем, что на шейке матки единовременно могут присутствовать как умеренная и тяжелая дисплазия, так и карцинома in situ или инвазивный рак. Проведение предварительной кольпоскопии позволяет выявить наиболее подозрительные участки и произвести забор материала именно с них. В связи с физиологическими гравидарными изменениями шейки матки проведение биопсии может сопровождаться кровотечением, к чему нужно быть готовым. Выскабливание цервикального канала во время беременности никогда не проводится, так как сопряжено с увеличением риска прерывания беременности [4, 15, 16].
В нашей больнице пока недостаточно опыта проведения лапароскопии с биопсией тазовых лимфатических узлов у беременных, но, согласно имеющимся международным публикациям, данная методика доступна в сроках до 22 недель беременности и не сопровождается повышением риска прерывания беременности.
При гистологически подтвержденном инвазивном РШМ проводится мультидисциплинарный онкологический консилиум с решением вопроса о дальнейшей тактике ведения пациентки. При необходимости проводится НАХТ или пассивное наблюдение с проведением терапии после родоразрешения [16]. Тактика определяется сроком беременности, стадией болезни и согласием женщины. Диагностика РШМ в IB2–IIA стадии является показанием для прерывания беременности в I триместре. При отказе пациентки и заинтересованности в сохранении беременности проводится НАХТ.
Оптимальным сроком родов является интервал между 37-й и 39-й неделями беременности. Методом родоразрешения является кесарево сечение, предпочтительно корпоральное. Кесарево сечение может сочетаться с трахелэктомией или гистерэктомией, с или без выполнения транспозиции яичников [3, 6, 15].
Заключение
РШМ является одним из наиболее часто выявляемых онкологических заболеваний у женщин репродуктивного возраста. Несмотря на широкое внедрение профилактических (вакцинация) и скрининговых (мазок на онкоцитологию) мероприятий, в мире пока не наметилось тенденции к снижению частоты данной патологии. Благодаря внедрению в практику клинических протоколов, с 2019 г. всем беременным при постановке на учет в женскую консультацию должен производиться забор материала с шейки матки для цитологического исследования. Соблюдение правил забора и транспортировки цитологического материала, а также тщательная его интерпретация являются залогом своевременного выявления пациенток группы риска по развитию РШМ. Дополнительное обследование этих пациенток с проведением тестирования на вирус папилломы человека и кольпоскопии, а при необходимости – и прицельной кольпоскопической биопсии позволит снизить частоту поздней диагностики РШМ.



