Молочная железа – это своеобразный интракринный, гормонозависимый орган, в котором есть все необходимые ферменты для локального синтеза и метаболизма эстрогенов. При этом концентрация эстрадиола (Е2) в кровотоке не отражает его уровень, синтезируемый в ткани молочной железы. Определение метаболитов эстрогенов в моче может в определенной степени отражать концентрацию эстрадиола в тканях. Основные метаболиты эстрадиола представлены в форме гидроксипроизводных эстрона – 2-ОНЕ1 (2-гидроксиэстрона) и 16α-ОНЕ1 (16α-гидроксиэстрона). Данные метаболиты характеризуются абсолютно противоположными биологическими свойствами. Если 2-ОНЕ1 обладает антипролиферативным эффектом, то 16α-ОНЕ1, наоборот, стимулирует клеточный рост [1, 2].
Для снижения уровня «канцерогенного» метаболита (16α-ОНЕ1) весьма перспективным является индолкарбинол. Противоопухолевой эффект этого вещества основан на широком спектре его активности [3]. Применение препарата на его основе, как показала практика, снижает риск злокачественной трансформации доброкачественных дисплазий молочной железы, предотвращает прогрессирование заболевания, предупреждает развитие мастопатии при предрасположенности к заболеваниям молочной железы и опухолевым заболеваниям женской половой сферы [4].
Индолкарбинол нормализует гормональный баланс, оказывает антипролиферативный эффект и стимулирует апоптоз, что делает его использование обоснованным в лечении циклической масталгии (мастодинии). Индолкарбинол способен нормализовать метаболизм эстрогенов путем усиления синтеза 2-ОНЕ1, обладающего защитным эффектом на гормончувствительные ткани, такие как молочная железа, матка, шейка матки. Высокая клиническая эффективность индолкарбинола как фармакологического корректора гиперпластических процессов в гормонозависимых тканях подтверждена в исследованиях, проводившихся на моделях диффузных мастопатий, миомы матки и дисплазий шейки матки [5, 6].
Целью проведенного исследования была оценка эффективности, безопасности и переносимости лекарственного препарата на основе индолкарбинола в лечении циклической масталгии (мастодинии), в том числе на фоне доброкачественной дисплазии молочной железы.
Материалы и методы исследования
Для решения поставленной цели проведено рандомизированное двойное слепое плацебо-контролируемое многоцентровое исследование лекарственного препарата на основе индолкарбинола (Индинол Форто) – средства таргетной терапии, созданного российскими учеными НИИ молекулярной медицины при Первом МГМУ им. И.М. Сеченова.
Исследование проводилось в 11 медицинских учреждениях России.
 Критерии включения: циклическая масталгия (мастодиния), в том числе на фоне доброкачественной дисплазии молочной железы (мастопатия); женщины в возрасте 20–45 лет, с регулярным менструальным циклом (26–30 дней), использующие негормональную контрацепцию, подписанное информированное согласие, одобренное локальным этическим комитетом.
Критерии включения: циклическая масталгия (мастодиния), в том числе на фоне доброкачественной дисплазии молочной железы (мастопатия); женщины в возрасте 20–45 лет, с регулярным менструальным циклом (26–30 дней), использующие негормональную контрацепцию, подписанное информированное согласие, одобренное локальным этическим комитетом.
Критерии исключения: доброкачественные и злокачественные новообразования; острые воспалительные заболевания молочных желез; гипер-, гипотиреоз; гиперпролактинемия; хронические заболевания других органов и систем.
Продолжительность исследования: период скрининга до 45 дней; период лечения пациентки в течение 6 менструальных циклов, 5 визитов к врачу.
В исследование включены 156 пациенток в возрасте 20–45 лет.
Группы наблюдения: 1-я группа – прием препарата Индинол Форто (производства МираксБиоФарма, Россия), содержащего 200 мг индолкарбинола в капсуле, по 200 мг 2 раза (400 мг) в сутки (104 пациентки); 2-я группа – прием плацебо по 1 капсуле 2 раза в сутки (52 пациентки).
Эффективность и безопасность оценивалась по следующим показателям: данные дневников пациенток, результаты пальпации молочных желез, результаты ультразвукового исследования (УЗИ) молочных желез, интенсивность боли оценивалась по визуально-аналоговой шкале (ВАШ). Данные дневников включали расчет и анализ средней интенсивности боли в молочных железах в течение менструального цикла (6 циклов), а также долю дней в цикле (%), в которые отмечалось нагрубание молочной железы.
Изучался анамнез, проводились тесты на инфекционные заболевания, пальпация молочных желез, гинекологический статус, тесты на беременность, УЗИ органов малого таза, УЗИ молочных желез в первую фазу цикла, общий анализ крови, общий анализ мочи, определение печеночных ферментов, определение уровней ФСГ, ЛГ, Е2, пролактина, тиреотропного гормона (ТТГ), уровня глобулина, связывающего половые стероиды (ГСПС), анализ мочи на метаболиты эстрогенов – 2-ОНЕ1 и 16α-ОНЕ1. Для определения метаболитов эстрогенов использовался набор для иммуноферментного анализа (производства Immunacare, США)
Безопасность препарата оценивалась в динамике по следующим показателям: анализ жалоб, физикального осмотра до начала исследования, при визитах 3 и 5. Общий анализ крови, общий анализ мочи и биохимический анализ крови проводились на визитах 2 и 4.
Для обеспечения большей мощности статистического анализа при анализе показателей, описываемых интервальными показателями с нормальным типом распределения, использовались параметрические методы. Для сравнения показателей в группах (для оценки гомогенности выборки) наряду с критерием Краскела–Уоллиса использован одномерный t-критерий Стьюдента для независимых выборок. Наряду с критерием ранговых сумм Вилкоксона и критерием Фридмана для оценки изменения показателей в динамике (визит скрининга – визит 5) использован дисперсионный анализ с повторными измерениями. Оценка 95% доверительных интервалов для показателя с бинарным типом шкалы произведена по Клопперу–Пирсону. Для статистической обработки результатов исследования использован пакет прикладных программ IBM® SPSS® Statistics версии 20.0.0 (IBM® Corporation) в операционной среде Microsoft Windows XP Professional. Для запланированных сравнений эффективности (номинальные переменные) значимость рассчитывалась как двусторонняя. Для показателей уровня Е2 в сыворотке крови дисперсионный анализ с повторными измерениями проводился для логарифмически преобразованных данных (в связи с данными о лог-нормальном характере распределения данного показателя).
Результаты исследования
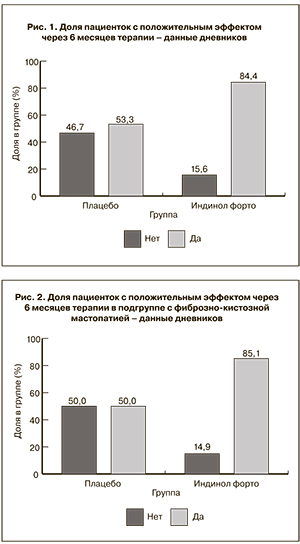
Поскольку циклическая масталгия (мастодиния) является преимущественно субъективным симптомокомплексом, эффективность препарата оценивалась по его влиянию на чувство боли и нагрубания в молочных железах. Пациентки использовали дневники, заполняемые ежедневно. Соответственно, критерием эффективности лечения был факт уменьшения (более чем на 2 балла по ВАШ) либо исчезновения ощущения боли и нагрубания в молочных железах. По данному критерию оценки эффективность лечения в группе терапии Индинолом Форто была значимо выше по сравнению плацебо как через 3 мес (80,2% по сравнению с 61,5%, р=0,044), так и через 6 мес лечения (84,4% по сравнению с 53,3%, р=0,002) (рис. 1). По данным пальпации и УЗИ молочных желез значимых различий выявлено не было.
Отдельного рассмотрения заслуживает вопрос эффективности лечения пациенток, у которых циклическая масталгия (мастодиния) развилась как проявление доброкачественной дисплазии молочных желез (мастопатии). В настоящем исследовании доля таких пациенток составила 67,5%. Диагноз устанавливался по данным УЗИ (наличие диффузных изменений ткани молочных желез и кист). Всего из 154 пациенток было 104 с мастопатией: 70 – в группе Индинола Форто, 34 – в группе плацебо. Частоты мастопатии в группах Индинола Форто и плацебо значимо не различались (р=1,0, точный критерий Фишера). По субъективному критерию оценки (по данным дневников пациентки) эффективность лечения в группе терапии Индинолом Форто значимо не различалась по сравнению с плацебо через 3 мес (78,9% по сравнению с 60,7%, р=0,118), но различалась через 6 мес лечения (85,1% по сравнению с 50,0%, р=0,004) (рис. 2).
По данным пальпаторного исследования молочных желез через 6 мес в группе терапии Индинолом эффективность была значимо выше, чем в группе плацебо, и составила 60,4 и 29,2% соответственно. Значимость различий в группах: р=0,023 (точный критерий Фишера). Точная односторонняя значимость: р=0,012 (точный критерий Фишера).
Ультразвуковая оценка размеров кист проводилась до и через 6 мес после начала лечения. В группе приема Индинола отмечено уменьшение размеров кист у 18% пациенток, стабилизация – у 71%, рост кист – у 11%. В группе плацебо отмечена стабилизация размеров кист – у 75% пациенток, рост кист – у 25%, уменьшения размеров кист отмечено не было.
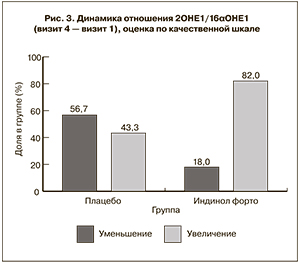
Проведен анализ метаболитов эстрогенов: соотношение 2ОНЕ1/16αОНЕ1. Данные исходного измерения (визит 1) и конечного измерения (визит 4), а также динамика показателя приведены ниже (рис. 3)
 Сравнение уровня репродуктивных гормонов показало отсутствие разницы в уровне ФСГ, ЛГ, а также ТТГ, однако установлен достоверный прирост уровня ГСПС, что, по-видимому, стало основанием для снижения свободного Е2 через 6 мес лечения (с 8,2 до 6,1 соответственно).
Сравнение уровня репродуктивных гормонов показало отсутствие разницы в уровне ФСГ, ЛГ, а также ТТГ, однако установлен достоверный прирост уровня ГСПС, что, по-видимому, стало основанием для снижения свободного Е2 через 6 мес лечения (с 8,2 до 6,1 соответственно).
Оценка безопасности и переносимост
Общее количество нежелательных явлений (НЯ), зафиксированных в ходе настоящего исследования – 52 (13 в группе плацебо, 39 в группе терапии Индинолом Форто). В 46 случаях из 52 (88,5%) тяжесть отмеченных НЯ классифицирована исследователем как легкая, в 6 случаях (11,5%) – как умеренная.
Из 52 НЯ для 1 случая исследователь не характеризовал связь НЯ с приемом препарата (протеинурия, оксалурия легкой степени). Из прочих НЯ для 21 случая связь с точки зрения исследователя отсутствовала, для 17 случаев – была вероятной, для 13 случаев – возможной. Значимые различия в 1-й и 2-й группах по количеству пациенток, у которых было отмечено наличие НЯ, не обнаружены (р=0,427, точный критерий Фишера).
Согласно проведенному анализу, зависимость частоты НЯ от группы исследования отсутствует. Таким образом, в группе терапии Индинолом Форто не отмечалось большее количество НЯ (как в целом, так и для визитов 1–4) по сравнению с группой плацебо.
Был проведен анализ параметров жизненно важных функций организма и данных объективного исследования в группах исследования (группа пациенток, принимавших плацебо, и группа пациенток, принимавших Индинол) в динамике: визит скрининга – визит 5: масса тела, индекс массы тела, систолическое артериальное давление, диастолическое артериальное давление, частота сердечных сокращений, частота дыхательных движений, температура тела.
Для анализа использована смешанная модель дисперсионного анализа с повторными измерениями (mixed-model ANOVA). По результатам анализа отсутствовала как значимая динамика данных показателей на фоне терапии (или была клинически не значимой), так и связь с препаратом исследования.
Аналогичный анализ был проведен для показателей общего анализа крови, биохимического анализа крови (уровень общего белка, креатинина, глюкозы, АЛТ, АСТ, общего билирубина, прямого и непрямого билирубина), показателей анализа крови на гормоны (эстрадиол, пролактин, ФСГ, ЛГ, ТТГ). По результатам анализа также отсутствовала как значимая динамика данных показателей на фоне терапии (или она была клинически не значимой), так и связь с препаратом исследования.
На основании полученных данных о безопасности, можно сделать вывод о благоприятном профиле безопасности препарата Индинол Форто.
Обсуждение полученных результатов
Положительное воздействие, оказываемое индолкарбинолом (интринолом), обусловлено широким спектром его биологических активностей. Один из механизмов действия заключается во взаимодействии данного вещества с арилгидрокарбоновым рецептором (AhR)[7], при активации которого происходит усиление экспрессии CYP1A1 – изоформы цитохрома P450, гидроксилирующей эстрон во 2-м положении с образованием 2-OHE1 [3], обладающего выраженной антипролиферативной (антиэстрогенной) активностью [2, 3]. В отсутствие индолкарбинола рецептор AhR активируется канцерогенными ариловыми углеводородами, поступающими в организм из окружающей среды или с продуктами питания (особенно с консервированной пищей), что способствует экспрессии CYP1B1 – изоформы цитохрома Р-450, гидроксилирующей эстрон по 16α- и 4-положениям с образованием 16α-OHE1 и 4-OHE1 [8]. Метаболит 16α-OHE1 способен ковалентно связываться с эстрогеновыми рецепторами, ядерными белками-гистонами и с ДНК, в результате чего происходит пролонгирование эстрогенной активности (эстроген-зависимого пролиферативного сигнала), а также инициация генотоксических повреждений ДНК [3, 9].
Индолкарбинол, проникая в клетку, препятствует фосфорилированию тирозиновых остатков киназ, что мешает каскадной передаче пролиферативных сигналов с поверхности к ядру клетки [10]. Кроме того, он ингибирует ядерный фактор транскрипции NF-κB, который является основным активатором транскрипции большого числа генов, вовлеченных в пролиферацию и воспаление [10, 11]. Была также показана способность индолкарбинола и его метаболитов ингибировать в клетках экспрессию генов, кодирующих антиапоптотические белки Bcl-2, PI3K, и ген белка сурвивина, входящего в группу апоптоз-ингибирующих белков IAP [12–14]. Кроме того, есть данные, указывающие на антиоксидантные свойства индолкарбинола, а также на его способность подавлять ангиогенные, инвазивные и миграционные процессы при канцерогенезе в молочных железах [15–18]. Установлено, что индолкарбинол является многообещающим методом химиопрофилактики рака молочной железы [19–21].
Оценка эффективности Индинола Форто в лечении доброкачественной дисплазии молочных желез (мастопатии) проводилась на основании данных УЗИ и физикального обследования (пальпации) молочных желез. Критерием эффективности по данным УЗИ был факт уменьшения числа и/или размеров кист, исчезновения дуктэктазий, снижения эхоплотности ткани молочной железы, а по данным пальпации – факт нормализации либо положительной динамики плотности и однородности ткани молочной железы. Через 6 мес терапии в подгруппе с мастопатией по результатам сравнения эффективности в группах терапии (оценка эффективности по данным пальпации) группы Индинола Форто и плацебо значимо различались (р=0,023, точный критерий Фишера). Эффективность в группе Индинола Форто была выше, чем в группе плацебо (60,4% по сравнению с 29,2%). По данным УЗИ значимых отличий не было. Значительная разница в частоте положительного эффекта Индинола и плацебо на плотность ткани молочной железы позволяет обосновать его эффективность в лечении доброкачественной дисплазии молочных желез (мастопатии).
По результатам изучения изменений гормонального профиля пациенток на фоне лечения было установлено, что в группе Индинола Форто происходит прирост содержания ГСПС в плазме крови и увеличение соотношения метаболитов эстрогенов в моче 2ОНЕ1/16α-OHE1. Последний эффект был также ранее описан в научной медицинской литературе [8, 20, 22, 23]. Оба данных факта свидетельствуют о том, что один из механизмов действия препарата может быть связан со снижением пролиферативной активности в ткани молочной железы вследствие снижения уровня ее эстрогенной стимуляции. А именно, рост содержания ГСПС в плазме крови приводит к снижению фракции свободных эстрогенов, в целом понижая эстрогенный фон, а увеличение соотношения 2ОНЕ1/16α-OHE1 обусловливает сдвиг метаболизма эстрогенов в сторону 2-гидроксиэстрона, практически не стимулирующего пролиферативные процессы в эстроген-чувствительных тканях.
Таким образом, в ходе проведенного исследования была доказана эффективность нового мультитаргетного лекарственного средства для лечения пациенток с циклической масталгией (мастодинией) и мастопатией. Учитывая, что известные механизмы действия индолкарбинола характеризуют его как средство, обладающее онкопротекторным эффектом [19–21], данный результат особенно важен в плане профилактики рака молочной железы у пациенток с циклической масталгией. По результатам проведенного исследования Министерством здравоохранения России был зарегистрирован первый в мире лекарственный препарат на основе индолкарбинола – Индинол Форто.
Выводы
- Начиная с 3-го месяца лечения, в группе плацебо положительная динамика сменилась отрицательной, в отличие от группы, принимающей Индинол Форто, где улучшение состояния пациентов продолжилось.
- Согласно объективной оценке (УЗИ) и пальпации молочных желез, отмечена положительная динамика в группе Индинол Форто к 6-му месяцу лечения.
- Индинол Форто повышает соотношение 2ОНЕ1/16αОНЕ1, способствуя антипролиферативному эффекту. Снижение на фоне терапии уровня глобулина, связывающего половые стероиды, ведет к уменьшению свободных фракций эстрогенов.
- Препарат Индинол Форто может быть рекомендован для мультитаргетной терапии пациенток как с циклической масталгией (мастодинией), так и мастопатией. Оптимальная длительность курса лечения – 6 месяцев.



