В настоящее время вспомогательные репродуктивные технологии широко применяются для лечения бесплодия, и с каждым годом увеличивается количество пациентов, проходящих лечение в программе ЭКО. Несмотря на постоянное совершенствование технологий в лечении бесплодия, эффективность программ ЭКО не превышает 30–35% [1].
Одним из основных способов улучшения результативности ЭКО является выбор эмбриона с высоким потенциалом к имплантации [2, 3]. В современной практике качество переносимых эмбрионов в основном оценивается согласно морфологическим критериям, включающим скорость, своевременность и равномерность деления клеток, форму бластомеров, степень их фрагментации и другие [4]. Однако информативность метода морфологического отбора эмбрионов не достаточно высока [5, 6].
В связи с этим возникает необходимость поиска новых критериев, определяющих качество эмбрионов и их потенциал к имплантации.
Известно, что одной из основных причин неудач имплантации может быть наличие хромосомной патологии у переносимых эмбрионов [7]. И хотя перенос эуплоидного эмбриона не является гарантией наступления беременности, он существенно повышает ее шансы, вплоть до 70–75% [8]. В связи с этим в последнее время в широкую практику входит применение молекулярных цитогенетических методов, которые позволяют оценить сбалансированность генома, например метод сравнительной геномной гибридизации (aCGH). Однако недостатком данного метода является высокая стоимость исследования, невозможность осуществить диагностику вследствие малого количества материала, риск повреждения эмбриона при биопсии бластомера или клеток трофоэктодермы, вероятность мозаицизма, а также невозможность исключить сбалансированные хромосомные аберрации и точечные мутации генов [9]. К неинвазивным методам оценки качества эмбрионов относят непрерывное наблюдение за их развитием (time-lapse embryo selection), а также протеомный анализ сред культивирования эмбрионов [10, 11]. Дальнейшее развитие малоинвазивных объективных методов оценки качества ооцитов и эмбрионов, позволяющих проводить селекцию эмбрионов с высоким потенциалом к имплантации и отсутствием хромосомных аномалий является одним из наиболее важных направлений репродуктивной медицины [12].
Достаточно многообещающе выглядят исследования последнего десятилетия, демонстрирующие возможность оценки качества ооцитов и эмбрионов по состоянию окружающих его клеток, получаемых при выделении кумулюсооцитарного комплекса после пункции фолликула [13–15].
Известно, что окружающие ооцит кумулюсные клетки образуются в процессе фолликулогенеза на этапе формирования полости внутри фолликула из низко дифференцированных предшественников – клеток гранулезы [16]. Кумулюсные клетки тесно связанны с ооцитом посредством специальных щелевых контактов, позволяющих осуществлять метаболический обмен и транспорт сигнальных молекул [17]. Таким образом, кумулюсные клетки оказывают непосредственное влияние на рост и развитие ооцита, регулируя его транскрипционную активность, а также ядерное и цитоплазматическое созревание [18, 19]. Важная роль кумулюсных клеток в оогенезе заставила ученых всего мира сосредоточиться на их исследовании [12, 20].
Доказано, что уровень экспрессии потенциально значимых генов в кумулюсных клетках коррелирует с показателями качества ооцитов и эмбрионов и частотой наступления беременности [14, 15, 21–23], а также обнаружена весомая связь с хромосомными аномалиями эмбрионов при проведении предимплантационной генетической диагностики [24]. Таким образом, оценка транскриптома кумулюсных клеток может стать новым дополнительным малоинвазивным методом прогнозирования наличия хромосомных аномалий у плода.
Цель исследования: поиск молекулярно-генетический маркеров, ассоциированных с вероятностью наличия хромосомных аномалий в эмбрионах, с целью оптимизации выбора переносимых эмбрионов для повышения эффективности программ ЭКО.
Материал и методы исследования
На базе отделения вспомогательных технологий в лечении бесплодия и лаборатории молекулярно-генетических методов ФГБУ Научный центр акушерства, гинекологии и перинатологии им. академика В.И. Кулакова Минздрава России проведено ретроспективное исследование случай-контроль.
 В кумулюсных клетках методом полимеразной цепной реакции с обратной транскрипцией в режиме реального времени был исследован уровень экспрессии мРНК 10 генов: генов внеклеточного матрикса (гиалуронан-синтетаза 2 (HAS2), версикан (VCAN), молекула клеточной адгезии активированных лейкоцитов (ALCAM или CD166)), генов, регулирующих передачу внутриклеточной информации (простагландин синтетаза 2 (PTGS2), гремлин (GREM1), инозитол-трифосфат 3 киназа А (ITPKA), синдекан 4 (SDC4), кальмодулин (CALM2)), а также гена, регулирующего убиквитинирование (супрессор цитокиновой сигнализации, содержащий SPRY-домен (SPSB2)) и гена опухолевого протеина (TP53I3) (реактивы ДНК-Технология, Россия).
В кумулюсных клетках методом полимеразной цепной реакции с обратной транскрипцией в режиме реального времени был исследован уровень экспрессии мРНК 10 генов: генов внеклеточного матрикса (гиалуронан-синтетаза 2 (HAS2), версикан (VCAN), молекула клеточной адгезии активированных лейкоцитов (ALCAM или CD166)), генов, регулирующих передачу внутриклеточной информации (простагландин синтетаза 2 (PTGS2), гремлин (GREM1), инозитол-трифосфат 3 киназа А (ITPKA), синдекан 4 (SDC4), кальмодулин (CALM2)), а также гена, регулирующего убиквитинирование (супрессор цитокиновой сигнализации, содержащий SPRY-домен (SPSB2)) и гена опухолевого протеина (TP53I3) (реактивы ДНК-Технология, Россия).
Во избежание деградации РНК взятие материала (кумулюсные клетки) осуществляли в пробирки с раствором гуанидинтиоционата (лизирующий раствор наборы «Проба НК»). Осаждение РНК проводили изопропанолом в присутствии соосадителя, с последующими отмывками промывочными растворами. В реакции обратной транскрипции использовали смесь специфических олигонуклеотидов всех исследуемых генов. Амплификацию осуществляли в режиме реального времени с измерением уровня флуоресценции по каналу FAM на каждом цикле при температуре отжига праймеров. Реализация «горячего старта» обеспечивалась использованием Taq-полимеразы, активность которой блокировалась антителами и восстанавливалась при прогреве. Реакцию ставили в двух повторах для каждой точки. Уровень экспрессии измеряли в условных единицах относительно референсных генов TBP, B2M, GUSB методом сравнения пороговых циклов (∆Cq) .
В исследование было включено 42 образца кумулюсных клеток, полученных от 11 пациенток, соответствовавших критериям включения (возраст 18–36 лет, женское бесплодие трубного происхождения, мужской фактор бесплодия при отсутствии тяжелой патозооспермии, регулярный менструальный цикл, проведение интрацитоплазматической инъекции сперматозоида в ооцит (ИКСИ)). Критериями исключения явились эндокринный фактор бесплодия, эндометриоз III–IV степени распространения, пороки развития половых органов и другие. Стимуляция суперовуляции проводилась препаратами гонадотропинов по протоколу с антагонистом гонадотропин-рилизинг гормона со 2–3-го дня менструального цикла.
Морфологическая оценка качества эмбрионов была произведена согласно классификации ESHRE от 2009 г., принятой Istanbul consensus workshop on embryo assessment («модифицированная» классификация D. Gardner) [25].
Сравнительная геномная гибридизация генетического материала эмбриона проводилась с использованием оборудования фирмы Agilent (США). Полногеномную амплификацию ДНК исследуемых клеток проводили с помощью набора для проведения WGA-PCR PicoPlex SingleCell WGA Kit (Rubicon Genomics, США) и набора для проведения MDA GenetiSure Pre-Screen Amplification and Labeling Kit (Agilent, США). Качество и количество полученной в ходе амплификации ДНК контролировали с помощью 1,2% агарозного электрофореза. Мечение ампликонов проводили с помощью набора SureTag DNA labeling Kit Agilent (США) согласно прилагаемой инструкции. Меченые ампликоны наносили на биочип Sure Print G3 8x60 aCGH Agilent (США), гибридизировали 16 часов, после чего проводили отмывку и сканирование на сканере биологических чипов SureScan Microarray Scanner. Интерпретацию полученных результатов проводили с помощью программного продукта Agilent CytoGenomics.
Все эмбрионы были разделены на 4 группы в зависимости от наличия в них хромосомных аномалий. I группа – эмбрионы без хромосомных аномалий (20 образцов), II группа – эмбрионы с анеуплоидиями по половым хромосомам (3 образца), III группа – эмбрионы с анеуплоидиями по соматическим хромосомам (15 образцов), IV группа – гетероплоидные эмбрионы (4 образца).
Также с целью выявления взаимосвязи уровня экспрессии мРНК генов и показателей качества эмбрионов, эмбрионы были разделены на 3 группы в зависимости от качества эмбрионов согласно морфологическим критериям оценки: I группа – эмбрионы хорошего качества (16 образцов), II группа – эмбрионы удовлетворительного качества (12 образцов), III группа – эмбрионы не удовлетворительного качества (14 образцов).
Исследование было одобрено комиссией по этике биомедицинских исследований ФГБУ НЦАГиП им. В.И. Кулакова Минздрава России. Статистическая обработка данных выполнена при помощи пакета прикладных программ SPSS Statistics 22.0. Для выявления прогностического маркера наличия хромосомных аномалий применялся дискриминантный анализ (при разделении эмбрионов на 2 группы в зависимости от наличия хромосомных аномалий в эмбрионах: I группа – эмбрионы без хромосомных аномалий (20 образцов), II группа – эмбрионы с хромосомными аномалиями (22 образца).
Для оценки характера распределения количественных данных предварительно проводился тест Шапиро–Уилка. Поскольку в большинстве случаев распределение данных было отлично от нормального, использовались методы непараметрической статистики.
В качестве меры центральной тенденции количественных признаков была выбрана медиана (Me), а в качестве интервальной оценки – верхний (H) и нижний квартили (L). Результаты представлены в виде Me (L-H).
В случае исследования нескольких независимых выборок использовали непараметрический тест Крускала–Уоллиса, при двух выборках – критерий Манна–Уитни для несвязанных совокупностей. Достоверность различий в частоте встречаемости качественных признаков определяли по критерию χ2. Статистически значимыми считались различия при р<0,05. Отношение шансов (ОШ) приведено с 95% доверительным интервалом.
Результаты исследования
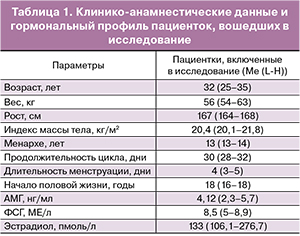
Средний возраст пациенток составил 30,64±5,97 года; средняя масса тела – 57,09±4,93 кг. Клинико-анамнестические данные и гормональный профиль пациенток представлены в табл. 1.
В ходе проведенного исследования была выявлена взаимосвязь между качеством эмбрионов согласно морфологическим критериям оценки и наличием хромосомных аномалий в эмбрионах (χ2-тест, р=0,048). Согласно проведенному исследованию, в группе эмбрионов плохого качества в 78,6% случаев встречаются хромосомные аномалии (ОШ=5,7 (1,4–23,9), р=0,023).
Для выявления молекулярно-генетических маркеров, ассоциированных с вероятностью наличия хромосомных аномалий в эмбрионах, нами был проведен дискриминантный анализ. По данным проведенного исследования уровень экспрессии мРНК гена CALM2 может являться единственным независимым маркером наличия хромосомных аномалий в эмбрионах в программах ЭКО. Доля дисперсии, объясненной данной моделью, составила 60%.
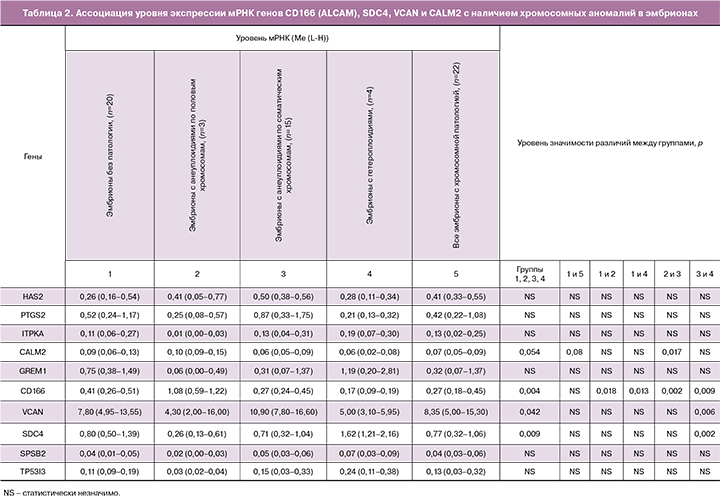
В ходе проведенного исследования была выявлена взаимосвязь между уровнем экспрессии мРНК генов СD166 (ALCAM), SDC4, VCAN и CALM2 и наличием различных хромосомных аномалий в эмбрионах (тест Крускала–Уоллиса, p=0,004, p=0,009, p=0,042, p=0,054 соответственно) (табл. 2).
При сравнении эмбрионов без патологии с эмбрионам с анеуплоидиями по половым хромосомам, а также эмбрионов без патологии с гетероплоидными эмбрионами установлена взаимосвязь уровня экспрессии мРНК гена СD166 (ALCAM) и наличия хромосомных аномалий в эмбрионах: наблюдается повышение уровня экспрессии мРНК в кумулюсных клетках эмбрионов с анеуплоидиями по половым хромосомам в 2,6 раза (тест Манна–Уитни, р=0,018) и снижение уровня экспрессии мРНК в кумулюсных клетках эмбрионов с гетероплоидиями в 2,4 раза (тест Манна–Уитни, р= 0,013) (табл. 2).
При сравнении эмбрионов с анеуплоидиями по половым хромосомам и эмбрионов с анеуплоидиями по соматическим хромосомам выявлены значимые различия между уровнем экспрессии мРНК генов СD166 (ALCAM) и CALM2 и наличием хромосомных аномалий: наблюдается повышение уровня экспрессии мРНК гена СD166 в 4 раза (тест Манна–Уитни, р=0,002) и гена CALM2 в 1,7 раза (тест Манна–Уитни, р=0,017) в кумулюсных клетках эмбрионов с анеуплоидиями по половым хромосомам (табл. 2).
В ходе проведенного исследования также была выявлена взаимосвязь уровня экспрессии мРНК генов СD166 (ALCAM), SDC4 и VCAN и наличия хромосомных аномалий в эмбрионах при сравнении эмбрионов с анеуплоидиями по соматическим хромосомам и гетероплоидных эмбрионов: наблюдается повышение уровня экспрессии мРНК гена СD166 в 1,6 раза (тест Манна–Уитни, р=0,009) и гена VCAN в 2,2 раза (тест Манна–Уитни, р=0,006) в кумулюсных клетках эмбрионов с анеуплоидиями по соматическим хромосомам. При анализе гена SDC4 наблюдается повышение уровня экспрессии мРНК в кумулюсных клетках эмбрионов с гетероплоидиями в 2,3 раза (тест Манна–Уитни, р=0,002) (табл. 2).
При сравнении эмбрионов без патологии и эмбрионов с анеуплоидиями по соматическим хромосомам, а также гетероплоидных эмбрионов с эмбрионами с анеуплоидиями по половым хромосомам, статистически значимых различий в уровне экспрессии мРНК исследуемых генов в ходе проведенного исследования обнаружено не было. Также не было выявлено статистически значимых различий между уровнем экспрессии мРНК исследуемых генов и качеством развивающихся эмбрионов согласно морфологическим критериям оценки (тест Крускала–Уоллиса, p>0,05).
Обсуждение
В попытке идентифицировать новые методы диагностики качества эмбрионов, которые могли бы использоваться отдельно или совместно с используемой в практике морфологической оценкой, ученые остановили свое внимание на альтернативных малоинвазивных методах исследования, основанных на оценке качества ооцита и/или эмбриона по уровню транскрипционной активности в кумулюсных клетках. Нами были выбраны гены, контролирующие клеточную репродукцию, передачу внутриклеточной информации, миграцию и пролиферацию клеток, ангиогенез, установление осей зародыша, программируемую гибель клеток, формирование внеклеточного матрикса, спецификацию мезодермы и, таким образом, потенциально ассоциируемые с процессами фолликулогенеза, оогенеза и с развитием эмбрионов. Известно, что HAS2 является ключевым ферментом, необходимым для синтеза кумулюсными клетками гиалуроновой кислоты, являющейся главным компонентом внеклеточного матрикса, связывающего вместе ооцит и кумулюсные клетки [26]. Гиалуроновая кислота играет важную роль в процессах овуляции, оплодотворения и в эмбриогенезе [27]. HAS2 стимулирует клеточную пролиферацию, индуцирует передачу внутриклеточной информации, а также обладает ангиогенным и иммуностимулирующим действиями [28].
Ген версикан (VCAN), относящийся к семейству протеогликанов, является одним из компонентов внеклеточного матрикса [29]. Он вовлечен в процесс клеточной адгезии, а также принимает участие в пролиферации и миграции клеток, ангиогенезе, апоптозе и играет ключевую роль в формировании структуры тканей и стабилизации белков внеклеточного матрикса [30].
Ген простагландин-синтетаза 2 (PTGS2) играет важную роль в реализации репродуктивной функции, принимая участие в процессах овуляции, оплодотворения, имплантации и родах [31]. Экспрессия PTGS2 регулируется ооцит-секретируемым паракринным фактором роста и дифференцировки – 9 (GDF9 – growth differentiation factor), и наряду с HAS2 принимает участие в передаче внутриклеточной информации и формировании внеклеточного матрикса [13, 15, 21].
Ген гремлин (GREM1) – антагонист костного морфогенетического белка, является GDF9-зависимым геном [32]. Считается, что гремлин осуществляет регуляцию функции кумулюсных клеток через ооцит-секретируемые факторы (GDF9 и BMP15) за счет селективного ингибирования экспрессии костного морфогенетического белка, но не фактора GDF9 [14, 32]. Являясь селективным ингибитором BMP15, гремлин предотвращает преждевременную лютеинизацию клеток гранулезы [32].
Следует отметить, что в нашем исследовании не было получено статистически значимых данных об ассоциации мРНК генов HAS2, VCAN, PTGS2 и GREM1 с вероятностью наличия хромосомных аномалий в эмбрионах.
Ген синдекан 4 (риудокан) (SDC4) кодирует белок, являющийся трансмембранным гепарансульфатным протеогликаном, который функционирует в качестве рецептора для передачи внутриклеточной информации. Он также ингибирует апоптоз клеток, опосредованный фактором некроза опухоли [33].
Синдеканы взаимодействуют с различными эффекторными молекулами, в том числе с факторами роста, компонентами внеклеточного матрикса, другими поверхностными молекулами и белками, принимающими участие в регуляции свертываемости крови и формировании межклеточного матрикса [34]. Известно, что синдекан 4 может выполнять несколько биологических функций, включая модуляцию ангиогенеза, пролиферацию клеток и повышение антикоагуляционной активности; он также вовлечен в процесс созревания фолликулов и играет важную роль в процессе овуляции [35]. По результатам проведенного нами исследования выявлена взаимосвязь между уровнем экспрессии мРНК гена SDC4 и наличием хромосомных аномалий в эмбрионах при сравнении эмбрионов с анеуплоидиями по соматическим хромосомам и гетероплоидных эмбрионов: наблюдается повышение уровня экспрессии мРНК в кумулюсных клетках эмбрионов с гетероплоидиями в 2,3 раза.
Инозитол-1,4,5-трифосфат-3-киназа – это ключевой фермент, регулирующий метаболизм инозитол полифосфатов, ответственных за передачу внутриклеточных сигналов. Он активирует ряд процессов, приводящих к открытию мембранных каналов и высвобождению кальция в цитозоль по градиенту концентрации [36]. Кальций необходим для функционирования клеточных мембран, а также для работы ядерного аппарата клетки [37]. Кальций является вторичным мессенджером, регулирующим ряд клеточных процессов, включающих пролиферацию и миграцию клеток, апоптоз, а также экспрессию генов [38]. Кальций зачастую действует как посредник только после взаимодействия с кальмодулином (CALM2), содержащимся в цитозоле. Кальмодулин является растворимым цитозольным белком, состоящий из двух доменов, каждый из которых содержит 2 центра связывания кальция [39]. При повышении концентрации кальция он активно присоединяется к кальмодулину, образуя комплекс 4Са2+-кальмодулин. Этот комплекс взаимодействует с Са2+-кальмодулин-зависимыми протеинкиназами, которые, в свою очередь, активируются [40]. Комплекс Са2+-кальмодулин способен активировать также Са2+АТФазы, НАД-киназы, НАД-оксидоредуктазы, липазы [39]. Активированная Са2+-кальмодулин-зависимая протеинкиназа фосфорилирует определенные белки и ферменты цитозоля клетки, в результате чего изменяется их активность и скорость метаболических процессов, в которых они участвуют [40].
По данным проведенного нами исследования именно уровень экспрессии мРНК гена CALM2 является наиболее информативным маркером наличия хромосомных аномалий в эмбрионах в программах ЭКО.
Молекула клеточной адгезии активированных лейкоцитов (ALCAM), также известная как CD 166 (кластер дифференцировки 166) – это мембранный белок, участвующий в связывании клеток между собой и с внеклеточным матриксом [41]. Данный белок экспрессируется в клетках эндометрия и бластоцистах, а также в кумулюсных и гранулезных клетках в период овуляции [42]. Известно, что ALCAM участвует в привлечении и миграции лейкоцитов в очаг воспаления и повреждения тканей, способствуя трансэндотелиальной миграции, включающей ряд четко скоординированных взаимодействий между воспаленным эндотелием и активированными лейкоцитами [43]. Считается, что процессы овуляции и имплантации активируют в организме процессы, аналогичные ответу на воспаление, и сопровождаются повышением проницаемости сосудов эндометрия в месте имплантации бластоцисты [44]. Таким образом, предполагают, что ALCAM принимает участие в процессах овуляции и имплантации.
По результатам проведенного нами исследования была выявлена взаимосвязь уровня экспрессии мРНК гена СD166 (ALCAM) и наличия хромосомных аномалий в эмбрионах при сравнении эмбрионов без патологии с эмбрионами с гетероплоидиями и анеуплоидиями по половым хромосомам. При этом наблюдается уменьшение в 2,4 раза уровня экспрессии мРНК в кумулюсных клетках эмбрионов с гетероплоидиями и повышение в 2,6 раза в кумулюсных клетках эмбрионов с анеуплоидиями по половым хромосомам по сравнению с нормой. Это позволяет предположить, что изменение уровня экспрессии мРНК гена ALCAM в ту или иную сторону свидетельствует о нарушении связывания клеток между собой и внеклеточным матриксом, что приводит к нарушению метаболического обмена и транспорта сигнальных молекул в ооцит, а также негативно отражается на его ядерном и цитоплазматическом созревании. Это подтверждает тот факт, что для нормального развития ооцита и эмбриона необходима тесная взаимосвязь между ооцитом и окружающими его соматическими клетками. Принимая во внимание важную роль данного маркера в процессе имплантации, можно предположить, что ген ALCAM не столь важен в предсказании наличия хромосомных аномалий в эмбрионе, сколь может являться маркером, определяющим его потенциал к имплантации.
Несмотря на то что уровень экспрессии гена ALCAM был существенно ниже при наличии гетероплоидий в эмбрионах и существенно выше в эмбрионах с анеуплоидиями по половым хромосомам по сравнению с нормой, по данным проведенного дискриминантного анализа уровень экспрессии мРНК гена ALCAM не является маркером наличия хромосомных аномалий в эмбрионах. Это можно объяснить небольшой выборкой эмбрионов, а также разнонаправленностью показателей экспрессии гена при различной хромосомной патологии. Таким образом, дальнейшие исследования, нацеленные на поиск новых биомаркеров наличия хромосомных аномалий в эмбрионах, необходимо проводить на более большой выборке эмбрионов, где также было бы возможно оценить их потенциал к имплантации.
По данным литературы к настоящему времени не проводилось исследований, оценивающих наличие ассоциации между уровнем экспрессии мРНК вышеописанных генов и наличием хромосомных аномалий в эмбрионах, однако имеется множество исследований, продемонстрировавших весомую связь с качеством эмбрионов согласно морфологическим критериям оценки. McKenzie и соавт. в своем исследовании показали, что уровень экспрессии мРНК генов PTGS2 и HAS2 был в 6 раз выше, а уровень экспрессии GREM1 в 15 раз выше в кумулюсных клетках ооцитов, развившихся до эмбрионов хорошего качества на 3-и сутки культивирования по сравнению с эмбрионами низкого качества [15]. В исследовании S. Wathlet и соавт. также была продемонстрирована значимая взаимосвязь генов PTGS2, CALM2, SDC4, ALCAM, GREM1 и ITPKA с морфологическими показателями оценки качества эмбрионов на 3-и и на 5-е сутки развития [21].
По данным проведенного нами исследования не было выявлено статистически значимых различий между уровнем экспрессии мРНК исследуемых генов и качеством развивающихся эмбрионов. Однако была выявлена взаимосвязь между качеством эмбрионов согласно морфологическим критериям оценки и наличием хромосомных аномалий в эмбрионах: в группе эмбрионов плохого качества в 78,6% случаев встречаются хромосомные аномалии. Таким образом, можно предположить, что наличие или отсутствие хромосомных аномалий определяет дальнейшее качество развивающихся эмбрионов согласно морфологической оценке.
Ген TP53I3 кодирует подсемейство белков, схожих с оксиредуктазами, которые участвуют в клеточных реакциях на окислительный стресс [45]. Этот ген индуцируется супрессором опухоли р53, принимает непосредственное участие в ответе на повреждение ДНК и, как полагают, участвует в p53-опосредованной гибели клеток [46]. Таким образом, снижение экспрессии мРНК гена TP53I3 может приводить к снижению реакции на повреждение ДНК, тем самым вызывая нарушение различных процессов, в том числе и апоптоза. Последнее, в свою очередь, приводит к сохранению кумулюсных клеток, не способных осуществлять свою основную функцию: метаболический обмен и транспорт сигнальных молекул, что приводит к нарушению созревания ооцита [24].
В 2012 г. Е. Fragouli и соавт. провели исследование с целью определения генов, уровень экспрессии которых коррелировал бы с наличием анеуплоидий у эмбриона. Ученые проанализировали экспрессию 96 генов и обнаружили, что уровни экспрессии мРНК генов SPSB2 и опухолевого протеина (TP53I3) были значительно ниже в кумулюсных клетках ооцитов с хромосомными аномалиями [24]. Известно, что SPSB2 регулирует убиквитинирование синтазы оксида азота, способствуя ее протеосомальной деградации [47]. Таким образом, снижение уровня экспресии мРНК гена SPSB2 в кумулюсных клетках приводит к повышению активности синтазы оксида азота, что за счет накопления оксида азота способствует избыточному образованию активных форм кислорода, оказывающих цитотоксическое воздействие на ооцит и окружающие его кумулюсные клетки [24].
Однако по результатам нашего исследования статистически значимых различий между уровнем экспрессии мРНК генов SPSB2 и TP53I3 и наличием хромосомных аномалий в эмбрионах выявлено не было.
Заключение
В группе эмбрионов плохого качества чаще встречаются хромосомные аномалии по сравнению с эмбрионами хорошего и удовлетворительного качества. Уровень экспрессии мРНК гена CALM2 является наиболее информативным маркером наличия хромосомных аномалий в эмбрионах в программах ЭКО среди списка исследуемых нами генов, однако его предсказательная способность недостаточно высока для клинического применения. Таким образом, необходимо дальнейшее изучение профиля экспрессии генов для поиска потенциальных биомаркеров в кумулюсных клетках с целью построения прогностической модели, предсказывающей наличие хромосомных аномалий в эмбрионах. Данная математическая модель позволит в дальнейшем оптимизировать выбор переносимых эмбрионов и тем самым повысить результативность программ ЭКО.



