Несмотря на широкое применение и развитие современных научных достижений в программах вспомогательных репродуктивных технологий (ВРТ), эффективность лечения бесплодия методом экстракорпорального оплодотворения (ЭКО) остается ограниченной и не превышает 30–40% [1]. При проведении программ ВРТ примерно у 15% перспективных в отношении наступления беременности супружеских пар отмечаются низкая частота оплодотворения ооцитов, арест эмбрионов на разных этапах дробления и получение эмбрионов неудовлетворительного качества [2]. Более того, у 70% супружеских пар при переносе эмбриона, соответствующего хорошему/отличному качеству согласно морфологическим критериям оценки, беременность не наступает при удовлетворительных показателях эндометрия в день переноса. Учитывая, что при переносе эуплоидного эмбриона частота беременности в программах ВРТ в значительной степени возрастает, в структуре наиболее частых причин повторных неудач имплантации следует выделить качество самого эмбриона [3]. В связи с этим наиболее перспективные научные исследования в области ВРТ сконцентрированы на разработке стратегии по улучшению качества гамет, а также условий культивирования эмбриона. Кроме этого, актуальным представляется изучение неинвазивных или малоинвазивных предикторов качества гамет, позволяющих прогнозировать не только качество получаемого эмбриона до начала овариальной стимуляции, но и эффективность лечения бесплодия методом ВРТ [4].
Известно, что на развитие ооцитов, оплодотворение и раннее дробление эмбриона влияет состав фолликулярной жидкости (ФЖ), который обеспечивает микроокружение, содержащее множество питательных веществ. ФЖ содержит микроэлементы и молекулы, окружающие и питающие ооцит, а также постоянно реагирующие на изменения, происходящие в интрафолликулярной среде [5]. Состав ФЖ влияет не только на созревание ооцитов, но и активирует ядерное и цитоплазматическое ооцитарное созревание, обеспечивает ооцит энергией для возобновления мейотического созревания, необходимого для формирования пронуклеусов после оплодотворения и дальнейшего потенциала к развитию [6]. С другой стороны, ооцит в созревающем фолликуле также секретирует различные факторы роста, обеспечивая постоянный баланс состава ФЖ. Одними из молекул, принимающими активное участие в обеспечении клеток источником энергии, а также участвующими в формировании основного структурного компонента плазматических мембран, сигнальных молекул и регуляторов белков, являются липиды. Было показано, что липопротеиды высокой плотности в ФЖ могут выполнять защитную роль, а также уменьшать фрагментацию ооцитов [7]. В настоящее время проведены исследования липидного профиля ФЖ при различных видах протоколов стимуляции [8, 9]. Результаты исследований показали, что определенный липидный состав положительно коррелирует с имплантацией эмбриона в программах ВРТ [6, 10]. Кроме этого, в литературе описаны изменения липидного состава ФЖ при эндометриозе [11], синдроме поликистозных яичников [12] и у пациенток старшего репродуктивного возраста [5, 13]. Изучение липидного профиля ФЖ в качестве дополнительного маркера оценки качества ооцитов представляется крайне перспективным и позволяет определить причину низкой частоты оплодотворения и получения эмбриона неудовлетворительного качества в программах ВРТ у пациенток с множественными неудачными попытками ЭКО в анамнезе. Особый интерес представляют исследования по прогнозированию качества ооцита до проведения программ овариальной стимуляции при помощи изучения липидного профиля плазмы крови. Núnez Calonge R. et al. показали, что липидный профиль крови может отражать липидный состав ФЖ и выступать маркером овариального ответа на стимуляцию [14].
Исследования всего набора липидов в тканях и плазме крови очень ограничены. Скрининг целого класса веществ, в том числе липидов, является основной прерогативой метода масс-спектрометрии. Учитывая, что разработка тест-системы по прогнозированию качества ооцитов, полученных во время овариальной стимуляции, при помощи изучения липидного профиля плазмы крови является крайне перспективной и актуальной задачей, цель данного исследования заключалась в анализе липидного профиля плазмы крови в зависимости от липидома ФЖ и определении потенциальных групп липидов, которые могут коррелировать с качеством ооцита.
Материалы и методы
В исследование были включены 40 супружеских пар в возрасте от 24 до 39 лет и с нормальным индексом массы тела (до 25 кг/м2), обратившихся за лечением бесплодия методом ВРТ в отделение вспомогательных технологий в лечении бесплодия им. проф. Б.В. Леонова. От каждой пары было получено письменное добровольное информированное согласие на участие в данном исследовании и обработку персональных данных. Критериями включения в исследование явились: бесплодие, обусловленное трубно-перитонеальным фактором, мужским фактором (без выраженной патозооспермии), а также сохраненный овариальный резерв. Критериями исключения послужили: аномалии строения матки, аномалии кариотипа, использование донорских ооцитов или сперматозоидов, ожирение II–III степени, тяжелые формы мужского бесплодия, а также наследственная гиперхолестеринемия.
Пациенткам, включенным в исследование, была проведена овариальная стимуляция по протоколу с антагонистом гонадотропин-рилизинг-гормона со 2-го или 3-го дня менструального цикла. По достижении диаметра фолликулов не менее 17 мм пациенткам был назначен триггер финального созревания ооцитов – препарат хорионического гонадотропина. Через 35–36 ч после введения триггера овуляции была проведена трансвагинальная пункция (ТВП) яичников с последующим забором ооцитов и оценкой их качества. Оплодотворение полученных ооцитов было выполнено методом ЭКО или интрацитоплазматической инъекции сперматозоида в ооцит (ИКСИ). Все этапы культивирования проводили в мультигазовых инкубаторах СООК (Ирландия) в каплях по 25 мкл под маслом (Irvine Sc., USA) на базе отделения вспомогательных технологий в лечении бесплодия им. проф. Б.В. Леонова. У пациенток, включенных в исследование, в день ТВП был произведен забор плазмы крови натощак перед проведением анестезиологического пособия. Аспирацию ФЖ производили под отрицательным давлением 140–150 мм водного столба в заранее подогретые стерильные пробирки, которые передавали эмбриологу.
Перед проведением анализа липидного спектра ФЖ, полученная из обоих яичников, а также плазма крови были обработаны и сохранены в коллекции Биобанка ФГБУ «НМИЦ АГП им. академика В.И. Кулакова» Минздрава России.
Экстракты липидов получали в соответствии с модифицированным методом Фолча. К 40 мкл образца добавляли 480 мкл раствора хлороформ-метанол (2:1, об./об.), смесь инкубировали в течение 10 минут, тщательно перемешивая. В полученный раствор добавляли воду. Смесь центрифугировали при 13 000 G в течение 10 минут при температуре окружающей среды. Отбирали 150 мкл органического нижнего слоя, содержащего липиды, в оставшуюся смесь добавляли 250 мкл раствора хлороформ-метанол (2:1, об./об.), повторно перемешивали, центрифугировали при 13 000 G в течение 10 минут и отбирали еще 300 мкл нижнего слоя. Органическую фазу высушивали в потоке азота, затем растворяли в 200 мкл смеси ацетонитрил-2-пропанол (1:1, об./об.) для последующего анализа.
Определение молекулярного состава образцов проводили с помощью хромато-масс-спектрометрии на жидкостном хроматографе Dionex UltiMate 3000 (Thermo Scientific, Германия), соединенном с масс-анализатором Maxis Impact qTOF с источником электро-распылительной ионизации (Bruker Daltonics, Германия). Разделение образцов осуществлялось методом обращенно-фазовой хроматографии на колонке Zorbax C18 (150×2,1 мм, 5 мкм, Agilent, США) с градиентом от 15 до 45% элюента B в течение 2 минут, а затем от 45 до 99% в течение 15 минут. В качестве элюента А использовали раствор ацетонитрил/вода (60/40, об./об.) с добавлением 0,1% муравьиной кислоты и 10 ммоль/л формиата аммония. Элюент В представлял собой раствор ацетонитрил/изопропанол/вода (90/8/2 об./об./об.) с добавлением 0,1% муравьиной кислоты и 10 ммоль/л формиата аммония. Скорость потока элюирования была 35 мкл/мин, объем инжектируемого образца – 0,5 мкл. Масс-спектры получали в режиме положительных ионов в диапазоне m/z 100–1700 со следующими установками: напряжение на капилляре 4,1 кВ, давление распыляющего газа 0,7 бар, скорость потока осушающего газа 6 л/мин, температура осушающего газа 200°C. Для идентификации липидов выполняли тандемную масс-спектрометрию в режиме зависимого сканирования с шириной окна 5 Да.
Для предварительной обработки хромато-масс-спектрометрических данных использовали программы msConvert из Proteowizard 3.0.9987 и MzMine. С помощью msConvert преобразовали исходные файлы в MzXml-формат, содержащий информацию о масс-спектре в любой момент времени, и ms2-формат, содержащий информацию о спектре фрагментации иона в заданный момент времени. MzMine использовали для выделения пиков, нормирования на полный ионный ток и создания таблицы, содержащей информацию о пике: массе иона, площади пика и времени выхода. Идентификация липидов производилась средствами скриптов LipidMatch [11]. Номенклатура липидов соответствует LipidMaps [12].
Статистический анализ
Статистическую обработку экспериментальных данных проводили с помощью скриптов, написанных на языке R [R Core Team (2018). R: A language and environment for statistical computing. R Foundation for Statistical Computing, Vienna, Austria. URL https://www.R-project.org/] в RStudio [RStudio Team (2016). RStudio: Integrated Development for R. RStudio, Inc., Boston, MA URL http://www.rstudio.com/].
Содержание липидов в образце оценивали полуколичественно по относительному уровню аналита, который рассчитывали делением площади хроматографического пика соответствующего аналита на суммарную площадь пиков аналитов в данном образце.
Перед статистической обработкой уровни липидов подверглись преобразованию так, чтобы среднее значение было равным 0, стандартное отклонение было равным 1, для лучшего графического представления анализируемых данных. Формула преобразования:
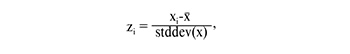
где zi – стандартизованное значение параметра, xi – исходное значение параметра, x− – среднее значение параметра, stddev(x) – стандартное отклонение совокупности.
Сравнение уровней липидов между группами проводилось с помощью рангового анализа вариаций по Краскелу–Уоллису. Для выявленных статистически значимых различий проводили попарное сравнение групп с помощью критерия Манна–Уитни с поправкой Бонферрони. Для оценки корреляционной зависимости применяли непараметрический корреляционный анализ Спирмена. Величину порогового уровня значимости p принимали равной 0,05.
Результаты
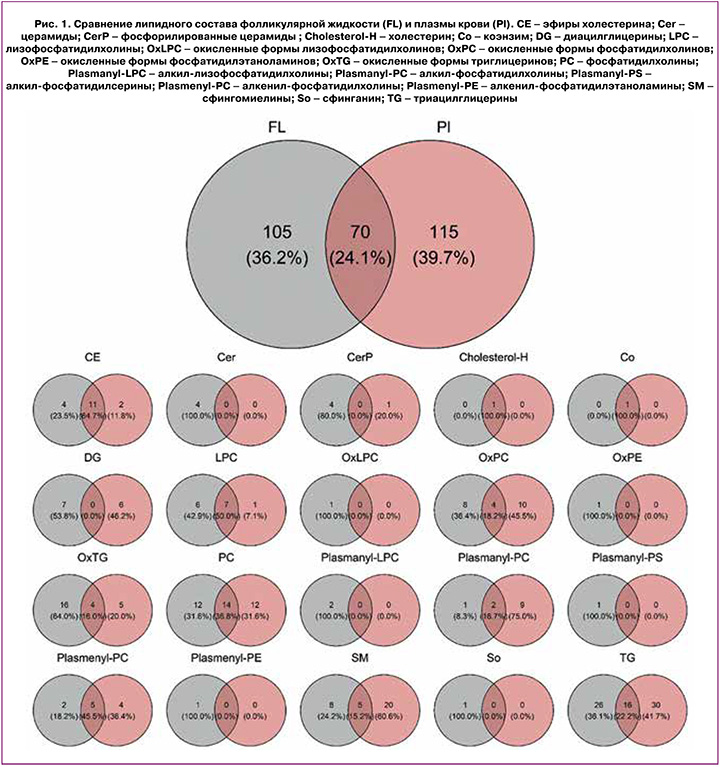
В результате анализа липидома было идентифицировано 175 липидов в образцах ФЖ и 185 липидов в образцах плазмы крови, относящихся к 20 классам. Из всех идентифицированных липидов 70 входили в состав как ФЖ, так и плазмы крови (рис. 1). Наибольшее количество общих липидов относится к классам холестериновых эфиров (CE), лизофосфатидилхолинов (LPC), фосфатидилхолинов (PC), сфингомиелинов (SM) и триацилглицеринов (TG).
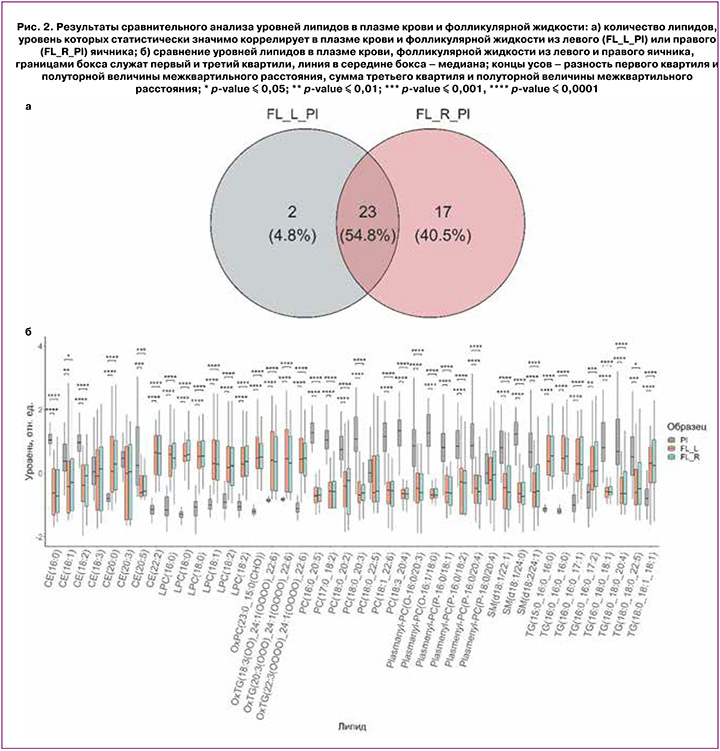
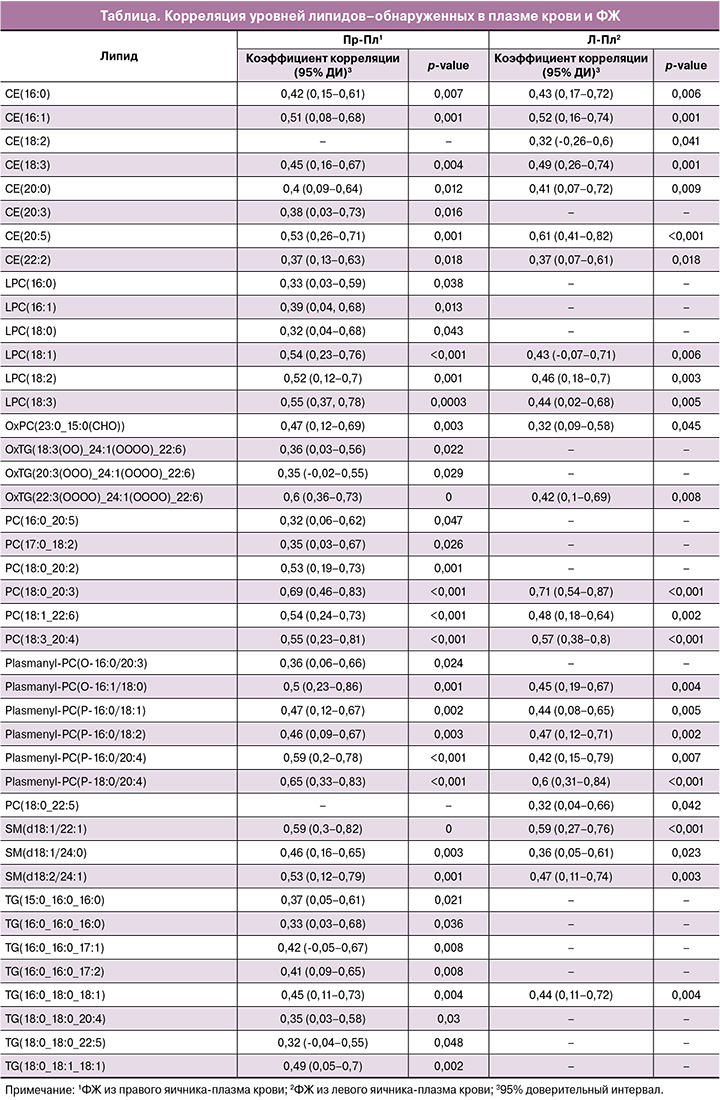
При анализе корреляции уровней липидов в плазме крови и ФЖ из левого и правого яичников было выявлено 25 липидов, уровни которых в плазме статистически значимо коррелируют с уровнями в ФЖ из левого яичника, и 40 липидов – со значимой корреляцией плазма-ФЖ из правого яичника (рис. 2а, таблица). Корреляция уровней между ФЖ из левого и правого яичников всех 175 идентифицированных липидов была статистически значимой. На рисунке 2б приведен результат сравнения уровней липидов, коррелирующих между плазмой крови и ФЖ. По результатам анализа с помощью метода Краскела–Уоллиса выявлены статистически значимые отличия для всех приведенных на рисунке 2а липидов, кроме CE(18:3), CE(20:3), PC(18:0_22:5) и Plasmenyl-PC(P-18:0/20:4). Дальнейшее попарное сравнение групп образцов методом Манна–Уитни с поправкой Бонферрони показало отсутствие статистически значимых отличий между уровнями липидов в ФЖ из левого и правого яичников. В то же время уровни тех же липидов в плазме крови существенно отличаются, несмотря на значительную корреляцию.
Обсуждение
Перспективным направлением дальнейших научных исследований в области повышения эффективности программ ВРТ, а также прогнозирования результата лечения бесплодия методом ЭКО является оценка липидомного профиля различных биологических жидкостей, в том числе липидома плазмы крови и ФЖ [15]. Анализ липидного состава плазмы крови при помощи хромато-масс-спектрометрии позволил выявить группы липидов, уровни которых статистически значимо коррелируют в плазме крови и ФЖ. Дальнейшее изучение профиля данных молекул представляется крайне перспективным с точки зрения определения новых неинвазивных молекулярных маркеров прогнозирования состава ФЖ и качества ооцита до овариальной стимуляции.
Одна из групп липидов, которые были определены в крови и в ФЖ, относится к классу фосфатидилхолинов. Фосфатидилхолины являются основным видом фосфолипидов на мембранах клеток, служат важным источником внутриклеточных сигнальных молекул, а также выполняют как метаболические, так и структурные функции [16]. Гидролиз данных липидов фосфолипазой и фосфатидатфосфогидролазой приводит к образованию в клетке жирных кислот, а именно арахидоновой кислоты. При избыточной активации метаболической системы уровень жирных кислот повышается, что приводит к образованию свободных радикалов и окислительному стрессу [17]. В 2021 г. было опубликовано исследование, результаты которого показали, что повышенный профиль фосфатидилхолина приводит к избыточному накоплению арахидоновой кислоты в ФЖ у пациентов в программе ВРТ [18]. Повышение концентрации арахидоновой кислоты ведет к снижению качества эмбриона на 3-е сутки после оплодотворения за счет ухудшения качества ооцита. В исследовании был использован метод машинного обучения (алгоритм «случайный лес») для определения других метаболитов в ФЖ, оказывающих влияние на качество ооцита и эмбриона. Среди таких метаболитов выявили липиды группы сфингомиелинов. Таким образом, накопленные метаболиты выделяются из ооцитов в ФЖ, и профилирование данной биологической среды отражает их уровень в самих клетках.
Сфинголипиды являются еще одним важным компонентом биологических мембран клеток. Данная группа представляет собой большой класс биоактивных липидов, которые опосредуют или регулируют пролиферативные реакции, ингибирование роста, апоптоз, дифференцировку, старение и подвижность клеток. Опубликованные работы показали, что уровни 4 видов сфинголипидов в ФЖ положительно коррелирует с качеством ооцитов в программе ВРТ [19]. Взаимодействие сфингомиелина, холестерина и гликосфинголипида приводит к образованию рафтов плазматической мембраны, которые, в свою очередь, участвуют в передаче сигналов клетками, сортировке липидов и белков, а также в транспортировке молекул. Один из представителей сфинголипидов – церамид, служит биологически активным компонентом митохондриальной мембраны [20]. Митохондрии служат важнейшими энергопроизводящими органеллами клетки, жизненно важными для клеточных процессов. Помимо производства энергии, митохондрии содержат ферменты, которые играют роль в окислении жирных кислот, гомеостазе кальция и апоптозе. Низкое качество ооцитов и эмбрионов может быть связано с нарушением выработки энергии в цитоплазме ооцитов [21]. Экспериментальное исследование Eliyahu E. et al. показало, что после добавления в культуральную среду фермента, называемого кислой цераминидазой, который экспрессируется в кумулюсных клетках человека и ФЖ, качество эмбрионов значительно повышается, а частота живорождения увеличивается в пять раз [22]. Следовательно, возможные генетические нарушения митохондриальной ДНК, связанные с метаболизмом липидов и их ферментов, могут играть критическую роль в развитии ооцитов. Shehadeh A. et al. показали, что у пациенток в программе ВРТ изменение липидомного профиля ФЖ ассоциировано с повышением частоты клинической беременности. Частота клинической беременности статистически значимо увеличивалась у пациенток с пониженным уровнем триглицеридов плазмы крови и с повышенным содержанием мембранных липидов (фосфолипидов и сфинголипидов). Результаты данного исследования также показали, что другие группы липидов, такие как эфиры холестерина, понижались в ФЖ, полученной от пациенток с положительным исходом лечения [6].
Липиды, относящиеся к классу «холестерины и их эфиры», в первую очередь, важны для работы клеточных мембран, а также для синтеза витамина D, необходимого для репродуктивной системы человека [16]. В отношении значимости витамина D результаты недавних исследований показали противоречивые данные. Ряд исследований подтвердил, что уровень метаболитов витамина D, образующихся из производных холестерина, ассоциирован с положительными результатами программы ВРТ [23, 24]. Несмотря на то что большинство исследований продемонстрировало положительное влияние уровня витамина D на результат лечения, другие работы показали, что концентрация в ФЖ 25-гидроксивитамина D отрицательно коррелирует со способностью ооцитов к оплодотворению и последующей имплантацией эмбриона [25]. Кроме этого, было показано, что более низкие концентрации 25-гидроксивитамина D в ФЖ ассоциированы с лучшим ответом на стимуляцию яичников [26].
Таким образом, определение липидного профиля ФЖ может быть информативным и перспективным способом диагностики. Тем не менее анализ ФЖ предоставляется возможным только после проведения овариальной стимуляции и получения ооцитов в ходе ТВП. В связи с этим анализ ФЖ может быть менее целесообразным. Наиболее перспективной задачей с практической точки зрения выступает прогнозирование липидного профиля ФЖ у пациенток, обратившихся за лечением бесплодия методом ВРТ, при помощи анализа плазмы крови на этапе до начала стимуляции. Для создания тест-системы необходимо определение липидов, идентифицированных в обоих биологических образцах (в ФЖ и в сыворотке крови). В исследовании Núñez Calonge R. et al. были получены результаты для 7 групп липидов, представленных в ФЖ, которые могут быть определены и в сыворотке крови при помощи масс-спектрометрии [14]. С использованием многомерной модели линейной регрессии для исключения влияния возраста и индекса массы тела было показано, что липидный профиль в ФЖ и сыворотке крови оказывает существенное влияние на овариальный ответ и количество зрелых ооцитов.
Стоит обратить внимание на результаты исследования, проведенного в 2021 г. Kermack A.J. et al. Полученные данные показали, что при модификации диеты перед проведением лечебного цикла ЭКО качество ооцитов значительно повышается. Диета включала в себя дополнительное назначение полиненасыщенных жирных кислот, омега-3, оливкового масла и витамина D у 55 супружеских пар за 6 недель до начала овариальной стимуляции. У супружеских пар также были собраны образцы сыворотки крови до и после лечения, а в день ТВП получена ФЖ из обоих яичников. В контрольной группе была обнаружена сильная корреляция липидов сыворотки крови после лечения с профилем ФЖ и качеством полученных ооцитов. Кроме этого, диета, обогащенная полиненасыщенными жирными кислотами, была ассоциирована с более низким содержанием арахидоновой кислоты в ФЖ [27].
Учитывая наличие в литературе исследований по возможному терапевтическому влиянию на липидный состав плазмы крови и ФЖ, исследование профиля липидов позволяет дифференцированно назначать персонифицированную подготовку пациенткам перед проведением овариальной стимуляции для повышения качества ооцитов. Разработка моделей прогнозирования результативности терапии бесплодия методом ВРТ, в том числе с использованием методов машинного обучения, на основании липидомного профиля крови и ФЖ с применением хромато-масс-спектрометрии выступает еще одной актуальной и важной задачей [28, 29].
Заключение
В настоящее время в клинической практике большое количество научных исследований сконцентрировано в области интегрированного анализа «омиксных технологий», в том числе липидомных данных, геномики, протеомики и метаболомики. Полученные результаты позволяют предположить, что липидный профиль ФЖ может быть ассоциирован с профилем сыворотки крови. Определение липидного профиля крови выступает малоинвазивным и удобным маркером не только оценки качества ооцитов, но и может быть использовано как маркер эффективности лечения.
На основании полученных результатов данной исследовательской работы возможны не только индивидуализация и персонификация лечения бесплодия и подготовки к программам ВРТ, но и более глубокое понимание механизмов нарушений созревания ооцитов и причин низкой частоты фертилизации у перспективных групп пациенток.



