Заболевания шейки матки являются одной из наиболее частых патологий женской половой сферы. Именно высокий удельный вес данной нозологии в структуре гинекологической заболеваемости обуславливает актуальность данной проблемы (от 10% до 38,5% и более), а также влияние на состояние детородной функции женского организма, риск восходящей инфекции (до 69,9%) и малигнизации (до 9,1%) [1].
Несмотря на достаточно хорошую изученность данной проблемы, современные методы диагностики и лечения заболеваний шейки матки из года в год претерпевают существенные изменения и являются предметом дискуссий и обсуждений.
Измененная картина тканей шейки матки определяет место данной патологии в совокупности заболеваний женских половых органов. Огромный удельный вес среди доброкачественных заболеваний шейки матки составляют воспалительные процессы, около 92%. Воспаление цервикального канала определяется примерно в 65% случаев, около 24% составляет воспаление шейки матки в сочетании с дефектом тканей [2].
Ведущей причиной возникновения и развития воспалительных процессов в тканях шейки матки являются инфекции, передаваемые половым путем (ИППП), и условно-патогенные микроорганизмы [3]. Попадание патогенных и условно-патогенных микроорганизмов в межклеточную субстанцию слизистой оболочки шейки матки способно вызывать длительно существующие хронические воспалительные процессы как в экзо- так и в эндоцервиксе [3]. Проспективное исследование, проведенное на Косте-Рике, показало положительную связь Gardnerella vaginalis с прогрессией цервикальной интраэпителиальной неоплазии 2 степени (CIN2), продемонстрировав влияние измененного цервиковагинального микробиома на прогрессирование рака шейки матки в когорте [4].
В развитии некоторых доброкачественных заболеваний шейки матки играет роль травма шейки матки, полученная во время родов или вследствие искусственных абортов. Акушерские разрывы шейки матки в родах относятся к числу часто встречающихся форм акушерского травматизма, среди фоновых заболеваний рубцовые деформации шейки матки занимают значимое место, их частота, по мнению ряда авторов, колеблется в значительных переделах (15,3–54,9%), а у женщин репродуктивного возраста может достигать 70% [1].
Причины, способствующие разрыву шейки матки в родах, как правило, многочисленны и нередко сочетанные, среди них: роды крупным плодом, переношенная беременность, ригидность или рубцовые изменения шейки матки, а также воспалительные изменения мягких тканей родовых путей.
Неадекватное восстановление целостности шейки матки или его отсутствие после акушерской травмы приводит к формированию выраженных рубцовых деформаций, эктропиона или старых разрывов различной степени выраженности [5]. Нарушение анатомической целостности шейки матки и, соответственно, цервикального канала влечет за собой снижение барьерной функции, что создает условия для воздействия инфекционных факторов, способных привести к восходящему пути инфицирования и в последующем вызывать хроническое воспаление органов малого таза [6]. Это, в свою очередь, может привести к развитию истмико-цервикальной недостаточности.
По МКБ-10 старые разрывы шейки матки кодируют N88.1. К сожалению, на сегодняшний день отсутствует четкая терминология анатомических изменений и рубцовых деформаций шейки матки. Чаще всего клиницисты используют классификацию акушерских разрывов шейки матки (О71.3), где выделяют:
- I степень – разрыв шейки матки с 1 или 2 сторон длиной не более 2 см;
- II степень – разрыв шейки матки с 1 или 2 сторон длиной более 2 см, но на 1 см не доходит до свода влагалища;
- III степень – разрыв шейки матки с 1 или 2 сторон, доходящий до свода влагалища или переходящий на него.
Также считаем необходимым отметить, что существуют и разногласия в тактике ведения пациенток со старыми разрывами шейки матки. Это либо динамическое наблюдение, либо электроконизация шейки матки и операция Эммета. На наш взгляд, только реконструктивно-пластические операции способны восстановить не только целостность шейки матки, но и ее функциональное значение. При этом широкое использование в комплексном лечении заболеваний шейки матки антисептических и антибактериальных средств нередко влияет на нормальную микрофлору генитального тракта, вызывая или усиливая дисбиотические нарушения. Это важно учитывать при выборе средств санации перед хирургическим лечением шейки матки, а также при подборе препаратов для профилактики послеоперационных осложнений.
Цель нашего исследования – представить опыт интравагинального применения препарата «Гайномакс» в комплексной предоперационной подготовке больных с рубцовой деформацией шейки матки.
Материалы и методы
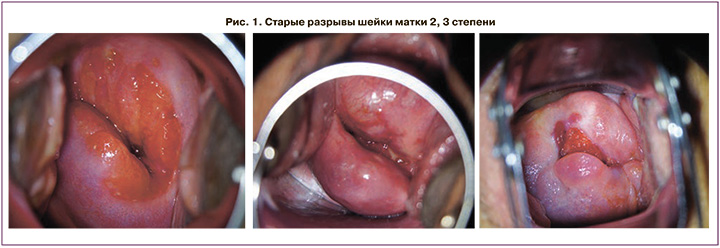
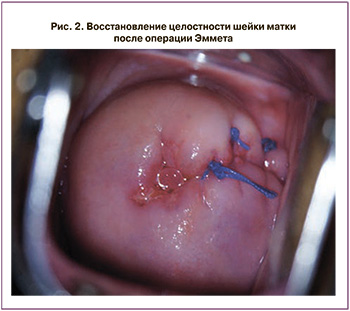 Нами обследованы 50 пациенток со старыми разрывами шейки матки, средний возраст которых составил 32,5 (5,6) года. Выраженность разрывов соответствовала 2, 3 степени (рис. 1). Все пациентки поступили на плановую реконструктивно-пластическую операцию в ООО ЛДЦ «РАЗУМЕД» (Казань) с апреля по декабрь 2019 г. Учитывая, что пациентки со старыми разрывами шейки матки находятся в группе риска по развитию воспалительных заболеваний нижнего отдела гениталий, пациенткам перед операцией, помимо стандартного микроскопического исследования влагалищного отделяемого, предложено проведение ПЦР-диагностики в режиме реального времени с тест-системами «Фемофлор 16». Получено информированное согласие женщин на проведение данного исследования. Всем пациенткам, вошедшим в исследование, выполнена операция Эммета с целью восстановления целостности шейки матки (рис. 2). Антибиотикопрофилактика проводилась цефазолином 1,0 в/в, после окончания операции шейка матки обрабатывалась 10% раствором бетадина с последующим использованием противовоспалительных влагалищных свечей в течение 7 дней.
Нами обследованы 50 пациенток со старыми разрывами шейки матки, средний возраст которых составил 32,5 (5,6) года. Выраженность разрывов соответствовала 2, 3 степени (рис. 1). Все пациентки поступили на плановую реконструктивно-пластическую операцию в ООО ЛДЦ «РАЗУМЕД» (Казань) с апреля по декабрь 2019 г. Учитывая, что пациентки со старыми разрывами шейки матки находятся в группе риска по развитию воспалительных заболеваний нижнего отдела гениталий, пациенткам перед операцией, помимо стандартного микроскопического исследования влагалищного отделяемого, предложено проведение ПЦР-диагностики в режиме реального времени с тест-системами «Фемофлор 16». Получено информированное согласие женщин на проведение данного исследования. Всем пациенткам, вошедшим в исследование, выполнена операция Эммета с целью восстановления целостности шейки матки (рис. 2). Антибиотикопрофилактика проводилась цефазолином 1,0 в/в, после окончания операции шейка матки обрабатывалась 10% раствором бетадина с последующим использованием противовоспалительных влагалищных свечей в течение 7 дней.
В качестве подготовки к плановому вмешательству у 20 пациенток с выявленными изменениями состояния микрофлоры во влагалище использовали короткую схему применения комбинации тиоконазола и тинидазола по 1 суппозиторию 2 раза в день интравагинально (утром и на ночь) в течение 3 дней
Тиоконазол – синтетическое противогрибковое средство с высокой активностью в отношении дрожжеподобных и других грибов (дерматофиты). Он эффективен также и в отношении бактериальных возбудителей: Gardnerella vaginalis, Bacteroides spp., некоторых грамположительных бактерий (вкл. Staphylococcus и Streptococcus spp.). Тинидазол эффективен в отношении как протозойных возбудителей (Trichomonas vaginalis, Entamoeba histolytica и Giardia lamblia), так и большинства анаэробных бактерий (Gardnerella vaginalis, Bacteroides fragilis, Bacteroides melaninogenicus, Bacteroides spp., Clostridium spp., Eubacterium spp., Peptostreptococcus spp. и Veillonella spp.).
Результаты
При анализе сопутствующей экстрагенитальной патологии у наблюдаемых пациенток констатирован достаточно высокий инфекционный индекс. Наиболее часто (у 36 (72%) женщин) встречались хронические воспалительные заболевания органов дыхания и мочевыводящих путей, а также вирусные респираторные инфекции. У 19 (38%) женщин выявлен дисбактериоз кишечника. В структуре гинекологических заболеваний отмечена высокая частота хронических воспалительных заболеваний нижнего отдела генитального тракта (у 47 (94%) женщин) и органов малого таза (у 23 (45%) пациенток). При изучении состава микробиоты влагалища у 20/50 (60%) пациенток были выявлены следующие дисбиотические состояния: у 8/30 (26,7%) женщин – Gardnerella vaginalis 105, у 5/30 (16,7%) – Escherichia coli 105, при этом у 7/30 (23,3%) из них – дисбиоз влагалища, связанный с сочетанием нескольких микроорганизмов – Gardnerella vaginalis, Enterobacterium spp., Streptococcus spp., Klebsiella pneumoniae, Candida albicans. Также необходимо отметить, что специфические инфекции не выявлены. После трехдневного интравагинального применения комбинации тиоконазола и тинидазола отмечено восстановление нормофлоры у всех пациенток.
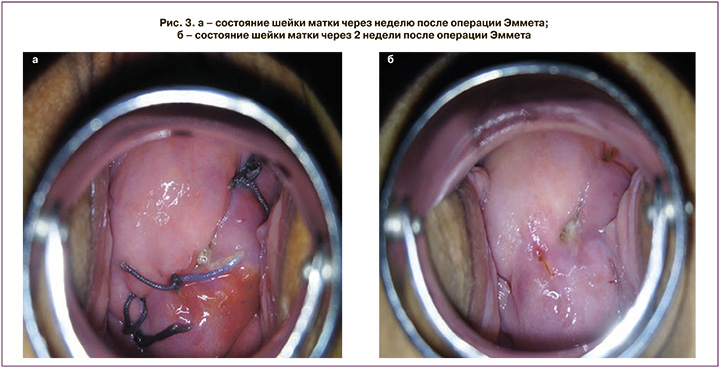
Контрольный осмотр проводился через 1 и 2 недели после оперативного лечения. При этом у всех пациенток основной группы констатирована состоятельность швов (рис. 3). Воспалительные изменения при кольпоскопическом осмотре и картина воспаления при микроскопии отделяемого из цервикального канала и влагалища отсутствовали.
Заключение
Проведенное исследование показало, что нарушение целостности шейки матки в виде старых разрывов сопровождается дисбиозом влагалища у 20/50 (40%) женщин. Поэтому считаем оправданным в предоперационной подготовке исследование микробиоты влагалища путем ПЦР-диагностики в режиме реального времени с тест-системами «Фемофлор 16» для выявления больных с дисбиозом влагалища. Этим женщинам перед оперативным вмешательством возможно трехдневное назначение интравагинально препарата «Гайномакс».



