Цистинурия – дефект реабсорбтивного транспорта цистина и двухосновных аминокислот (орнитина, аргинина и лизина) через люминальные мембраны прокисмальных канальцев почек и тонкого кишечника с частотой встречаемости 1:7000 [1]. Данное заболевание имеет, как правило, аутосомно-рецессивный тип наследования, реже – аутосомно-доминантный и сцепленный с полом [2]. На основании результатов генетических исследований выделяют три типа цистинурии: тип I (А) – обусловлен мутацией в гене SLC3A1, кодирующем тяжелую цепь rbAT почечной цистин-транспортной системы и расположенном в хромосоме 2р; тип II (В) – мутацией в гене SLC7A9 (кодирует легкую цепь b0AT); тип III (АВ) – мутацией в обоих генах [3, 4]. Подобные генетические мутации были выявлены не только у людей, но также у собак и домашних кошек. В рамках цистинурии I типа часто рассматривают синдром гипотонии-цистинурии (HCS) и синдром делеции 2p21. Если у пациентов с HCS существует мутация в генах SLC3A1 и PREPL, то при делеции 2p21 имеет место утрата двух генов – C2orf34 и PPM1B, что сопряжено с умеренной умственной отсталостью и дефицитом комплекса дыхательной цепи IV [5].
Существуют различные тестовые системы, позволяющие определить наличие мутации – MutationTaster, PolyPhen-2, Пантера, FATHMM. PhDSNP и MutPred применяются для прогнозирования вероятности развития заболевания при миссенс-мутациях. Различают две формы нарушения обмена цистина: цистинурия (избыток аминокислоты откладывается в почках, мочеточнике, мочевом пузыре) и цистиноз (цистин накапливается в почках, коже, печени, селезенке, костном мозге и лимфоузлах) [6].
 Плохая растворимость цистина в моче способствует рецидивирующему формированию коралловидных камней (рис. 1), требующих постоянных хирургических вмешательств и часто сопровождающихся рецидивирующими пиелонефритами, что обычно проявляется во второй или третьей декаде жизни [7, 8].
Плохая растворимость цистина в моче способствует рецидивирующему формированию коралловидных камней (рис. 1), требующих постоянных хирургических вмешательств и часто сопровождающихся рецидивирующими пиелонефритами, что обычно проявляется во второй или третьей декаде жизни [7, 8].
Выделяют различные генетические и биохимические механизмы развития мочекаменной болезни, в том числе в рамках ферментопатий – первичной гипероксалурии, дефицита аденин-фосфорибозил-трансферазы, недостаточности фосфорибозил-пирофосфат-синтетазы, ксантинурии, синдрома Леш-Нихана – и связанные с ними нарушения мембранного транспорта, известные как болезни Дента, семейная гипомагниемия с гиперкальциурией и нефрокальцинозом, гипофосфатемическая мочекаменная болезнь, дистальный тубулярный ацидоз, цистинурия, синдром Барттера. Существует также комплексная генная панель NGS для диагностики наследственной мочекаменной болезни [9].
Специфического лечения цистинурии в настоящее время не существует. Нефрологи рекомендуют обильный прием жидкости для снижения концентрации цистина, а также использование диеты, приводящей к защелачиванию мочи, так как при рН выше 7,5 растворимость этой аминокислоты резко повышается, однако при этом редко растворяются уже образовавшиеся камни [10]. Прием тиола снижает концентрацию цистина в моче менее 300 мг/мл.
Препарат пеницилламин при взаимодействии с цистином образует смешанный дисульфидцистеин-пеницилламин, растворимость которого намного выше, что способствует растворению цистиновых камней. Пеницилламин широко применяется для лечения цистинурии, ревматоидного артрита и склеродермии. Прием пеницилламина во время беременности – вопрос дискуссионный вследствие его способности практически полностью проникать через маточно-плацентарный барьер: имеются сообщения о формировании дефектов соединительной ткани у плодов, описаны случаи рождения детей с пороками сердца, чрезмерно растяжимой кожей и необычными чертами лица, матери которых во время беременности принимали пеницилламин [11]. По этой причине большинство нефрологов и акушеров отказываются от назначения данного препарата в период гестации.
В связи с относительной редкостью патологии, противоречивостью подходов к терапии во время беременности, возможностью развития вторичных осложнений (острый пиелонефрит, почечная недостаточность), интересным для клиницистов является описание течения беременности и исходов родов у пациенток с цистинурией.
Клиническое наблюдение
Первобеременная пациентка В., 27 лет, доставлена в родильный дом при ГБУЗ «ГКБ имени С.С. Юдина ДЗМ» бригадой скорой медицинской помощи на сроке 29–30 недель с жалобами на тянущие боли в поясничной области справа и повышение температуры тела до 37,5° С.
Из анамнеза: в возрасте 4 лет впервые развился приступ левосторонней почечной колики. При ультразвуковом исследовании обнаружен коралловидный камень в чашечно-лоханочной системе левой почки, проводилась дистанционная ударно-волновая литотрипсия – ДУВЛТ (рис. 2), а затем уретеролитотомия.
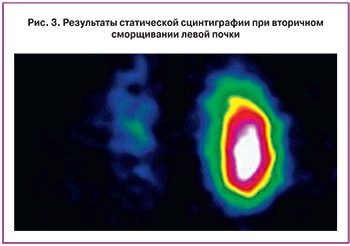 В дальнейшем в результате неоднократных хирургических вмешательств произошло вторичное сморщивание левой почки, и с 11-летнего возраста при проведении лучевой диагностики последняя не визуализировалась (рис. 3).
В дальнейшем в результате неоднократных хирургических вмешательств произошло вторичное сморщивание левой почки, и с 11-летнего возраста при проведении лучевой диагностики последняя не визуализировалась (рис. 3).
С 12-летнего возраста зафиксировано образование конкрементов в чашечно-лоханочной системе правой почки. В течение последующих трех лет трижды проводилась ДУВЛТ и трижды перкутанная нефролитолапаксия (чрескожная литотрипсия). При проведении химического анализа состава камня был обнаружен цистин. Консультирована врачом-генетиком – диагностирована врожденная цистинурия.
К 21 году в связи с рецидивирующим образованием конкрементов в правой почке, осложнявшимся многократным развитием пиелонефрита, трижды проводилась пиелонефролитотомия и неоднократно – нефростомия. Тогда же диагностирована хроническая почечная недостаточность. Назначена курсовая терапия препаратом пеницилламин, в результате которой с 24-летнего возраста при регулярном обследовании органов мочевыделительной системы регистрировалось отсутствие конкрементов.
Настоящая беременность – первая, желанная, наступила самостоятельно. С 26 недель обнаружена бессимптомная лейкоцитурия, следы белка в моче. Прибавка массы тела за первые два триместра составила 10 кг.
При ультразвуковом исследовании органов забрюшинного пространства на момент поступления была выявлена уретеропиелокаликоэктазия справа, что сопровождалось лейкоцитозом (11,2×109/л) и лейкоцитурией. Для восстановления пассажа мочи проведена эндоскопическая трансуретеральная катетеризация правой чашечно-лоханочной системы. Начата терапия уросептиками, спазмолитиками. Однако спустя сутки развился выраженный болевой синдром в правой поясничной области с повышением температуры до фебрильных цифр. Повторно осмотрена урологом – произведена чрескожная пункционная нефростомия, к лечению добавлена антимикробная терапия цефалоспоринами третьего поколения. На фоне проведенного лечения состояние пациентки стабилизировалось, произошла нормализация температуры тела, снизился уровень лейкоцитов в клиническом анализе крови (до 8,76×109/л) и в анализах мочи по Нечипоренко (с 51600 в мл до 3400 в мл). Моча выводилась посредством нефростомы. Диурез был адекватным.
Спустя месяц в процессе динамического наблюдения было выявлено уменьшение диуреза (620 мл/сут), снижение показателей клубочковой фильтрации (50,1 мл/мин), нарастание протеинурии (2,76 г/л), креатинина (149,2 ммоль/л). Учитывая прогрессирование хронической почечной недостаточности у пациентки с единственной функционирующей правой почкой, согласно заключению врачебного консилиума, от дальнейшего пролонгирования беременности решено было отказаться и родоразрешить пациентку досрочно.
На сроке 34 недели выполнено чревосечение по Джоэлу-Кохену, кесарево сечение в нижнем маточном сегменте в условиях спинальной анальгезии. В целом плодном пузыре в головном предлежании извлечен живой недоношенный мальчик массой 2160 г, ростом 44 см, с оценкой состояния новорожденных по шкале Апгар 7/7 баллов, что обусловлено морфо-функциональной незрелостью. Ребенок переведен на второй этап выхаживания на самостоятельном дыхании. В течение первой недели после родоразрешения произошла нормализация показателей клубочковой фильтрации (85,7 мл/мин), снижение протеинурии (0,3 г/л), восстановление адекватного диуреза (1270 мл/сутки). Пациентка выписана из стационара на 7-е сутки в удовлетворительном состоянии.
Обсуждение
Под определение «единственная почка» подпадает не только врожденное отсутствие почки, но также удаление или потеря функций органа в результате какого-либо заболевания (пиелонефрит, гидронефроз, мочекаменная болезнь, опухоли, травмы). Компенсаторная перестройка оставшейся почки продолжается в течение 1,5–2 лет и протекает в две стадии: 1) утрата функционального резерва с развитием объемной и функциональной гипертрофии клубочковой и канальцевой зон; 2) полная функциональная компенсация с увеличение кровотока на 30–50%. После нефрэктомии или утраты функций одной из почек беременность рекомендуют не ранее, чем через 2 года. Резервные возможности единственной почки ограничены, она чутко реагирует на различные эндо- и экзогенные воздействия, поэтому, по мнению урологов, лиц с единственной почкой нельзя считать абсолютно здоровыми [12]. В единственной почке гораздо чаще возникает пиелонефрит с нарушением депурации конечных продуктов обмена и поражением канальцевого аппарата, что представляет высочайший риск для развития перинатальной заболеваемости, а также тяжелых перипартальных осложнений [13]. При решении вопроса о возможности наступления беременности у пациенток с единственной почкой учитывается целый ряд факторов; при заболеваниях (нефролитиаз или пиелонефрит) или функциональном истощении оставшегося органа прогноз для матери и плода оказывается крайне неблагоприятным [14]. Беременность категорически противопоказана при снижении функционального резерва оставшейся почки, при наличии азотемии и артериальной гипертензии, а также при туберкулезе и пиелонефрите единственной почки [15].
Среди осложнений беременности у 13% пациенток с единственной почкой имеют место отеки и патологическая прибавка массы тела. Согласно данным литературы, у беременных с гидронефрозом одной из почек второй и третий триместры протекают на фоне угрозы преждевременных родов, лейкоцитурии, повышения С-реактивного белка, увеличения переднего и заднего диаметров почечной лоханки (MADP) – что зачастую требует проведения хирургической коррекции уродинамики [16–17].
Заключение
В настоящем клиническом наблюдении показанием для досрочного родоразрешения послужило прогрессирование хронической почечной недостаточности у пациентки с единственной функционирующей почкой. Однако, неукоснительное соблюдение регламента ведения беременных с хронической почечной недостаточностью, а также с пиелонефритом единственной почки – перманентный контроль функции оставшейся почки, восстановление уродинамики, проведение антимикробной терапии с учетом срока гестации, своевременное принятие решения о родоразрешении – дало уникальную возможность пролонгировать беременность до оптимального срока с точки зрения минимизации перинатальных осложнений.



