Венозные тромбозы, в том числе осложненные тромбоэмболией легочной артерии, представляют собой многофакторные заболевания, частота которых увеличивается с возрастом и составляет около 50 случаев на 100 000 в возрастной группе 25 лет и 120 на 100 000 в возрасте 50 лет. Тромбоэмболия легочной артерии (ТЭЛА) является основным осложнением венозных тромбозов, вызывая смерть у 1–2% пациентов [1]. В Российской Федерации частота венозных тромбозов ежегодно увеличивается на 90–100 тысяч случаев [2].
Согласно современным мета-анализам, отечественным и международным руководствам, к значимым факторам риска тромбозов относятся: возраст старше 35 лет, антифосфолипидный синдром и наследственные тромбофилии, курение, хирургические манипуляции, малоподвижный образ жизни (в том числе иммобилизация, связанная с госпитализацией), ожирение, беременность и послеродовый период, применение комбинированных оральных контрацептивов (КОК) и менопаузальной гормонотерапии [1–5].
Цель исследования: выявить основные конфаундинг факторы первичных венозных тромбозов и эмболий у женщин репродуктивного периода.
Материал и методы исследования
Для реализации поставленной цели выполнено ретроспективное когортное исследование, в которое вошли 53 женщины репродуктивного возраста, госпитализированные в лечебные учреждения г. Читы по поводу впервые возникших венозных тромбозов и эмболий, отобранные сплошным методом в рамках одного календарного года. Основные критерии включения в исследование: возраст пациенток 18–45 лет; первый в жизни эпизод венозного тромбоза; отсутствие тяжелой соматической патологии. Во всех случаях дополнительно к специфической картине заболевания и повышенному уровню D-димера, диагноз тромбоза был подтвержден ультразвуковым дуплексным ангиосканированием, ТЭЛА – электро- и эхокардиографией, рентгенографией органов грудной клетки [2].
При статистической обработке результатов использовали метод описательной статистики с определением среднего арифметического, дисперсии, cреднеквадратического отклонения (σ), расчета абсолютных (n) и относительных (%) величин. Достоверность разницы между двумя средними показателями оценивали по критерию Стьюдента (t). Значения считали статистически достоверными при р≤0,05.
Результаты исследования и обсуждение
Средний возраст женщин составил 31,3±7,9 года и варьировал от 18 до 45 лет.
Наиболее распространенными из факторов риска венозных тромбо-эмболических осложнений (ВТЭО) в исследуемой когорте были варикозное расширение вен нижних конечностей, которое диагностировано у 79,2% (42/53) пациенток, возраст старше 35 лет – 62,4% (33/53), малоподвижный образ жизни – 60,4% (32/53), использование КОК – 43,4% (23/53), курение и ожирение – по 33,9% (по 18/53), отягощенный семейный анамнез по тромбозам/генетически подтвержденная тромбофилия – 20,8% (11/53), беременность – 17,0% (9/53), послеродовый период – 7,5% (4/53).
К так называемым специфическим «репродуктивным» факторам риска венозных тромбозов у женщин относят беременность, послеродовой период и гормональную контрацепцию [1].
В исследуемой когорте пациенток удельный вес ВТЭО, непосредственно ассоциированных с беременностью или использованием КОК, существенно превышал другие причины и составил 67,9% (36/53). При этом у 63,9% (23/36) пациенток репродуктивного периода основным триггером развития первичных ВТЭО явился прием КОК, у 36,1% (13/36) – беременность и послеродовый период.
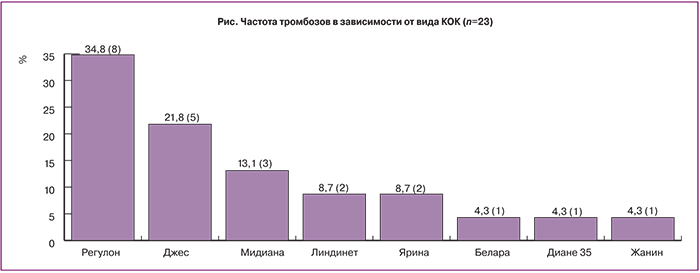
На рисунке представлена частота венозных тромбозов в зависимости от вида гормонального орального контрацептива, на фоне которого возникли ВТЭО. В анализируемой когорте наибольшее число женщин принимали регулон – 34,8% (8/23), джес – 21,8% (5/23), мидиану – 13,1% (3/23), линдинет-30 и ярину – по 8,7% (по 2/23), белару, диане-35, жанин – по 4,3% (по 1/23).
У всех пациенток тромбозы на фоне КОК развились в первые 4 месяца приема препарата, что согласуется с данными других авторов о повышенной тромбоопасности КОК в течение первых 3–6 месяцев их использования [6, 7].
Следует особо отметить, что 22 из 23 пациенток (95,7%) с ВТЭО, возникшими при приеме КОК, имели сопутствующие факторы риска тромбозов. Наиболее распространенным фоновым фактором риска ВТЭО был возраст 35 лет и старше – 60,9%. Далее в порядке ранжирования распределились варикозная болезнь вен нижних конечностей – 39,1%, малоподвижный образ жизни – 34,8%, курение – 30,4%, ожирение (индекс массы тела ³30 кг/м2) – 26,1%, наследственные тромбофилии и/или отягощенный семейный анамнез по тромбозам (у ближайших родственников) – 21,7%.
Согласно современным сведениям, применение КОК в течение первого года после родов существенно повышает риск ВТЭО [8]. В исследуемой нами группе 13% женщин начали прием КОК через 3–6 месяцев после родов.
В последние годы получено большое количество доказательств того, что эндокринопатии модулируют нарушения гемостатического баланса, при этом нарушения коагуляции и фибринолиза варьируют от легких лабораторных изменений до клинически серьезных тромботических событий [9, 10]. Обнаружена взаимосвязь между увеличением уровня пролактина, агрегационной активностью тромбоцитов и повышением фактора VIII и фактора фон Виллебранда [11]. Выявлен дозозависимый эффект уровня пролактина и риска ВТЭО: при уровне пролактина 8 г/л относительный риск тромбозов составил 1,7 (95% ДИ 1,0–2,7), при 16 г/л – повысился до 4,7 (95% ДИ 1,8–11,8) по сравнению с концентрацией до 6 г/л (ниже 50-го перцентиля) [12].
Согласно полученным нами данным, у 13,0% женщин с первичными тромбозами, индуцированными приемом КОК, имелись эндокринные заболевания (болезни щитовидной железы с нарушением функции – 8,7%, микропролактинома – 4,3%).
В среднем на одну пациентку с ВТЭО, использующую гормональную контрацепцию, пришлось 3,4±0,1 фактора риска тромбоза. У 21,7% (5/23) женщин этой группы тромбоз илеофеморальных и подвздошных вен осложнился ТЭЛА. Их средний возраст составил 35,0±7,8 года (от 25 до 45 лет), все они имели от 3 до 7 факторов риска (в среднем 4,8±0,4).
Многочисленные источники литературы свидетельствуют о повышенном риске ВТЭО при использовании КОК, содержащих ципротерона ацетат, а также прогестагены третьего (гестоден, дезогестрел) и четвертого (дросперинон) поколения по сравнению с первым и вторым (хлормадинон, левоноргестрел) [1, 13–16].
Европейское медицинское агентство в своей резолюции от 29 мая 2013 года особо подчеркнуло, что польза назначения препаратов, содержащих этинилэстрадиол/ципротерона ацетат (диане-35 и его дженерики), перевешивает риски при условии, что приняты меры, чтобы минимизировать риск тромбоэмболии. Эти лекарственные средства должны использоваться исключительно при лечении умеренных и тяжелых акне, связанных с гиперандрогенией, или при гирсутизме у женщин репродуктивного возраста. Кроме того, диане 35 используют для лечения угрей, когда альтернативные методы лечения (местная терапия и оральная антибиотикотерапия) оказались неэффективными [17].
Нами не выявлено повышенной частоты ВТЭО у пользовательниц КОК, содержащих третью и четвертую генерации прогестагенов, а также ципротерона ацетат (рисунок). При этом отмечено, что женщины, принимающие КОК с прогестагенами первого и второго поколения имели большее число факторов риска тромбозов, чем использующие КОК с прогестагенами третьей и четвертой генерации: в среднем у одной пациентки выявлено 5,0±0,3 фактора риска против 3,2±0,2 соответственно (p<0,05). Так, на одну пациентку, использующую хлормадинон-содержащий КОК, пришлось 4,0 фактора риска ВТЭО, диеногест – 6,0±0,3, гестоден – 3,0±0,2, дезогестрел – 3,4±0,1, дросперинон – 3,2±0,2, ципротерона ацетат – 3,0±0,2 Полученные факты совпадают с мнением других исследователей и позволяют сделать заключение о многофакторности причин тромбозов у пользовательниц КОК [1, 3, 16, 18].
С целью уменьшения риска ВТЭО назначать КОК должен медицинский специалист с учетом критериев их приемлемости, при этом должны быть приняты во внимание и обсуждены с женщинами различные свойства и побочные эффекты препаратов [14, 17, 19].
Беременность и послеродовый период явились основным триггером развития первичных ВТЭО у 24,5% (13/53) пациенток, что составило 36,1% (13/36) в структуре «репродуктивных» причин тромбозов.
Абсолютно все пациентки этой когорты имели описанные выше сопутствующие факторы риска, а у 61,5% женщин дополнительно выявлены от одного до трех акушерских фактора – преэклампсия, кесарево сечение, анемия [5, 20–22]. На одну беременную в среднем пришлось 2,7±0,1, на родильницу – 4,0±0,2 ко-фактора риска тромбоза, а общее число факторов риска на одну женщину этих групп составило 3,7±0,2 и 5,0±0,1 соответственно.
Наиболее распространенными фоновыми факторами риска тромбозов у беременных были курение и ожирение – по 44,4%. Второе по частоте встречаемости место заняли варикозная болезнь вен нижних конечностей, анемия средней степени тяжести, малоподвижный образ жизни, отягощенный семейный анамнез (тромбозы у близких родственников) – по 33,3%. Наследственные тромбофилии находились на третьем ранговом месте – их удельный вес составил 22,2%. С наименьшей частотой зарегистрированы преэклампсия и заболевания органов эндокринной системы (диффузный зоб с нарушением функции) – по 11,1%.
Основными ко-факторами риска тромбозов у родильниц были кесарево сечение и варикозная болезнь вен нижних конечностей – по 75,0%. Половина этих женщин (50%) находились в возрасте старше 35 лет (средний возраст 37,8±2,5 года), вели малоподвижный образ жизни, особенно при беременности, страдали ожирением и анемией. Отягощенный семейный анамнез по тромбозам отметили 25% пациенток этой группы.
В крупномасштабном когортном исследовании M. Blondon и соавт. (2015) продемонстрирована взаимосвязь низкой массы тела новорожденного и тромботического события у матери в послеродовом периоде [23]. Ранее нами показано, что при задержке роста плода имеются нарушения в системе гемостаза матери (снижена концентрация антитромбина III, интенсивно потребляется плазминоген, повышено содержание продуктов деградации фибрина), увеличивается концентрация суммарных антител к тканевому фактору (FIII) в 5 раз по сравнению с беременными, имеющими нормальную массу тела плода (35,1±7,9 против 175,8±14,6 нг/мл, р<0,001); в околоплодных водах появляется фактор Виллебранда и повышается их прокоагулянтная активность [24]. Однако в настоящем исследовании нами не выявлено ассоциативной связи между массой плода и ВТЭО у матери – маловесных детей у включенных в исследование пациенток не было.
Суммируя полученные сведения, следует заключить, что 52,5% (21/40) ко-факторов риска ВТЭО у беременных и родильниц были управляемыми (курение, ожирение, малоподвижный образ жизни, дисфункция щитовидной железы, анемия), а 15,0% (6/40) – условно управляемыми (варикозная болезнь вен нижних конечностей), то есть они должны быть устранены на этапе преконцепционной подготовки, в гестационном и пуэрперальном периоде. В этом аспекте особое значение приобретают прегравидарная коррекция веса и имеющихся соматических нарушений, отказ от вредных привычек, физическая активность. Данная концепция поведения должна быть продолжена при беременности и в послеродовом периоде и дополнена лечебно-профилактическими мероприятиями, регламентированными соответствующими федеральными клиническими рекомендациями [5, 20, 21].
Заключение
КОК, беременность и послеродовый период являются триггерными факторами тромбозов у 67,9% пациенток репродуктивного периода. У 95,7% женщин с ВТЭО прием КОК сочетался с дополнительными факторами риска, основными из которых были возраст старше 35 лет, курение, ожирение, тромбофилия/отягощенный семейный анамнез по тромбозам. Беременные и родильницы с тромбозами имели от 2 до 5 сопутствующих факторов риска, из которых 67,5% были управляемыми и условно управляемыми. Таким образом, резервы снижения риска тромбозов у пользовательниц КОК: сбор анамнеза (семейный анамнез, тромбозы в анамнезе, акушерские факторы – синдром потери плода, курение и др.), соблюдение критериев приемлемости и рецептурный отпуск контрацептивов, обратная связь врача и пациентки, междисциплинарный подход у пациенток группы риска по ВТЭО. Пациенткам, планирующим беременность, следует оценить риски тромбозов на прегравидарном этапе, далее – при беременности и в послеродовом периоде, включить их в информацию пациента и предпринять меры по их устранению или минимализации.



