Эндометриоз – мультифакторное дисгормональное иммунозависимое и генетически детерминированное воспалительное заболевание с хроническим течением, при котором определяется наличие ткани, по морфологическим и функциональным свойствам подобной эндометрию вне полости матки [1–5].
Клинические проявления эндометриоза значительно варьируют – от выраженных тазовых болей, бесплодия, аномальных маточных кровотечений (АМК) до бессимптомных форм, которые представляют немалую проблему ввиду поздней диагностики [6–9]. Особую сложность представляет эндометриоз яичников у женщин молодого возраста из-за отсутствия четкой тактики ведения и необходимости сохранения фертильности у этой категории пациенток [10–13].
Наиболее распространенной классификацией в настоящее время является пересмотренная классификация Американской ассоциации репродуктивной медицины (r-ASRM), согласно которой оцениваются типы и локализация эндометриоидных очагов, внешний вид и глубина инфильтратов, наличие эндометриом и спаек [14]. Единая классификация эндометриоза, учитывающая многофакторность патогенеза и многогранность его клинических проявлений для определения тактики ведения пациенток, на данный момент отсутствует.
Цель исследования: анализ особенностей ведения пациенток с эндометриозом, прооперированных в гинекологическом отделении за 2 года, в аспекте персонализированной терапии эндометриоза. Анализ предпочтительной длительности применения дидрогестерона в контексте эффективной противорецидивной терапии эндометриоза.
Материалы и методы
Проведено ретроспективное исследование на базе клиники акушерства и гинекологии ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет им. академика И.П. Павлова» Минздрава России. Проанализировано 1417 историй болезни пациенток, прооперированных лапароскопическим доступом в 2022–2023 гг. Эндометриоз подтвержден у 438/1417 (30,9%) пациенток, из них 345/438 (78,8%) женщин репродуктивного возраста, старше 16 лет, были отобраны для дальнейшего анализа. 93/438 (21,2%) пациентки с аденомиозом или эндометриоидными кистами в сочетании с миомой матки и последующей гистерэктомией в возрасте старше 49 лет исключены из дальнейшего анализа.
В предоперационном периоде больным проводилось ультразвуковое исследование органов малого таза. У всех пациенток диагноз был в дальнейшем подтвержден гистологическим исследованием. При операциях по поводу эндометриом с целью сохранения овариального резерва использовали щадящие виды энергии (биполярная, ультразвуковая).
При статистической обработке данных характеристики пациенток представлены как среднее значение (M) со стандартным отклонением (SD), медиана (Me) с интерквартильным диапазоном (Q1; Q3) или количественными (n) и процентными (%) величинами.
Обсуждение предпочтительной длительности терапии проведено на основании как ретроспективных данных, так и отдельных клинических случаев применения противорецидивной терапии дидрогестероном более 48 месяцев.
Результаты
При характеристике обследованных групп отмечено, что средний возраст пациенток с эндометриозом составил 35,7 (7,3) года. Средний возраст менархе – 13,0 (1,4) года. Основными причинами обращения в клинику были тазовые боли – у 167/345 (48,4%) пациенток и бесплодие – у 95/345 (27,5%), при этом 83/345 (24,1%) пациентки госпитализированы в связи с другими причинами (сочетанием причин). У 302/345 (87,5%) женщин данное оперативное лечение по поводу эндометриоза было проведено впервые, 36/345 (10,5%) перенесли оперативное лечение эндометриоза ранее, 7 (2,0%) из них были оперированы 2 и более раз. В 88,1% случаев пациенткам ранее не проводилась медикаментозная терапия эндометриоза (табл. 1).
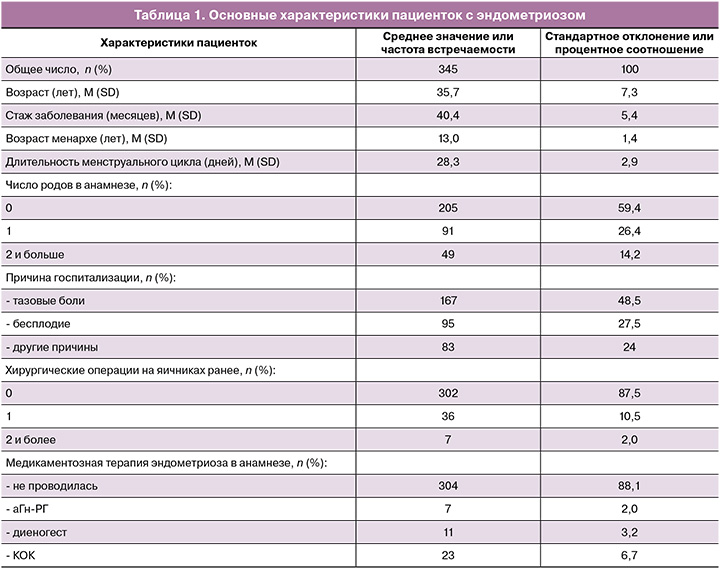
Для дальнейшего анализа были отобраны 292 больные в репродуктивном возрасте (16–49 лет). Пациентки были разделены на 2 группы по степени тяжести эндометриоза. В группу 1 вошли 104 пациентки с 1–2 стадиями, в группу 2 – 188 больных c 3–4 стадиями эндометриоза (табл. 2).
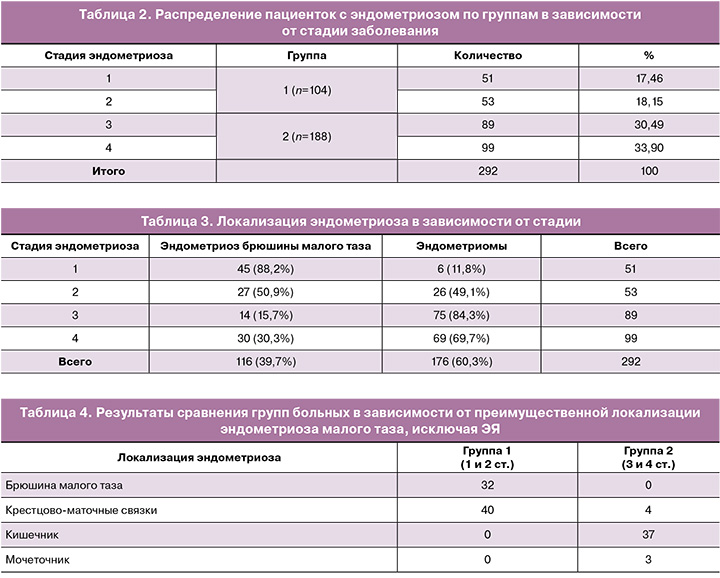
В группе 1 средний возраст составлял 35,6 (7,4) года, в группе 2 – 34,5 (6,5) года. Индекс массы тела (ИМТ) обследованных находился в пределах от 16,8 до 36,9 кг/м2; среднее значение – 23,1 (5,2)кг/м2. Среднее значение ИМТ в группе 1 составило 22,5 (5,2) кг/м2, в группе 2 – 22,7 (5,5) кг/м2. При сравнительной оценке значимых различий между группами по возрасту и ИМТ (р=0,23 и р=0,82 соответственно, критерий t-test) не обнаружено.
Эндометриомы яичников (ЭЯ) были выявлены у 176/292 больных эндометриозом (60,3%), остальные 116 пациенток прооперированы по поводу наружных форм эндометриоза с поражением тазовой брюшины различной степени тяжести – от поверхностных очагов до глубокого инфильтративного эндометриоза (ГЭ). У большинства больных были сочетанные эндометриоидные поражения, при которых отмечены ЭЯ и наличие инфильтративной формы различной степени тяжести. Для возможности дальнейшей статистической оценки мы принимали во внимание наиболее тяжелую по степени патологию (табл. 3).
Наибольшее число ЭЯ в проведенном исследовании отмечено у больных с 3–4 стадиями эндометриоза (р<0,0001).
Эндометриоз, локализованный исключительно на брюшине малого таза, значимо чаще встречался у пациенток с 1–2 стадиями заболевания (р=0,000002) (табл. 4).
При оценке проводимой противорецидивной терапии выявлено: не получали медикаментозную терапию 41/104 (39,4%) пациентка из группы 1 (с 1–2 стадиями эндометриоза), из них 24/41 (58,5%) только с перитонеальным эндометриозом и 17/41 (41,5%) – с эндометриомами небольших размеров. В группе 2 все пациентки с 3–4 стадиями эндометриоза после выписки из стационара получали гормономодулирующую терапию.
Среди пациенток 1-й группы первые 6 месяцев после операции агонисты гонадотропин-рилизинг-гормона (аГн-РГ) получали 2/63 (3,2%) женщины, 14/63 (22,2%) принимали диеногест 2 мг/сут, 13/63 (20,6%) получали дидрогестерон 20 мг/сут в непрерывном режиме. Во 2-й группе 122/188 (64,9%) пациентки получали аГн-РГ, 42/188 (22,3%) – диеногест 2 мг/сут, 15/188 (8%) – дидрогестерон 20 мг/сут в непрерывном режиме.
Длительность гормономодулирующего лечения у пациенток с эндометриозом варьировала до 24 месяцев (на момент опроса больных), Me (Q1; Q3)=6 (4; 7) месяцев.
Обнаружено, что у 9/345 (2,6%) пациенток (у 7 из 1-й группы (с 1–2 стадиями эндометриоза) и у 2 из 2-й группы (с 3–4 стадиями эндометриоза)) диагностирован рецидив эндометриоза за время проведения данного исследования. При анализе лечения пациенток с рецидивом эндометриоза определено, что все 7 пациенток из 1-й группы не получали гормономодулирующую противорецидивную терапию. Из двух пациенток 2-й группы с рецидивом эндометриоза одна получала комбинированные оральные контрацептивы (КОК) с целью контрацепции в течение 3 месяцев, отменила самостоятельно в связи со снижением либидо. Через год после самостоятельной отмены у нее вновь обнаружена эндометриома по данным УЗИ. У второй пациентки на фоне самостоятельной отмены терапии диеногестом (ввиду плохой переносимости) через 9 месяцев после операции диагностирован рецидив эндометриоза яичников.
Большинство пациенток не планируют беременность до 30 лет, что необходимо учитывать в персонифицированной тактике пролонгированной терапии эндометриоза на сроки достижения пациентами репродуктивных планов. Накоплен опыт ведения пациенток с эндометриозом с использованием дидрогестерона в пролонгированном циклическом режиме (20 мг/сут с 5-го по 25 дни менструального цикла) более 24 месяцев, ряд пациенток успешно продолжают терапию более 4 лет. При динамическом наблюдении на фоне проводимой терапии у всех пациенток отмечается купирование или значительное уменьшение тазовой боли и улучшение качества жизни в виде нормализации самочувствия, социально-ролевого функционирования, сексуальной жизни. За время терапии не отмечено нежелательных лекарственных реакций.
В качестве примера пролонгированного использования дидрогестерона приводим несколько клинических случаев из нашей практики.
Клиническое наблюдение № 1
Пациентка А., 21 год, проходила лечение в отделении онкогинекологии №7 ФГБОУ ВО «ПСПбГМУ им. акад. И.П. Павлова» Минздрава России с 15.03.2021 г. по 22.03.2021 г. Диагноз: Наружный генитальный эндометриоз IV ст. Двусторонние эндометриомы яичников. Эндометриоидный инфильтрат ректовагинальной перегородки, крестцово-маточных связок. Эндометриоидные гетеротопии брюшины мочевого пузыря. Синдром хронической тазовой боли (8 баллов по ВАШ). Дисменорея (10 баллов по ВАШ) и диспареуния (5 баллов по ВАШ). При УЗИ размеры ЭЯ слева 57×41×43 мм, справа 42×28×32 мм. Б – 0. Беременность не планировала.
16.03.2021 г. – Лапароскопия. Двусторонняя овариоцистэктомия. Иссечение эндометриоидного инфильтрата ректовагинальной перегородки. Резекция крестцово-маточных связок. Аргоноплазменная коагуляция эндометриоидных гетеротопий брюшины мочевого пузыря. Двусторонний сальпингоовариолизис. Левосторонний уретеролизис. Двусторонний нейролизис. Хромогидротубация. Установка противоспаечного барьера (рис. 1).
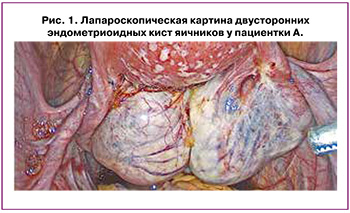
Гистологическое заключение: Эндометриоидный инфильтрат ректовагинальной перегородки (материал представлен стенкой влагалища, эпителиальная выстилка многослойным плоским эпителием типового строения. В строме перивазально и периневрально расположены множественные очаги эндометриоидной ткани). Эндометриоидные кисты правого и левого яичника. Эндометриоидное поражение крестцово-маточных связок (фиброзно-жировая ткань, признаки эндометриоидной гетеротопии).
В послеоперационном периоде пациентка получала противорецидивную гормономодулирующую терапию, дидрогестерон (Дюфастон) 10 мг 2 раза в день с 5-го по 25-й дни менструального цикла в пролонгированном режиме более 36 месяцев с системным динамическим наблюдением каждые 6 месяцев. На фоне проводимой терапии женщина отмечает улучшение состояния – боли при менструации значительно уменьшились (2 балла по шкале ВАШ), хроническая тазовая боль отсутствует, диспареуния отсутствует. По данным УЗИ, признаков рецидива эндометриоза не определяется. Репродуктивных планов нет. Терапию переносит хорошо, настроена продолжать лечение.
Клиническое наблюдение № 2
Пациентка К., 42 года, находилась в клинике акушерства и гинекологии ФГБОУ ВО «ПСПбГМУ им. акад. И.П. Павлова» Минздрава России в марте 2020 г. с жалобами на обильные менструации с менархе, альгоменорею до 8 баллов и диспареунию до 3 баллов по ВАШ. Диагноз эндометриоза установлен в 2018 г., спустя 2 года после дебюта жалоб. УЗИ органов малого таза: билатеральные кисты яичников: справа 3×4×4 см и слева 6×5×6 см, соответствующие по эхографическим характеристикам эндометриоидной кисте.
В 2018 г. выполнены лапароскопия, двусторонняя цистэктомия, адгезиолизис. После оперативного лечения пациентка получала терапию диеногестом 2 мг, отменила самостоятельно.
Через 2 месяца после возобновления менструаций пациентка отметила альгоменорею до 8 баллов по ВАШ, диспареунию до 2 баллов по ВАШ. Пациентка использовала анальгетики с временным положительным эффектом. Консультирована гинекологом по месту жительства, гормономодулирующая терапия не назначалась.
В 2020 г. по данным УЗИ и МРТ органов малого таза с контрастированием признаки рецидива эндометриоза: правый яичник 3,4×2,6 см, локализован у правого ребра матки с наличием кистозных включений с высокобелковым (геморрагическим) содержимым, размерами о 2,2×1,5 см. Левый яичник значительно увеличен в размерах до 6,8×4,2 см, содержит кистозные включения с высокобелковым (геморрагическим) содержимым от 0,6 до 4,2 см, МР-признаки эндометриоидного инфильтрата в ретроцервикальном пространстве размерами 2,4–2,8 см, спаечного процесса в малом тазу (рис. 2).
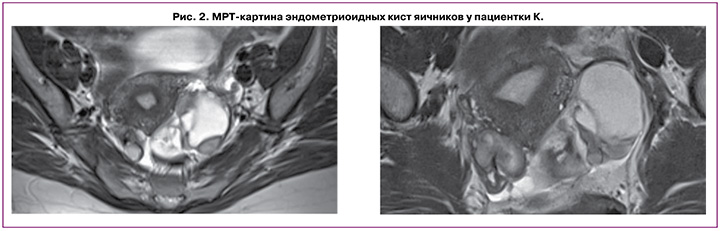
Данные онкомаркеров: СА-125 – 45 ммоль/л, НЕ4, индекс ROMA – в пределах референсных значений, уровень антимюллерова гормона (АМГ) – 1,3 нг/мл.
Принимая во внимания жалобы пациентки, рецидив эндометриоза, было запланировано плановое оперативное лечение. Рекомендована консультация репродуктолога с целью решения вопроса о криоконсервации ооцитов или эмбрионов до оперативного лечения, однако репродуктолога не посетила в связи с отсутствием репродуктивных планов.
27.03.2020 г. проведено оперативное лечение: лапароскопия, иссечение эндометриоидного инфильтрата обеих крестцово-маточных связок, мочевого пузыря, брюшины, двусторонняя цистэктомия, адгезиолизис, сальпингоовариолизис, двусторонний уретеролизис, двусторонний нейролизис, хромогидротубация.
Гистологическое исследование: 1) участок эндометриальной ткани с железами пролиферативного типа, множественные очаговые кровоизлияния, признаки хронического эндометрита; 2) фиброзно-жировая ткань с локусами эндометриоидной эктопии; 3) участки стенок эндометриоидных кист.
Послеоперационный период без осложнений. Рекомендована противорецидивная гормономодулирующая терапия дидрогестероном (Дюфастон) 10 мг 2 раза в день с 5-го по 25-й дни менструального цикла длительно, до планирования беременности.
На фоне комбинированного лечения эндометриоза через 6 месяцев отмечено полное отсутствие болевого синдрома при менструации и половой жизни. Пациентка продолжала принимать дидрогестерон по 10 мг 2 раза в день с 5-го по 25-й дни менструального цикла до 2023 г.
В 2023 г. запланировала беременность. Овариальный резерв: АМГ – 0,51 нг/мл, эстрадиол, ФСГ, ЛГ, онкомаркеры – в рамках референсных значений. Пациентке была рекомендована консультация репродуктолога, однако в связи с крайней заинтересованностью в самостоятельной беременности схема терапии дидрогестероном была скорректирована до 10 мг 2 раза в день с 16-го по 25-й дни менструального цикла, даны рекомендации по планированию беременности. При динамическом осмотре пациентки в 2024 г., после более 48 месяцев непрерывной терапии дидрогестероном, отмечен значимый клинический эффект в отношении купирования болевого синдрома. Женщина отмечает высокий уровень качества жизни, снижение проявления болей со стороны органов репродуктивной системы. Не отмечено наличия проявлений нежелательных лекарственных реакций, снижения комплаентности к терапии. Пациентке даны повторные рекомендации о необходимости консультации репродуктолога и рассмотрения варианта применения вспомогательных репродуктивных технологий. Терапия дидрогестероном продолжена в соответствии с алгоритмами терапии эндометриоза, до наступления менопаузы с перерывом на поздние сроки беременности и лактацию [15]. Нежелательных лекарственных реакций не отмечено.
Обсуждение
В представленном ретроспективном исследовании основные характеристики пациенток были связаны со степенью тяжести эндометриоза и наличием ЭЯ. Средний возраст больных эндометриозом составил 35,7 (7,3) года. По данным литературы, чаще всего эндометриоз диагностируется в возрасте 25–29 лет, реже после 44 лет [16–19].
Известно, что у женщин, перенесших хирургическое лечение по поводу хронической тазовой боли или бесплодия, эндометриоз представляет одну из наиболее распространенных патологий органов малого таза [20–23].
В проведенном исследовании наибольшее число ЭЯ обнаружено среди пациенток с 3–4 стадиями наружного эндометриоза (р<0,0001). Эндометриоз повреждает ткань яичников, отрицательно влияя на их функцию и нарушая физиологические репродуктивные механизмы, потенциально прерывая спонтанную овуляцию. Эндометриоз и связанные с ним структурные изменения тканей в коре яичников могут быть причиной снижения овариального резерва [24]. Kim J.Y. et al. (2013) в своем исследовании сравнили сопоставимые по возрасту и индексу массы тела группы женщин, обследованных перед операцией, с эндометриомами и зрелыми тератомами яичников. До операции уровень АМГ в сыворотке крови был значительно ниже у пациенток с эндометриомами (особенно при 4 стадии заболевания) по сравнению с пациентками со зрелыми кистозными тератомами, что говорит о негативном влиянии эндометриоза на овариальный резерв даже без хирургического лечения [25]. В последнее время многие литературные данные подтверждают, что повторные оперативные вмешательства ухудшают прогноз заболевания в отношении фертильности и овариального резерва [26, 27]. В проведенном нами исследовании у 302/345 (87,7%) женщин данное оперативное лечение по поводу эндометриоза было первым, 36 (10,4%) пациенток ранее уже подвергались хирургическому лечению эндометриоза и 7 (1,9%) из них были оперированы 2 раза и более.
Целесообразно придерживаться противорецидивного подхода к терапии эндометриоза. Назначение гестагенов первой линией терапии рекомендуется после проведенного хирургического лечения эндометриоза и вплоть до менопаузы. В период наступления беременности и до 20 недель дидрогестерон также может быть использован в соответствии с актуальной характеристикой лекарственного препарата. После 20-й недели беременности и до завершения лактации предусмотрен перерыв в данной терапии. Следует учитывать потенциальные риски отмены терапии при наличии нежелательных реакций при приеме диеногеста. Учитывая риски со стороны репродуктивной системы, обязательно назначение патогенетической терапии, не подавляющей овуляцию. По нашему мнению, назначение гестагенов, не подавляющих овариальную функцию и позволяющих добиться лучших результатов качества жизни и реализации репродуктивных планов, рекомендуется как наиболее безопасный и эффективный метод лечения. По поводу рецидивов эндометриоза, их профилактики, необходимости длительной медикаментозной терапии эндометриоза также имеется множество публикаций.
Главная парадигма современного лечения эндометриоза состоит в том, что хирургическое лечение при данной патологии необходимо проводить строго при наличии показаний. При интраоперационном стадировании заболевания с учетом объема проведенной операции и репродуктивных планов пациентки обязательна индивидуально подобранная долгосрочная терапия [28–30] в соответствии с алгоритмами терапии эндометриоза [15].
Заключение
На основании многочисленных исследований можно утверждать, что хирургическое лечение при эндометриозе необходимо проводить строго при наличии показаний с обязательным интраоперационным стадированием заболевания. С учетом того факта, что многие пациентки имеют репродуктивные планы только после 30 лет, для профилактики рецидивов заболевания им необходима индивидуально подобранная долгосрочная терапия. Дидрогестерон позволяет обеспечить длительную, более 48 месяцев, эффективную противорецидивную терапию при благоприятном профиле безопасности.



