Актуальность проблемы
Неиммунная водянка плода (НИВП) – это патологическое состояние, характеризующееся скоплением жидкости в двух и более серозных полостях плода, включая отек кожи, асцит, плевральный выпот, гидроперикард и др. По данным зарубежных исследований, частота встречаемости НИВП колеблется от 1:1700 до 1:3000 случаев и составляет около 90% случаев водянки плода. Несмотря на успехи в области перинатальной медицины, летальность при НИВП колеблется в пределах 55–98%.
В связи с тем что заболеваемость и смертность зависят от причины НИВП, понимание этиологии имеет важное значение для определения прогноза для плода, тактики ведения беременности, информирования родителей о целесообразности пролонгирования беременности, риске преждевременных родов, возможной необходимости антенатальной и постнатальной терапии матери, плода и новорожденного. В основе неиммунной водянки плода лежат различные этиологические причины (более 150 нозологий), однако в 44% случаях причины остаются неизвестными.
Было установлено, что одной из причин водянки является группа генетических нарушений – синдром Бругада. Первые генетические находки, которые связали с развитием синдрома Бругада, были обнаружены в гене SCN5A. Мутации в этом гене приводят к изменению ионной проницаемости мембран кардиомиоцитов, вследствие чего возникают патологии сердечного ритма и проводимости, создающие повышенный риск внезапной сердечной смерти.
Манифестация данной патологии может произойти в любом возрасте – от нескольких дней жизни до 80 лет, но преимущественно встречается среди молодых мужчин в возрасте 35–45 лет, обычно во время сна или отдыха в связи с усилением парасимпатической стимуляции.
Основные клинические проявления (в том числе как первые и фатальные) – потеря сознания и остановка сердца, обусловленные приступом желудочковой тахикардии, который обладает высоким риском трансформации в жизнеугрожающую фибрилляцию желудочков.
В мировой литературе описано всего 2 клинических случая развития тяжелой аритмии и неиммунной водянки у плода при патогенном варианте в гене SCN5A (в сочетании патогенной мутации и частого полиморфизма rs1805124).
В рамках перинатального консилиума ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Минздрава России (Центра) на 2022 г. было диагностировано 2 случая синдрома Бругада. Исследования были выполнены в Институте репродуктивной генетики Центра под руководством д.б.н., проф. Трофимова Д.Ю.
Клиническое наблюдение № 1
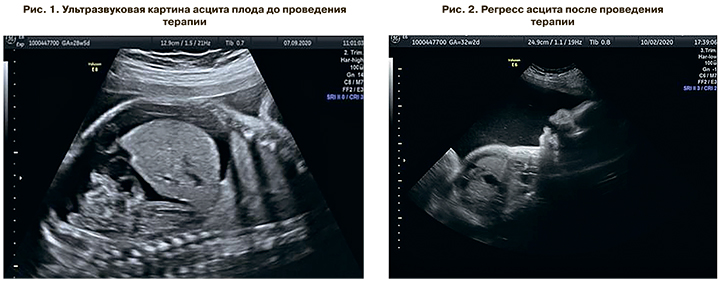
В 2020 г. на перинатальный консилиум Центра обратилась пациентка, первая беременность которой завершилась в сроке 32 нед антенатальной гибелью плода с признаками неиммунной водянки (анасарка, асцит, гидроторакс, гидроперикард) (рис. 1). При обследовании у пациентки была диагностирована неполная блокада правой ножки пучка Гиса, блокада передневерхней ветви левой ножки пучка Гиса. В данную беременность в сроке 27 нед была вновь диагностирована НИВП. С 33 нед беременная получала терапию β-блокаторами (бисопролол – 2,5 мг), на фоне которой наблюдался полный регресс явлений НИВП (рис. 2).
В рамках диссертационной работы Кадырбердиевой Ф.З. под руководством д.м.н., проф. Шмакова Р.Г. и д.м.н., проф. Бокерия Е.Л. при проведении полноэкзомного секвенирования на антенатальном этапе были диагностированы мутации в гене SCN5A, что позволило объяснить этиологию водянки плода и своевременно начать терапию на антенатальном этапе.
Клиническое наблюдение № 2
В 2021 г. на перинатальный консилиум Центра обратилась пациентка, у которой первая беременность завершилась рождением здорового ребенка, вторая беременность – внематочная (лапароскопия, туботомия справа), а третья беременность завершилась гибелью ребенка на 2-е сутки жизни в связи с сердечной недостаточностью, был диагностирован синдром гипоплазии левых отделов сердца. Данная, четвертая, беременность протекала без осложнений, и в 26 нед по результатам УЗИ впервые была выявлена НИВП. В 29 нед в Центре была проведена инвазивная диагностика, подтвержден нормальный женский генотип. Однако, учитывая снижение систоло-диастолической функции миокарда плода, была начата трансплацентарная терапия Дигоксином под контролем его уровня в крови матери. После рождения ребенок был консультирован кардиологом, д.м.н., проф. Бокерия Е.Л., и в качестве патогенетической терапии при синдроме удлиненного интервала QT был назначен атенолол.
Выводы
По-видимому, при НИВП неясной этио-логии подобные редкие причины могут иметь место. Вероятно, формируется аритмогенная активность, которая вызывает нарушение ритма сердца плода внутриутробно, что и приводит к формированию НИВП. При своевременной диагностике данного состояния может быть проведена коррекция β-блокаторами.
Таким образом, необходимо дальнейшее исследование для определения необходимости антенатального тестирования на данную группу генов у беременных с НИВП для подбора терапии внутриутробно и после рождения.
Люшнина Д.Г., Бокерия Е.Л., Шубина Е., Тетруашвили Н.К.
НМИЦ АГП им. акад. В.И. Кулакова, Москва



