Хроническая артериальная гипертензия (ХАГ) – повышение артериального давления (АД) ≥140/90 мм рт. ст. до беременности или в течение первых 20 недель беременности, которое обычно сохраняется в течение более 42 дней после родов [1, 4].
Гестационная (индуцированная беременностью) артериальная гипертензия (ГАГ) – повышение АД, впервые зафиксированное после 20-й недели беременности и не сопровождающееся значимой протеинурией (<0,3 г/л) [1, 4]. В 25% случаях ГАГ, развившаяся ранее 34 недель беременности, сопровождается преэклампсией (ПЭ) [1, 4, 5].
Гипертоническая болезнь (ГБ) – хронически протекающее заболевание, проявлением которого является АГ, при отсутствии других заболеваний или патологических процессов, для которых также характерно повышение АД [1, 4].
Умеренная ПЭ – осложнение беременности, родов и послеродового периода, характеризующееся повышением после 20-й недели беременности систолического АД (САД) ≥140 мм рт. ст. и/или диастолического АД (ДАД) ≥90 мм рт. ст. независимо от уровня АД в анамнезе в сочетании с протеинурией ≥0,3 г в сутки или ≥0,3 г/л в 2 порциях мочи, взятых с интервалом 6 ч.
Тяжелая ПЭ – осложнение беременности, родов и послеродового периода, характеризующееся повышением после 20-й недели беременности САД≥160 мм рт. ст. и/или ДАД≥110 мм рт. ст. независимо от уровня АД в анамнезе в сочетании с протеинурией ≥5 г в сутки или ≥3 г/л в 2 порциях мочи, взятых с интервалом 6 ч, или хотя бы одним другим параметром, свидетельствующим о присоединении полиорганной недостаточности [4].
Эклампсия – серия судорог, сначала тонических, а затем клонических, которые, как правило, возникают на фоне тяжелой ПЭ при отсутствии других причин [4].
HELLP-синдром – осложнение тяжелой ПЭ, характеризующееся гемолизом, повышением печеночных трансаминаз (АЛТ, АСТ) и тромбоцитопенией [4]. HELLP-синдром возникает у 4–12% женщин с тяжелой ПЭ и является потенциально смертельным ее осложнением (тяжелая коагулопатия, некроз и разрыв печени, кровоизлияние в мозг).
Клиническая картина
Для классической формы заболевания характерна триада симптомов: АГ, протеинурия и отеки, явные или скрытые [19–21]. Однако отеки не являются обязательным диагностическим критерием ПЭ. Для тяжелой ПЭ характерно также наличие дополнительных параметров, свидетельствующих о присоединении полиорганной недостаточности. Диагноз тяжелой ПЭ устанавливается при наличии АГ в сочетании с хотя бы одним из следующих симптомов: генерализованные отеки (особенно внезапно появившиеся); со стороны ЦНС – головная боль, нарушение зрения, отек зрительного нерва и др.; диспептические расстройства – тошнота, рвота; боли в эпигастрии или в правом верхнем квадранте; олигурия <500 мл/сут (<30 мл/ч); отек легких, цианоз; повышение АЛТ, АСТ в крови ≥40 МЕ/л; тромбоцитопения <50 000/мкл; повышение уровня креатинина в крови ≥90 мкмоль/л; гемолиз в периферической крови; HELLP-синдром.
Комментарий: Для подтверждения диагноза ПЭ также возможно определять соотношение ангиогенных факторов sFLT/PlGF [72, 182, 183], что является надежным, но пока еще малодоступным методом исследования. Соотношение sFlt/PlGF <38 исключает развитие ПЭ в течение 7 дней. При сроке беременности <34 недель соотношение sFlt/PlGF >85, а в сроке беременности >34 недель соотношение sFlt/PlGF >110 указывает на высокую вероятность развития ПЭ.
Однако эти показатели не являются универсальными, возможны и другие пороговые значения соотношения sFlt/PlGF, разработанные лабораториями или предоставленные компаниями-разработчиками [184–186].
Симптомы – предвестники эклампсии. Эклампсия
Об угрозе эклампсии у беременной с ПЭ свидетельствуют появление неврологической симптоматики, нарастание головной боли, нарушения зрения, боли в эпигастрии и в правом подреберье, периодически наступающий цианоз лица, парестезии нижних конечностей, боли в животе и нижних конечностях без четкой локализации, одышка, возбужденное состояние или, наоборот, сонливость, затрудненное носовое дыхание, покашливание, сухой кашель, слюнотечение, боли за грудиной. Однако 25% женщин не имеют каких-либо предшествующих симптомов [22, 23]. Судороги могут возникнуть во время беременности, родов и в послеродовом периоде [16–18, 22, 24, 25].
Тромботическая микроангиопатия (ТМА) (МКБ-10 M31.1) – синдром, характерный для ряда разрозненных заболеваний, проявляющихся тромбоцитопенией, микроангиопатической гемолитической анемией, микроваскулярным тромбозом концевых артериол и капилляров и множественной дисфункцией органов [28, 29]. В эту группу входят болезни, как связанные с беременностью (HELLP-синдром, атипичный гемолитико-уремический синдром (а-ГУС)), так и не связанные с ней (ТТП, типичный гемолитико-уремический синдром (ГУС).
Массивный внутрисосудистый гемолиз, определяемый визуально в сыворотке крови и по характерному бурому цвету мочи, встречается только у 10% пациенток. Для уточнения диагноза внутрисосудистого гемолиза необходимо дополнительно получить данные лабораторных исследований:
- наличие фрагментированных эритроцитов (шизоцитов) (норма 0–0,27%);
- уровень лактатдегидрогеназы (ЛДГ) >600 МЕ/л;
- уровень непрямого билирубина >12 г/л;
- снижение уровня гаптоглобина <0,3 г/л.
HELLP-синдром диагностируется на основании следующих признаков: свободный гемоглобин в сыворотке и моче (Hemolysis), повышение ACT, AЛT (Elevated Liver Enzimes) и тромбоцитопения (Low Platelets). HELLP-синдром возникает у 4–12% женщин с тяжелой ПЭ и является потенциально смертельным ее осложнением (тяжелая коагулопатия, некроз и разрыв печени, кровоизлияние в мозг). В зависимости от набора признаков выделяют полный HELLP-синдром и ELLP-синдром при отсутствии гемолитической анемии. Тромбоцитопения – обязательное условие для диагноза HELLP-синдрома. В настоящее время HELLP-синдром рассматривается как один из частных случаев ТМА, связанных с беременностью. Клиническая картина HELLP-синдрома вариабельна и включает следующие симптомы:
- боли в эпигастрии или в правом верхнем квадранте живота (86–90%);
- тошнота или рвота (45–84%);
- головная боль (50%);
- чувствительность при пальпации в правом верхнем квадранте живота (86%);
- ДАД ≥110 мм рт. ст. (67%);
- массивная протеинурия (>5 г/сут; 85–96%);
- отеки (55–67%);
- АГ (80%).
У каждой третьей женщины с HELLP-синдромом первые клинические симптомы появляются в первые часы после родоразрешения. При отсутствии регресса клинических проявлений ПЭ/HELLP-синдрома в течение 48–72 ч после родоразрешения следует диагностировать другие варианты ТМА [46, 47]. Разграничение «чистых акушерских» ТМА, то есть тех вариантов, когда сама беременность запускает реализацию ТМА (ПЭ/HELLP-синдром), от других вариантов ТМА (ТТП, а-ГУС) возможно только после родоразрешения. Только уровень ADAMTS-13<10% позволяет установить диагноз ТТП, другие клинико-лабораторные алгоритмы позволяют лишь предположить диагноз.
Диагноз а-ГУС следует считать диагнозом исключения, который устанавливается на основании наличия симптомов ТМА, персистирующих после родоразрешения, и должен быть подтвержден лабораторными данными, исключающими другие ТМА, прежде всего ТТП и септические вторичные ТМА.
- Рекомендована профилактика РДС плода у пациенток с тяжелой ПЭ с 24 до 336 недель беременности по схеме согласно клиническим рекомендациям «Преждевременные роды» [131]. (А-1)
Родоразрешение
- Не рекомендована профилактика РДС плода при родоразрешении в сроке <24 недель и >34 недель беременности за исключением особых ситуаций (см. Клинические рекомендации «Преждевременные роды») [132, 133].
- Рекомендовано родоразрешение в экстренном порядке при кровотечении из родовых путей, подозрении на преждевременную отслойку нормально расположенной плаценты (ПОНРП), острую гипоксию плода [134].
- При ПЭ рекомендовано родоразрешение в неотложном порядке после стабилизации состояния при постоянной головной боли и нарушении зрения; постоянной эпигастральной боли, тошноте или рвоте; прогрессирующем ухудшении функции печени и/или почек; эклампсии; артериальной гипертензии, не поддающейся медикаментозной коррекции; количестве тромбоцитов <100×109/л; нарушении состояния плода по данным КТГ; отрицательном или нулевом кровотоке в артерии пуповины; нулевом или отрицательном кровотоке в венозном протоке; ЗРП <5 перцентиля и одновременной патологии фетальной или фетоплацентарной перфузии (нулевой или реверсный кровоток в маточной артерии); выраженном маловодии (<5 см) в 2 исследованиях с интервалом 24 ч при сроке беременности более 30 недель [135–139].
- При ГАГ и умеренной ПЭ в сроке с 240 до 336 недель беременности первоначально рекомендована выжидательная тактика ведения [18, 40, 140, 141], которая возможна под строгим динамическим наблюдением за состоянием матери и плода до достижения гестационного срока 376 недель [2, 142]. При выявлении отрицательной тенденции в состоянии матери или плода показано родоразрешение [18, 40, 143].
- Клинические ситуации, исключающие выжидательную тактику [4, 16–18, 40] со стороны матери: тяжелая ПЭ и предвестники эклампсии (вне зависимости от срока беременности); неконтролируемое рефрактерное к терапии АД (≥160/110 мм рт. ст.); постоянные головные боли, не поддающиеся терапии; эпигастральная боль или боль в правом верхнем квадранте, не отвечающая на повторный прием анальгетиков; нарушение зрения, моторики или чувствительности; цереброваскулярные нарушения (инсульт); левожелудочковая недостаточность; инфаркт миокарда; PRES-синдром; новая или усугубляющаяся почечная дисфункция (креатинин сыворотки более чем в 2 раза выше исходного уровня); отек легких; эклампсия; подозрение на острую отслойку плаценты или влагалищное кровотечение при отсутствии предлежания плаценты; аномальные лабораторные тесты (повышение печеночных трансаминаз ≥500 МЕ/л); прогрессирующее снижение количества тромбоцитов <100×109/л; коагулопатия (МНО>2) в отсутствие альтернативных причин; преждевременное излитие околоплодных вод; HELLP-синдром [18, 40, 144]. Клинические ситуации, исключающие выжидательную тактику со стороны плода: дистресс-синдром плода; антенатальная гибель плода; летальные ВПР; крайняя недоношенность; постоянно отсутствующий или реверсный конечный диастолический кровоток в пуповинной артерии; постоянный реверсный диастолический поток в пуповинной артерии.
- При тяжелой ПЭ и ЗРП <5 перцентиля в сроке <336 недель беременности не рекомендовано родоразрешение при отсутствии отрицательной динамики в состоянии беременной и стабильном состоянии плода [40, 140, 141, 145, 146].
- При ГАГ или умеренной ПЭ рекомендовано родоразрешение в 376 недель беременности в качестве предпочтительной лечебной тактики [18, 40].
- Рекомендована индукция родов у беременных с хронической артериальной гипертензией и контролируемыми цифрами АД (до 160/110 мм рт. ст.) в 38–39 недель беременности [147–149].
- Рекомендована индукция родов у беременных с гестационной артериальной гипертензией с учетом ее тяжести и эффективности терапии в сроке 37 недель беременности и более в качестве предпочтительной тактики для снижения частоты материнских осложнений [18, 150].
- При тяжелой ПЭ рекомендована следующая тактика ведения беременности в зависимости от срока беременности: 22–24 недели – прекращение жизнеугрожающей беременности или при отсутствии жизнеугрожающей ситуации – родоразрешение через естественные родовые пути; 25–33 недели – пролонгирование беременности при отсутствии неконтролируемой АГ, прогрессирования органной дисфункции у матери, дистресс-синдрома плода, профилактика РДС плода, КС – по акушерским показаниям; ≥34 недель – лечение, подготовка, родоразрешение, КС – по акушерским показаниям [40]. (С-5)
- Рекомендовано родоразрешение через естественные родовые пути во всех случаях ПЭ (в том числе тяжелой) при готовности родовых путей (особенно у повторнородящих), при отсутствии абсолютных показаний к КС и удовлетворительном состоянии плода [16–18, 40, 146]. (С-5)
Комментарий: При тяжелой ПЭ и сроке беременности менее 32 недель предпочтительно КС, после 32 недель – родоразрешение через естественные родовые пути при головном предлежании плода [18].
- Рекомендовано вагинальное применение простагландинов при «незрелой» шейке матки с целью повышения шансов успешного влагалищного родоразрешения [18, 40, 146, 151].
- Рекомендовано КС при повышенной резистентности в сосудах пуповины, что почти вдвое снижает процент успешных вагинальных родов (>50%), а также при нулевом или реверсном кровотоке (по данным ультразвукового допплерометрического исследования) [18, 146]. (С-5)
Комментарий: Окончательный выбор метода родоразрешения должен основываться на анализе клинической ситуации, состояния матери и плода, возможностей учреждения, опыта врачебной бригады, информированном согласии пациентки.
- Рекомендована противосудорожная и антигипертензивная терапия на протяжении всего периода родоразрешения [4, 17, 18, 40, 79–83] с достижением целевых уровней САД<160 мм рт. ст. и ДАД<110 мм рт. ст. [6, 18]. (В-1)
Комментарий: В 3-м периоде родов для профилактики кровотечения вводят окситоцин 10 ЕД внутримышечно или 5 ЕД внутривенно капельно [146]. Введение указанных препаратов должно выполняться после нормализации АД.
- Не рекомендован метилэргометрин с целью профилактики кровотечения в 3-м и раннем послеродовом периоде (противопоказан при АГ) [16, 40, 91, 152]. (С-5)
- Для профилактики ранней послеродовой эклампсии во время и по окончании родоразрешения рекомендована инфузия магния сульфата в дозе 1,0 г/ч (в зависимости от показателей почасового диуреза) в течение не менее 24 ч [4, 16, 18, 40, 79–83, 153]. (В-1)
- Рекомендована документальная оценка факторов риска венозных тромбоэмболических осложнений непосредственно перед и после операции для назначения гепаринотерапии [154]. (С-5)
- В периоперационном периоде при отсутствии противопоказаний рекомендована эластическая компрессия нижних конечностей для снижения риска венозных тромбоэмболических осложнений [154]. (С-5)
Антигипертензивная терапия

Помощь пациентке с ПЭ в приемном покое
В приемном покое проводится оценка тяжести ПЭ по следующим показателям: АД, уровень сознания, головная боль, судороги, одышка, боли в животе, кровотечение из родовых путей, сердцебиение плода.
Врач анестезиолог-реаниматолог в обязательном порядке вызывается врачом акушером-гинекологом в приемный покой и начинает оказывать медицинскую помощь при следующих состояниях [1, 4, 24]:
- судороги (судороги в анамнезе);
- отсутствие сознания;
- высокое АД – выше 160/110 мм рт. ст.;
- нарушение дыхания;
- рвота;
- кровотечение из родовых путей (ПОНРП), геморрагический шок.
Ведение пациентки с ПЭ в отделении интенсивной терапии
Ведение пациентки с тяжелой ПЭ/эклампсией должно проводиться в условиях отделения анестезиологии-реанимации совместно врачом анестезиологом-реаниматологом и врачом акушером-гинекологом с привлечением, по мере необходимости, других смежных специалистов. Диагноз, показания и противопоказания к родоразрешению устанавливаются врачом акушером-гинекологом. Интенсивная терапия, метод анестезиологического обеспечения родоразрешения, необходимость привлечения профильных специалистов устанавливаются врачом анестезиологом-реаниматологом.
Принципы ведения:
1) оценка состояния;
2) наблюдение/мониторинг;
3) обследование;
4) контроль АД: терапия, направленная на снижение АД;
5) профилактика судорог: магния сульфат;
6) профилактика РДС плода: кортикостероиды;
7) контроль водного баланса;
8) решение вопроса о времени родоразрешения;
9) постоянная настороженность в послеродовом периоде;
10) профилактика отдаленных осложнений.
Катетеризация центральной вены не должна выполняться для контроля ЦВД и должна производиться только по показаниям: плохо развитая периферическая венозная система, шок ≥II, как дополнительный венозный доступ с целью обеспечения адекватной инфузионно-трансфузионной терапии.
Мониторинг основных параметров
Мониторинг со стороны матери:
- измерение АД: каждые 15 минут до достижения стабилизации, затем каждые 30 минут. В некоторых ситуациях, после всесторонней оценки возможен переход к менее частому измерению;
- наличие, распространенность отеков;
- состояние глазного дна;
- рефлексы ± судороги;
- анализы всех образцов мочи на белок;
- контроль диуреза;
- общий анализ крови;
- электролиты;
- мочевина, креатинин;
- печеночные ферменты (АЛТ, АСТ).
Мониторинг со стороны плода:
- КТГ (продолжительно, до стабилизации АД; непрерывно, если в родах) позволяет получить информацию о состоянии плода, но не дает информации в отношении прогноза [17, 63, 159, 160];
- УЗИ (фетометрия, амниотический индекс, плацентометрия) и допплерометрия (артерии пуповины, средние мозговые артерии) [17, 63, 160].
Режимы введения и мониторинга магния сульфата

Клинико-лабораторный контроль при введении магния сульфата
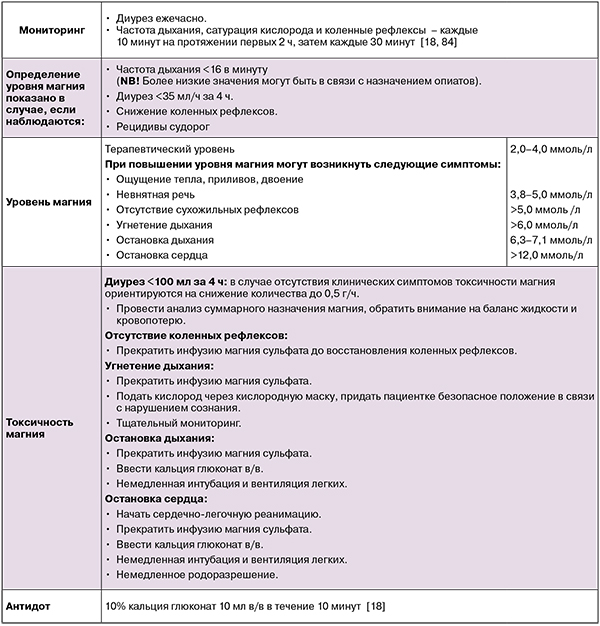
Первая помощь пациентке с ПЭ и эклампсией
Рекомендовано до приезда акушерско-анестезиологической реанимационной бригады, в условиях акушерских стационаров 1-й и 2-й групп, а также непрофильной бригады скорой медицинской помощи выполнить следующий объем медицинской помощи [1, 4, 24].
- Оценить тяжесть ПЭ: АД, сознание, головная боль, судороги, одышка, боли в животе, кровотечение из родовых путей, сердцебиение плода.
- Обеспечить венозный доступ: периферическая вена.
- Ввести магния сульфат 25% 16 мл внутривенно медленно (за 10 мин) и 100 мл через инфузомат со скоростью 1 г/ч (инфузия только раствора магния сульфата, разбавленная 0,9% раствором натрия хлорида).
- При АД выше 140/90 мм рт. ст. – гипотензивная терапия: метилдопа, нифедипин.
- При судорогах: обеспечить проходимость дыхательных путей.
- При отсутствии сознания и/или серии судорожных приступов – перевод на ИВЛ с тотальной миоплегией.
- При эвакуации пациентки с ПЭ/эклампсией линейной бригадой скорой медицинской помощи последняя должна оповестить акушерский стационар, куда транспортируется больная.
- При ПЭ с жизнеугрожающими клиническими проявлениями необходимо решение вопроса о родоразрешении после стабилизации состояния матери, при возможности, после проведения профилактики РДС плода при сроке беременности менее 34 недель и перевода матери в акушерский стационар 3-й группы.
Рекомендовано в стационаре наряду с клинической оценкой (включая рефлексы и клонус) выполнять следующие исследования:
- мониторинг АД;
- повторные исследования протеинурии;
- минимум 2 раза в неделю (при необходимости – чаще) анализы крови (гемоглобин, тромбоциты, АЛТ, АСТ, ЛДГ);
- тесты оценки функции почек, включая мочевую кислоту, почасовой диурез, при этом не использовать первую утреннюю мочу для количественной оценки протеинурии.
Наличие гиперурикемии у беременных с АГ свидетельствует о высоком риске нежелательных исходов со стороны матери и плода [57]. В ранние сроки беременности всем женщинам необходимо провести исследование на наличие протеинурии для выявления имеющихся заболеваний почек, а во второй половине беременности – с целью исключения ПЭ. Выявление протеинурии ≥1+ является показанием для быстрого определения соотношения альбумин-креатинин [4, 16, 18, 24, 40, 61].
Целью своевременного обращения является предоставление достаточного количества времени беременным и учреждению для того, чтобы в спокойной, плановой ситуации определить индивидуальный риск и выбрать дальнейший алгоритм наблюдения [18, 59].
Лечение массивного внутрисосудистого гемолиза
При установлении диагноза массивного внутрисосудистого гемолиза (свободный гемоглобин в крови и моче) и отсутствии возможности немедленного проведения гемодиализа консервативная тактика может обеспечить сохранение функции почек [129, 210–213]. В зависимости от клинической картины возможно несколько вариантов подобного лечения.
При сохраненном диурезе (>0,5 мл/кг/ч)
- При выраженном метаболическом ацидозе при рН<7,2 – введение 4% натрия гидрокарбоната 100 мл для предотвращения образования солянокислого гематина в просвете канальцев почек. Согласно инструкции, доза препарата для взрослых составляет 50–100 мл 4% или 5% раствора, детям в зависимости от возраста и массы тела от 3–8 мл/кг вводится в течение 4–8 ч.
- Внутривенное введение натрия хлорида из расчета 60–80 мл/кг массы тела со скоростью введения до 1000 мл/ч.
- Параллельная стимуляция диуреза фуросемидом 20 мг, дробно, внутривенно, для поддержания темпа диуреза – до 150–200 мл/ч [214].
- Индикатором эффективности проводимой терапии является снижение уровня свободного гемоглобина в крови и моче. На фоне объемной инфузионной терапии может ухудшаться течение ПЭ, но эта тактика позволит избежать формирования острого канальцевого некроза и острой почечной недостаточности [129].
При олиго- или анурии [129, 130, 211, 215]
Необходимо отменить магния сульфат и ограничить объем вводимой жидкости (только для коррекции видимых потерь) вплоть до полной отмены и начинать проведение почечной заместительной терапии (гемофильтрация, гемодиализ) при подтверждении почечной недостаточности:
- темп диуреза <0,5 мл/кг/ч в течение 6 ч после начала инфузионной терапии, стабилизации АД и стимуляции диуреза 100 мг фуросемида;
- нарастание уровня креатинина сыворотки в 1,5 раза, либо снижение клубочковой фильтрации >25%, либо развитие почечной дисфункции и недостаточности стадии «I» или «F» по классификации RIFLE или 2–3 стадии по классификации AKIN или KDIGO.
Алгоритмы действий врача

Во время проведения УЗИ I триместра рекомендовано измерить пульсационный индекс (PI) в маточных артериях для предикции ранней ПЭ. Оптимальный скрининг на ПЭ включает калькуляцию риска на основании оценки факторов риска, измерения среднего АД, PI в маточных артериях и определения плацентарного фактора роста (PlGF) [173–176] (например, калькулятор риска ПЭ, созданный фондом фетальной медицины – The Fetal Medicine Foundation). При отсутствии возможности определения PlGF скрининг на ПЭ включает калькуляцию риска на основании оценки факторов риска, измерения среднего АД и PI в маточных артериях [5]. PlGF является лучшим, но пока еще малодоступным биохимическим маркером. При высоком риске ПЭ низкие значения этого маркера свидетельствуют о высоком риске ранней ПЭ, часто в сочетании с ЗРП (частота ложноположительных результатов составляет 9%) [177].

Примечание. Поскольку настоящий Алгоритм составлен на основании Клинических рекомендаций «Преэклампсия. Эклампсия. Отеки, протеинурия и гипертензивные расстройства во время беременности, в родах и послеродовом периоде» (2021), нумерация ссылок по тексту приведена в соответствии с порядком цитирования в Клинических рекомендациях.



